Борани
Бораните са вид химични съединения, водородни съединения на бора. Открити са от немския химик Алфред Сток в периода 1912 – 1937 г., който и дал името им.[1] Могат да бъдат твърди, течни или газообразни. Съществуват няколко вида борани.
Синтезирани и характеризирани са от немския химик Алфред Сток в периода 1912 – 1937 г., който и дал името им. Той открил борани с общи формули BnH2n+4 и BnH2n+6. Тъй като леките борани са летливи, чувствителни на въздух и влага и токсични, Сток развива високовакуумни методи и апаратури за изследването им.
През 40-те години на 20 век започва тяхното интензивно изучаване.[2]
През Втората световна война правителството на САЩ финансира програми за намиране на летливи уранови компоненти за разделяне на изотопи.[1] През 1950 г., когато се отделят средства за развитие на високоенергийни горива за ракети и самолети, се открива, че бораните и производните им отделят много по-голямо количество топлина от въглеводородните горива.[1]
Наличие в природата[редактиране | редактиране на кода]
Физични свойства[редактиране | редактиране на кода]
Диборанът и тетраборатът(10) са газове, пента- и хескаборанът са течности, а останалите са твърди вещества. Техните точки на топене и кипене нарастват с увеличаване на комплексността и молекулната маса.[1]
| Формула | Наименование | TT, °C | TK, °C |
|---|---|---|---|
| B2H6 | диборан | -165,5 | -92,5 |
| B4H10 | тетраборан(10) | -120 | 16 |
| B5H9 | пентаборан(9) | -46,8 | 58,4 |
| B5H11 | пентаборан(11) | -123,3 | 65 |
| B6H10 | хексаборан(10) | -65,1 | 108 |
| B10H14 | декаборан(14) | 99,5 | 213 |
Леките борани са летливи. Те са безцветни, диамагнитни, с неприятна миризма, силно отровни при вдишване или попадане върху кожата.
Химични свойства[редактиране | редактиране на кода]
Борани[редактиране | редактиране на кода]
Бораните са термодинамично нестабилни съединения. Те не могат да се получат чрез пряка синтеза. Най-простият боран (BH3) не съществува при обикновени условия.[2]
Много реакционноспособни са и някои от тях с по-малка молекулна маса се самозапалват на въздуха. Горят със зелен пламък:[2]
.
Други характерни реакции за диборана са:[2]
,
,
,
.
Диборанът дава голям брой органични произдовни.
Химичните реакции, особено до леките борани, са аналогични с тези на диборана. Всички се отнасят като Люисови киселини и могат да реагиран с Люисови основи.[2] Разцепването на молекулата може да стане симетрично или несиметрично, например:

,
.
Последната реакция се извършва със силна Люисова основа.[2]
При по-тежките борани не се извършва разцепване, а депротониране:
.
Това се случва при превръщане на трицентрона двуелектронна връзка се превръща в двуцентрова двуелектронна връзка без съществено разрушаване:
.
В такъв случай бораните действат като Брьонстедови киселини и активността им нараства с увеличаване на молекулната маса – B4H10 < B5H9 < B10H14.
Това се обяснява с по-голямата делокализация на заряда при по-големите клъстери на бораните. Свойствата на бораните се обясняват с електронно-дефицитната химична връзка между атомите. Тя е причината в тези съединения да се образуват двуцентрови ковалентни B–H връзки, трицентрови мостови B–H┄B връзки, двуцентрови ковалентни В–В врзки, трицентрови В–В–В и многоцентрови борни връзки.
Борхидридни аниони[редактиране | редактиране на кода]
Най-простият борхидриден анион е тетрахидрогенборатният комплексен йон, BH4-, който е изоелектронен на CH4 и NH4+. Съединенията на алкалните метали с BH4- са най-стабилни. Те имат солеобразен характер с йонна връзка. Разтварят се добре във вода, течен амоняк, наякои амини и етери. Получават се от алкални хидриди при взаимодействие с B2H6 или BX3 в подходящ разтворител:
;
.
Най-използван е NaBH4. Намерен е промишлен метод за неговото полуаване от боракс, примесен с пясък:
.[2]
Натриевият тетрахидрогенборат се екстрахира от сместа с течен амоняк и от този разтвор се отделя бял прах. От него се получават тетрахидрогенборатите на дву- или тривалентните метали чрез обменна реакция във воден разтвор:
.
Литиевият, натриевият и калиевият тетрахидрогенборат са търговски продукти и широко се използват в органичния синтез.
Видове борани[редактиране | редактиране на кода]
Едноклъстерни борани[редактиране | редактиране на кода]
Съществуват няколко вида борани. Техните наименовани се образуват с посочване на броя на борните и водородните атоми и дескрипторна представка в наклонен шрифт, отделена от името с късо тире „-“ пред тях.[3]
| Дескриптор | Скелетни електронни двойки | Базов хидрид | Описание на структурата |
|---|---|---|---|
| хиперклозо- | n | BnHn | Нестабилна затворена полиедрена структура само с триъгълни страни. |
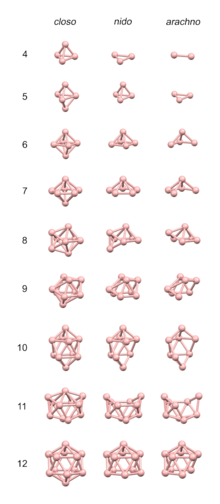
| клозо- | n+1 | BnH2n+2 | Затворена полиедрена структура само с триъгълни страни. |
| [BnHn]2-[2] | Открити са борхидридни аниони във вид на поледри с обща формула [BnHn]2-, наречени клозоборхидридни аниони.[2] Познати са аниони със състав n=5 до n=12. Клозо-борхидридите и техните карбонилни аналози са термодинамично стабилни съединения с умерена реакционна способност. | ||
| нидо- | n+2 | BnH2n+4 | Гнездоподобна, незатворена полиядрена структура. Заети са n върха на базовия (n+1)-атомен клозо полиедър. Името им произлиза от латинската дума „nidus“ – гнездо, защото имат структура, приличаща на гнездо.[2][BnHn]4- се получават при прибавяне на два електрона към клозо-[BnHn]2-, разтваряйки пирамидалната му струкура. |
| [BnHn]4-[4] | |||
| арахно- | n+3 | BnH2n+6 | Гнездоподобна, незатворена полиядрена структура. Заети са n върха на базовия (n+2)-атомен клозо полиедър. Името им произлиза от гръцката дума „ἀράχνη“ – паяжина, защото структурата им прилича на паяжина.[2] |
| хифо- | n+4 | BnH2n+8 | Гнездоподобна, незатворена полиядрена структура. Заети са n върха на базовия (n+3)-атомен клозо полиедър. Открити само в адукти. |
| кладо- | n+5 | BnH2n+10 | Гнездоподобна, незатворена полиядрена структура. Заети са n върха на базовия (n+4)-атомен клозо полиедър. |
| фиско-[4] | |||
| ретикуло-[4] | n+6 |
Тези представки не се използват за най-простите борани, които могат да бъдат разглеждани като получени от клозо-борани.
Полислъстерни борани[редактиране | редактиране на кода]
| Дескриптор | Описание на структурата |
|---|---|
| кладо- | разклонени клъстери |
| конюкто- | конюгирани клъстери |
| мегало- | множесто конюгирани клъстери |
Производни набораните[редактиране | редактиране на кода]
Ненаситени борани[редактиране | редактиране на кода]
Борените са производни на бораните, съдържащи двойна B=B връзка. Борините са производни на бораните, съдържащи тройна B≡B връзка.
Хетероборани[редактиране | редактиране на кода]
Хетеробораните са борани, в молекулата на които има един или повече атоми, различни от B и H. Получаването на хетероборани често налага добавяне на хетероатоми към нидо-борани в т. нар. „раекции с разширяване на скелета“ (cage expansion reactions).[4] Два от най-използваните борани за този синтез са нидо-B5H9 и нидо-B10H14.
При взаимодействие на бораните с някои органични производни се получават молекули, съдържащи борни и въглеродни атоми. Тези съединения се наричат карборани (карбоборани). Те са по-стабилни от бораните и силни редуктори. Аналогично на въглеводородите, при тях са възможни много производни.
Металакарбобораните са съединения, които съдържат клъстерни полиедри, изградени от въглерод, бор и метални атоми в различни комбинации. Първите клъстери от металакарбоборани са синтезирани от Хоторн (Hawthorne) през 1965 г. и са получени от икосаедричния клозокарбаборан 1,2-C2B10H12 чрез заместване на един BH връх с метален център.[4]
Органобораните са органични съединения, съдържащи връзката C–B.[4]
Номенклатура[редактиране | редактиране на кода]
Неутралните полиборни хидриди се наричат борани, а най-простата възможна базова структура, BH3, се нарича „боран“.[3] Броят на борните атоми в молекулата на борен хидрид се дава с мултиплицираща представка. Броят на водородните атоми се представя с арабска цифра в кръгли скоби веднага след името. Такива наименования носят композиционна информация (B20H16 – ейкозаборан(16)).
Систематично номериране на полиядрени клъстери[редактиране | редактиране на кода]
Борният скелет на всеки клъстер трябва да се номерира систематично, така ме да позволи недвусмислено номериране на заместени производни. За целта се приема, че борните атоми от клозо структури заемат равнини, разположени перпендикулярно спрямо оста с най-голяма симетрия. Ако има няколко такива оси, се избира пресичащата се от най-голям брой перпендикулярни равнини.
Номерирането започва от най-близкия борен атом, когато клъстерът се наблюдавано направление на тази ос и продължава обратно на часовниковата стрелка или по посока, обратна на часовниковата стелка за борните атоми от първата равнина. Номерирането продължава по същия начин в следващата равнина, започвайки от борния атом, разположен най-близо до борния атом с най-малък атом от предишната равнина, и се следва посоката на номериране.[3]
Скелетно заместване[редактиране | редактиране на кода]
Възможно е скелетната структура на борани да бъде запазена в техни производни, в които един или повече борни атоми са заместени с други атоми. Наименованията на тези съединения се образуват чрез адаптиране на заместителната номенклатура, което води до имена като карбаборани, фосфаборани, тиаборани и т.н.
В хетеробораните, броят на най-близките съседи на хетероатома е различен. Адаптират се на заместителните наименования към полиборни съединения.
Заместването на борен атом с друг атом се посочва в наименованиетозаедно с броя на водородните атоми в резултатната полиедрена структура. Представките клозо, нидо, арахно и т.н. се запазват за описание на борни хидриди. Позициите на заместващите хетероатоми в полиедрената рамка се посочват с локанти, които като група са възможните най-малки числа, съответсващи на номерирането в базовия полиборан.[3]
Получаване[редактиране | редактиране на кода]
Бораните са термодинамично нестабилни съединения. Те не могат да се получат чрез пряка синтеза поради много голямата енергия на връзката в молекулата на водорода (436 kJ/mol) и голямата енергия на атомизация на бора (565 kJ/mol).
Диборанът се получава лабораторно при взаимодействие на борен халогенид с LiAlH4 или LiBH4 в етерен разтвор:[2]
.
Синтезата се извършва във вакум, защото B2H6 се самозапалва на въздух.
Разработени са няколко промишлени метода за получаването на борани.
- Редукция на BF3 с натриев хидрид:
.
- Взаимодействие на алкални тетрахирогенборати с фосфорна киселина:
От диборана се получават всички останали борани, като се регулира налягането, температурата и скоростта на процеса. Например B4H10 се получава като диборан се държи 10 дни под налягане под 25 °C:
.
Източници[редактиране | редактиране на кода]
- ↑ а б в г Лефтеров, Димитър. Химичните елементи и техните изотопи. София, Издателство на БАН „Проф. Марин Дринов“, 2015. ISBN 978-954-322-831-7. с. 251 – 252.
- ↑ а б в г д е ж з и к л м н Киркова, Елена. Химия на елементите и техните съединения. София, Университетско издателство „Св. Климент Охридкси“, 2013. ISBN 978-954-07-3504-7. с. 134 – 144.
- ↑ а б в г д G. Connely, Neil, M. Hartshorn, Richard, Damhus, Ture. Номенклатра по неорганична химия. Препоръки на IUPAC 2005. София, Академично издателство „Проф. Марин Дринов“, 2013. ISBN 978-945-322-330-5. с. 79 – 82, 86-87.
- ↑ а б в г д е ж King, R. Encyclopedia of Inorganic Chemistry [10 Volumes]. с. 412-522.
|



![{\displaystyle {\ce {B2H6 + HCl ->[{↓t}] 2BCl3 + 6 HCl}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f9f1ac2ecc6d89ee0d047e64f0769eb9555263c6)



![{\displaystyle {\ce {H2B=H2BH2 + 2NH3 -> [H2B(NH3)2]^+ + [BH4]^-}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/0578e6e9a62b73bc9d2bad3c73ddb25af39b7e27)
![{\displaystyle {\ce {B4H10 + N(CH3)3 -> [HN(CH3)3]^+ [B10H13]^-}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1302cf95238b8a960345ef2bad11c5abca95b9d6)
![{\displaystyle {\ce {B-H-B -> [B-B]^- + H^+}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/eca0db74fc1bdd7741ee207a804aa797357f4287)
![{\displaystyle {\ce {2LiH + B2H6 ->[{Et₂O}] 2Li[BH4]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ff5a941f67ddca31a8e0eff93c60e424caae29da)
![{\displaystyle {\ce {4NaH + BCl3 -> Na[BH4] + 3NaCl}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/776b08ae59a5ddc0b40f8d10342cc803acb9af11)
![{\displaystyle {\ce {Na2B4O7 + 7SiO2 +16Na +8H2 ->[{t°=450-500°C}] 4Na[BH4] + 7Na2SiO3}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/39f5582b0863073832301cd1355443d679eeebf7)
![{\displaystyle {\ce {3NaBH4 + AlCl3 ->[{H₂O}] Al[BH4]3 + 3NaCl}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c4d35435069a80a81243f8eccbb62d5591c3f354)

![{\displaystyle {\ce {2BF3 + 6NaH ->[{180°C}] B2H6 + 6NaF}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/0fde42edffc895bfd94dae57ba7a2173e0c01fa8)

