Биохимия: Разлика между версии
{{lang-la}} => {{lang|la}} |
м форматиране: 4x нов ред (ползвайки Advisor) |
||
| Ред 46: | Ред 46: | ||
{{основна|Въглехидрат|Монозахарид|Дизахарид|Полизахарид}} |
{{основна|Въглехидрат|Монозахарид|Дизахарид|Полизахарид}} |
||
[[Файл:Sucrose-inkscape.svg|мини |
[[Файл:Sucrose-inkscape.svg|мини|Структура на [[захароза]], дизахарид изграден от (глюкоза и фруктоза).]] |
||
Въглехидратите са изградени от мономери наречени ''[[монозахарид]]и''. Представители на монозахаридите са [[глюкоза]] (C<sub>6</sub>H<sub>12</sub>O<sub>6</sub>), [[фруктоза]] (C<sub>6</sub>H<sub>12</sub>O<sub>6</sub>) и [[дезоксирибоза]] (C<sub>5</sub>H<sub>10</sub>O<sub>4</sub>). При [[кондензация]]та на два монозахарида се образува молекула вода от [[Хидроксилна група|хидроксилната група]] на единия и [[водороден атом]] от другия монозахарид. |
Въглехидратите са изградени от мономери наречени ''[[монозахарид]]и''. Представители на монозахаридите са [[глюкоза]] (C<sub>6</sub>H<sub>12</sub>O<sub>6</sub>), [[фруктоза]] (C<sub>6</sub>H<sub>12</sub>O<sub>6</sub>) и [[дезоксирибоза]] (C<sub>5</sub>H<sub>10</sub>O<sub>4</sub>). При [[кондензация]]та на два монозахарида се образува молекула вода от [[Хидроксилна група|хидроксилната група]] на единия и [[водороден атом]] от другия монозахарид. |
||
| ⚫ | |||
=== Липиди === |
=== Липиди === |
||
| ⚫ | |||
{{основна|Липид|Глицерол|Мастна киселина}} |
{{основна|Липид|Глицерол|Мастна киселина}} |
||
| Ред 56: | Ред 56: | ||
=== Протеини === |
=== Протеини === |
||
| ⚫ | |||
{{основна|Протеин|Аминокиселина}} |
{{основна|Протеин|Аминокиселина}} |
||
| ⚫ | |||
Протеините са огромни биополимери изградени от мономери наречени ''аминокиселини''. Има 20 канонични аминокиселини, като всяка има [[карбонилна група]], [[аминогрупа]] и страничен [[Радикал (химия)|радикал]], който се бележи с „R“. Страничният радикал е този, който отличава аминокиселините една от друга и им придава специфична роля при изграждането на [[Полипептидна верига|полипептидната верига]] и триизмерната структура на протеина. Аминокиселините се свързват при кондензация формирайки [[пептидна връзка]], като по този начин се синтезират дългите вериги на белтъците. Процесът е известен като [[Транскрипция (биология)|транскрипция]]. |
Протеините са огромни биополимери изградени от мономери наречени ''аминокиселини''. Има 20 канонични аминокиселини, като всяка има [[карбонилна група]], [[аминогрупа]] и страничен [[Радикал (химия)|радикал]], който се бележи с „R“. Страничният радикал е този, който отличава аминокиселините една от друга и им придава специфична роля при изграждането на [[Полипептидна верига|полипептидната верига]] и триизмерната структура на протеина. Аминокиселините се свързват при кондензация формирайки [[пептидна връзка]], като по този начин се синтезират дългите вериги на белтъците. Процесът е известен като [[Транскрипция (биология)|транскрипция]]. |
||
| ⚫ | |||
=== Нуклеинови киселини === |
=== Нуклеинови киселини === |
||
| ⚫ | |||
{{основна|Нуклеинова киселина|ДНК|РНК|Нуклеотид}} |
{{основна|Нуклеинова киселина|ДНК|РНК|Нуклеотид}} |
||
Нуклеиновите киселини играят ключова роля в съхраняването на наследствената информация ([[ДНК]], при някои [[вируси]] [[РНК]]), както и в процесите на нейната реализация (РНК) до функционално активен протеин. Мономерите на нуклеиновите киселини се наричат [[нуклеотид]]и. В състава на ДНК участват предимно четирите нуклеотида – [[аденин]], [[цитозин]], [[гуанин]] и [[тимин]], при РНК вместо тимин се среща [[урацил]]. |
Нуклеиновите киселини играят ключова роля в съхраняването на наследствената информация ([[ДНК]], при някои [[вируси]] [[РНК]]), както и в процесите на нейната реализация (РНК) до функционално активен протеин. Мономерите на нуклеиновите киселини се наричат [[нуклеотид]]и. В състава на ДНК участват предимно четирите нуклеотида – [[аденин]], [[цитозин]], [[гуанин]] и [[тимин]], при РНК вместо тимин се среща [[урацил]]. |
||
{{Br}} |
|||
=== Нискомолекулни съединения === |
=== Нискомолекулни съединения === |
||
Версия от 11:53, 22 март 2019

Биохимията е наука за химичния състав на организмите, химичните процеси в тях и връзката на тези процеси с проявите на жизнена дейност. Занимава се със структурата и функцията на клетъчните компоненти като протеини, липиди, въглехидрати, нуклеинова киселина и други биомолекули.
Въпреки че има голям брой различни биомолекули, много от тях са комплексни съединения (наричани полимери), които са съставени от голям брой повтарящи се градивни частици (наречени мономери). Различните класове полимери имат различни градивни мономери. Например протеините са изградени от 20 мономера наречени аминокиселини. Биохимията изучава свойствата на важни биомолекули като протеините и в частност ензимно-каталитичните реакции.
Биохимията на клетъчния метаболизъм и ендокринната система е добре описана. Други области, в които биохимията има напредък са генетичния код (ДНК и РНК), синтеза на белтъци, транспорта през клетъчната мембрана и др.
Биохимията бива:
- биохимия на растенията, с широко застъпен дял за микроорганизмите;
- биохимия на животните;
- биохимия на човека, с практически важен за медицината дял патологична биохимия (клинична).
Биохимията има приложение във всички биологични и медицински дисциплини, в технологията на ферментационните процеси и други.
Връзка на биохимията с другите субклетъчно-ориентирани биологични науки

В биохимията се използват техники и методи присъщи единствени за нея, но също и идеи, техники и методи специфични за други области на познанието като генетика, молекулярна биология и биофизика. Трудно може да се постави разделителна линия между тези науки, особено в контекста на използваните техники и способи. В днешно време термините молекулярна биология и биохимия са до голяма степен взаимозаменяеми. Схемата в дясно дава едно интерпретиране на отношенията на частните биологични науки, изучаващи живота на субклетъчно равнище.
- Биохимията е наука, изучаваща химичните компоненти участващи в жизнените процеси на живите организми. Биохимията е основно фокусирана върху ролята, функцията и структурата на биомолекулите.
- Генетиката изучава свойствата наследственост и изменчивост на организмите, като акцентира върху физическите носители на тези свойства – тяхната структура, функции и процесите, в които участват.
- Молекулярната биология изучава реализацията на генетичната информация, посредством преноса на данни при процесите репликация, транскрипция и транслация (Централна догма на молекулярната биология), като се фокусира не само върху механизма и ролята на отделните компоненти в него, но и начините за регулация в това число и с терапевтична цел.
Методи в биохимията
В биохимията се прилагат множество разнообразни методи от различни области. В класическата биохимия се използват методиките от аналитична химия, органична химия, физикохимия и физика. Важни техники са центрофугиране, хроматография, електрофореза, спектроскопия, изотопни техники, кристализация, потенциометрични, електрохимични, поларографски и манометрични техники. През последните десетилетия се използват молекулярно-биологични техники, методи от компютърните науки, микробиология и други науки. Освен това в съвременната биохимия винаги се прави и количествена оценка на резултатите с математически методи и създаването на формални теории, с помощта на математиката.
История на биохимията
Историята на биохимията започва преди около 400 години. Въпреки че терминът „биохимия“ вероятно е използван за пръв път през 1882 г., е прието, че думата „биохимия“ е въведена от немският учен Карл Нойберг през 1903 г. Първоначално се е вярвало, че живото не е предмет на законите на науката по начина, по който неживото е. Вярвало се е, че само живите организми притежават жизнена сила (на латински: Vis Vita) и само те могат да произвеждат молекулите на живота. През 1828 г. Фридрих Вьолер публикува статия относно синтезата на уреята, с което доказва че органични компоненти могат да бъдат създавани изкуствено, като развенчава тази идея.[1][2]
Важни за биохимията събития
- 1828 – Синтезът на органичен карбамид от неорганичния амониев цианат от Фридрих Вьолер
- 1833 – Откриването на първия ензим (Диастаза, Амилаза) от Анжел Пайен
- 1869 – Откриването на нуклеиновите киселини от Фридрих Мишер
- 1896 – Откриването на безклетъчна ферментация от Едуард Бухнер
- 1926 – Откриването на дихателния ензим цитохром оксидаза от Ото Варбург
- 1929 – Установяването на механизма на гликолизата от Густав Ембден, Ото Майерхоф и Якоб Парнас
- 1932 – Откриване на цикъла на лимонената киселина от Ханс Адолф Кребс (в негова чест „цикъл на Кребс“)
- 1953 – Установяването на структурата на дезоксирибонуклеиновата киселина от Джеймс Уотсън и Франсис Крик
Биомолекули
Четирите основни класа биомолекули в биохимията са: въглехидрати, липиди, протеини и нуклеинови киселини. Повечето биомолекули са полимери – изградени от мономери, които са относително нискомолекулни съединения свързани помежду си в полимери, чрез процес наречен поликондензация (често се използва неправилното полимеризация).
Въглехидрати

Въглехидратите са изградени от мономери наречени монозахариди. Представители на монозахаридите са глюкоза (C6H12O6), фруктоза (C6H12O6) и дезоксирибоза (C5H10O4). При кондензацията на два монозахарида се образува молекула вода от хидроксилната група на единия и водороден атом от другия монозахарид.
Липиди
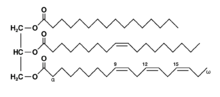
Липидите често, но не задължително, са изградени от глицерол и свързани към него други молекули. При триглицеридите, главната група липиди, глицеролът е естерифициран (свързан) с три мастни киселини. Другият главен клас липиди, стероидите, са производни на холестерола, получени чрез добавяне или заместване на функционални групи.
Протеини
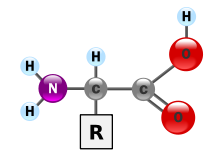
Протеините са огромни биополимери изградени от мономери наречени аминокиселини. Има 20 канонични аминокиселини, като всяка има карбонилна група, аминогрупа и страничен радикал, който се бележи с „R“. Страничният радикал е този, който отличава аминокиселините една от друга и им придава специфична роля при изграждането на полипептидната верига и триизмерната структура на протеина. Аминокиселините се свързват при кондензация формирайки пептидна връзка, като по този начин се синтезират дългите вериги на белтъците. Процесът е известен като транскрипция.
Нуклеинови киселини

Нуклеиновите киселини играят ключова роля в съхраняването на наследствената информация (ДНК, при някои вируси РНК), както и в процесите на нейната реализация (РНК) до функционално активен протеин. Мономерите на нуклеиновите киселини се наричат нуклеотиди. В състава на ДНК участват предимно четирите нуклеотида – аденин, цитозин, гуанин и тимин, при РНК вместо тимин се среща урацил.
Нискомолекулни съединения
Някои нискомолекулни съединения, които не участват в изграждането на биополимерите, също са предмет на биохимията, поради голямата им значимост в регулацията и осъществяването на цялостния метаболизъм. Повечето са кофактори в ензимно-катализираните реакции (напр. НАД, ФАД, НАДФ, АМФ, коензим А и много други); други са сигнални молекули, участващи в междуклетъчната сигнализация, както и вторични посредници (second messenger) при осъществяването на сигналната трансдукция (фосфатидилинозитол-3,4-бифосфат, ГТФ, цАМФ, NO).
Източници
- ↑ Wöhler, F. Ueber künstliche Bildung des Harnstoffs // Ann. Phys. Chem. 12. 1828. с. 253 – 256.
- ↑ Kauffman, G. B. and Chooljian, S.H. Friedrich Wöhler (1800 – 1882), on the Bicentennial of His Birth // The Chemical Educator 6 (2). 2001. DOI:10.1007/s00897010444a. с. 121 – 133.
| ||||||||||||||
| ||||||||||||||
