Невроонкология
Тази статия съдържа списък с ползвана литература, препоръчана литература или външни препратки, но източниците ѝ остават неясни, защото липсва конкретно посочване на източници за отделните твърдения. (7 май 2023) |

Невроонкологията е специалност в медицината, която съчетава неврологията и онкологията.
Невроонкологията се занимава основно с диагностика, терапия и изследване на туморни заболявания на нервната система, което включва следните видове тумори:
- първични тумори на централната нервна система (мозъчни тумори и тумори на гръбначния мозък)
- вторични тумори на централната нервна система (мозъчни метастази и метастази в гръбначния мозък)
- злокачествени лимфоми на централната нервна система
- Тумори на периферната нервна система
Този списък вече показва, че това е широка област, която е трудна за дефиниране. Докато лечението на централните нервни лимфоми също следва указанията за хематологично лечение и мозъчните метастази не се лекуват отделно от основната терапия на първичния тумор, туморите на периферните нерви са доброкачествени, като невриномите, и подобно на други тумори на меките тъкани често се локализират в ортопедични площ.
Основна информация[редактиране | редактиране на кода]
Първични тумори на централната нервна система[редактиране | редактиране на кода]
Първичните мозъчни тумори могат да възникнат във всяка възраст, от ранна детска възраст до късна възраст. Фактори като възраст, местоположение на тумора и клинична картина са полезни при диференциалната диагноза. Повечето видове първични мозъчни тумори са по-чести при мъжете, с изключение на менингиомите, които са по-чести при жените.
Метастатични тумори на централната нервна система[редактиране | редактиране на кода]
Директната инвазия или компресия на непрекъснати тъкани е свързана с близостта на нервната система до други структури.
Интракраниални метастази[редактиране | редактиране на кода]
Има три вида вътречерепни метастази: мозъчни метастази, дурални метастази и менингеално-лептоменингеални метастази. Мозъчните метастази могат да бъдат единични или множествени и да засегнат всяка част на мозъка. Метастазите в дурални структури обикновено възникват чрез хематогенно разпространение или директна инвазия от съседна кост. Дуралните метастази могат да нахлуят в подлежащия мозък и да причинят фокален оток и свързани неврологични симптоми. Поради тяхното кортикално местоположение, тези процеси са склонни да причиняват гърчове в началото на курса. Лептоменингеалните метастази са рядък, но добре познат клиничен феномен при пациенти с рак. Лептоменингеалните метастази най-често се дължат на първични тумори на гърдата, белите дробове или меланома.
Черепни метастази[редактиране | редактиране на кода]
Метастазите в черепа се разделят на две категории: калвариум и основа на черепа.
Първични тумори на централната нервна система[редактиране | редактиране на кода]
Първото подразделение на туморите на централната нервна система (ЦНС) възниква между първични (произхождащи директно от ЦНС) и метастатични (произхождащи от друг орган) тумори. Последните имат честота приблизително десет пъти по-голяма от първата. Мозъчните тумори са неоплазми, които се развиват в мозъка. Тумори като менингиом, който поради своята маса компресира, но не прониква в мозъка, и тумори на хипофизата и епифизата, които се намират в мозъчния ствол, често се наричат неправилно мозъчни тумори. Терминът интракраниални тумори ги обобщава по-точно.
Първичните тумори на ЦНС включват различни патологични единици, всяка със собствена естествена история. Поради факта, че само глиалните тумори са почти 40 % от тези тумори, първо може да се направи разграничение между глиални тумори (глиоми) и неглиални тумори. Най-често срещаните глиоми са астроцитоми (произхождащи от глиални астроцитни клетки), олигодендроглиоми (произхождащи от олигодендроглиални клетки) и епендимоми (произхождащи от епендимни клетки).
Епидемиология[редактиране | редактиране на кода]
Злокачествените първични тумори на централната нервна система са относително редки и представляват около 2 процента от всички злокачествени новообразувания. Туморните заболявания на централната нервна система са разпределени в 95 бр процента върху мозъка и до 5 Процент върху менингите, черепните нерви и гръбначния мозък. Те могат да се появят във всяка възраст, като рискът от развитие на заболяването нараства с възрастта. При възрастни глиоми могат да бъдат открити хистологично, произхождащи от поддържащата тъкан на нервните клетки, от които около 75 процент глиобластоми Астроцитоми IV. степени с неблагоприятна прогноза. Ембрионалните тумори преобладават при кърмачета и малки деца. Средно процентът на преживяемост е 21 процента за мъжете и 24 процента за жените. Статистиката също рядко включва хистологично доброкачествени тумори на ЦНС, които се срещат при около 6000 нови случаи per годишна лъжа. Около 65 Процент от него идва от менингите. Жените са засегнати много по-често. Ако не се лекуват с операция или лъчева терапия, дори доброкачествените тумори могат да бъдат фатални поради прогресивния растеж в затвореното черепно пространство. Най-честият злокачествен вътречерепен тумор на ЦНС е глиобластомът, най-честият доброкачествен е менингиомът.
Етиология[редактиране | редактиране на кода]
Генетичното предразположение към неоплазми на централната нервна система е сравнително рядко, въпреки че някои глиоми могат да възникнат като усложнения на множество фамилни заболявания.
Мутацията на някои туморни супресорни гени характеризира няколко наследствени синдрома, които показват повишена чувствителност към развитието на мозъчни тумори. Следните мутации и техните синдроми са свързани с по-висок риск от развитие на мозъчни тумори: NF1 генна мутация с неврофиброматоза тип 1, APC мутация със синдром на Turcot, PTCH мутация със синдром на Gorlin и TP53 или CHEK2-мутация със синдром на Li-Fraumeni.
Факторите на околната среда, свързани с първичните мозъчни тумори, са трудни за идентифициране. В някои проучвания излагането на винилхлорид е свързано с повишена честота на глиома с висока степен. Единствената рядка, но добре идентифицирана причина за първичен мозъчен тумор е йонизиращото лъчение. По-специално, лъчетерапията на деца с tinea capitis и на пациенти с остра лимфна левкемия, краниофарингиома или неходжкинов лимфом е свързана с повишен риск от глиома. Съществува повишен риск от първичен церебрален лимфом при пациенти със СПИН.
Клиника[редактиране | редактиране на кода]
Признаци и симптоми[редактиране | редактиране на кода]
Симптомите на церебралната неоплазия се характеризират с изместване или Разрушаване на околната тъкан и инфилтрация на същите причини.
Най-честият симптом, докладван от 35 процента от пациентите, е главоболието. Появата на тежки главоболия при пациенти, които иначе рядко страдат от тях, често е характерна, особено ако пристъпите на главоболие или мигрена са по-тежки сутрин и са придружени от гадене, повръщане и неврологични дефицити. При пациенти, които по-често страдат от главоболие, промяната във формата, увеличаването на честотата или интензивността на атаките може да бъде симптом на развитието на мозъчен тумор. Припадъци се появяват при около една трета от пациентите с глиома, особено при тумори с ниска степен или ЦНС. Фокалните неврологични дефицити са свързани с местоположението на тумора. Промени в психичното състояние се наблюдават и при 15 до 20 процента от пациентите с глиома.
Образна диагностика[редактиране | редактиране на кода]

Компютърната томография (CT) и ядрено-магнитен резонанс (MRI) могат ефективно да открият неоплазия в мозъка. MRI е по-чувствителен от CT за идентифициране на лезии, но има противопоказания за пациенти със сърдечни пейсмейкъри, несъвместими протези, метални скоби и други. КТ остава методът на избор за откриване на калцификации в рамките на лезии или костни ерозии на черепната шапка или основата. Използването на контрастни вещества, които са йодирани в случай на CT и парамагнитни (гадолиний) в случай на MRI, позволява получаването на информация за васкуларизацията и целостта на кръвно-мозъчната бариера, по-добра дефиниция на туморния тумор в сравнение с към околния оток и генериране на хипотези за степента на злокачественост. Рентгенологичното изследване също така позволява оценка на механичните ефекти и последващите промени в мозъчните структури, произтичащи от тумора, като хидроцефалия и херния, последиците от които могат да бъдат фатални. И накрая, при подготовката за операция, тази диагностика може да се използва за определяне на местоположението на лезията или инфилтрацията на тумора в жизненоважни области на мозъка. За тази цел MRI е по-ефективен от CT, тъй като може да осигури триизмерни изображения.
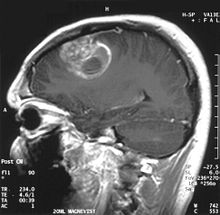
Диагностичните радиологични образни инструменти подчертават промяната в неопластичната тъкан в сравнение с нормалния мозъчен паренхим (чрез промени в електронно изобразената тъканна плътност при CT и интензитета на сигнала при MRI). Както повечето патологични тъкани, туморите също се разпознават чрез повишено натрупване на вътреклетъчна вода. В компютърната томограма те изглеждат хиподенсни, т.е. с по-малка плътност от мозъчния паренхим, в магнитно-резонансната томограма със спин-решеткова релаксация хипоинтензивен и в спин-спин релаксация както и хиперинтензивно протонно претегляне (PD).
Здравата област на мозъка не трябва да показва никаква конкретна луминесценция на радиологично изображение. Следователно, разбира се, вниманието се обръща на по-големите диапазони на контрастния сигнал.
В туморната тъкан, като цяло, по-голямата част от усилването на контраста се дължи на специфичната кръвно-туморна бариера, която позволява преминаването на йод (CT) и гадолиний (MRI) в интратуморното екстраваскуларно интерстициално пространство. Това увеличава сигнала (плътност или интензитет) на тумора. Все пак трябва да се внимава, за да се гарантира, че усилването на контраста не разграничава окончателно неоплазията от околорановия оток. Всъщност анатомично-патологичната находка в туморна тъкан на злокачествен инфилтриращ глиом, като например при глиобластом и анапластичен астроцитом, също показва отвъд вазогенния оток, причинен от разрушаването на кръвно-мозъчната бариера от тумора. Последното клинично състояние е слабо откриваемо чрез образна диагностика.
Компютърната томография на мозъка обикновено показва тъканна маса, която може да бъде увеличена от двата контраста. При компютърна томография нискостепенните глиоми обикновено изглеждат изоденсни към нормалния паренхим и следователно може да не показват усилване на контраста. По същия начин лезиите в задната черепна ямка са трудни за идентифициране при КТ. Следователно резултатите само от такава томография не винаги са достатъчни за диагностични цели. В съмнителни случаи е необходимо използването на по-чувствителен ядрено-магнитен резонанс.
На – ЯМР показва вътречерепен тумор като масивна лезия, която може да стане по-луминисцентна след използване на контрастното средство. Винаги обаче има сигнална аномалия – Ядрено-магнитен резонанс, който показва наличието на неоплазия или вазогенен оток. Обикновено повишената луминесценция (усилване на контраста) е показателна за тумор с по-висока степен на злокачествено заболяване. Контрастният пръстен е характерен за глиобластома, като луминесцентната част съответства на жизнената част на злокачествения тумор, а по-тъмната – hypointense зона, съответстваща на тъканна некроза.
Постановка[редактиране | редактиране на кода]
Повечето първични интракраниални тумори остават локализирани в черепа, така че не са необходими системни процедури за стадиране.
Обратно, първичните невроектодермални тумори, медулобластоми, тумори на зародишни клетки на ЦНС и първични лимфоми на ЦНС често се разпространяват през субарахноидалното пространство до лептоменингите. Следователно за всички пациенти с такива диагнози е необходим и спинален магнитен резонанс или лумбална пункция.
Видове тумори[редактиране | редактиране на кода]
Глиоми[редактиране | редактиране на кода]
Първичните тумори на централната нервна система (ЦНС) включват различни патологични тъкани, всяка със собствена естествена история. Поради факта, че само глиомите представляват почти 40 процента от всички тумори на ЦНС, в литературата е обичайно да се прави разлика между глиални и неглиални тумори.
Астроцитоми[редактиране | редактиране на кода]
С течение на времето в литературата са предложени различни категорийни системи за класифициране на злокачествеността на астроцитомите. От 1993 г. четиристепенната рейтингова система, предложена от Световната здравна организация (СЗО), е най-широко използваната и прилагана. Базира се на четири хистологични характеристики: повишена клетъчна плътност, митоза, ендотелна пролиферация и некроза. След това астроцитомите от степен I, като пилоцитните астроцитоми, обикновено са с доброкачествена хистология. Астроцитоми II. Степените (дифузни) показват повишена клетъчна плътност като единствена хистологична характеристика и са неоплазми с по-ниска степен на инфилтрация. Астроцитомите III показват значителна митоза. степен (анапластичен). Ендотелна пролиферация или некроза се наблюдават при астроцитоми IV. градуса, така наречените глиобластоми.
Нискокачествени астроцитоми[редактиране | редактиране на кода]

Пилоцитни астроцитоми (включително пиломиксоиден аастроцитом ), субепендимални гигантски клетъчни астроцитоми и плеоморфни ксантастроцитоми са сред ограничените тумори. Това са малко по-редки неоплазми с доброкачествена хистология, които често могат да бъдат излекувани само чрез операция. Ако изрязването е непълно, останалата туморна тъкан може да бъде успешно лекувана с лъчева терапия. В редки случаи, когато локалното лечение не работи, системната химиотерапия може да бъде успешна, която трябва да бъде индивидуално коригирана. Децата реагират на комбинация от карбоплатин и винкристин.


При компютърна томография се появяват дифузни астроцитоми II. Степени от по-малко интензивни лезии. При предпочитаното ядрено-магнитен резонанс контрастните вещества може да не са в състояние да подчертаят тези неоплазми, тяхната луминесценция може да е по-тънка и по-слаба. По-интензивен може да показва тъкани с повишена анаплазия. Когато е възможно, се препоръчва биопсия за получаване на проби от анапластичната част на тумора.
В повечето случаи пациентите с дифузни астроцитоми са на възраст от 20 до 40 години. Характерна за тях е появата на епилептични припадъци. Условия за благоприятна прогноза са млада възраст, размер на тумора под 50 милиметра и възможно най-обширна хирургична резекция на тумора. Късните рецидиви са сравнително чести, поради което пациентите трябва да бъдат проследявани в продължение на 15 години след отстраняване на тумора.
Въпреки сравнително бавния си ход, повечето астроцитоми прогресират до лезии, характеризиращи се с обширна анаплазия, които обикновено са рефрактерни на операция и лъчева терапия. Въпреки това, терапията за пациенти с дифузни нискостепенни астроцитоми не показва единодушен консенсус в литературата. Ролята на пълната резекция се обсъжда в професионален контекст. Резултатите от някои изследвания показват, че максималното отстраняване на тумора дава най-добри резултати. Всъщност малките и едностранни тумори могат да бъдат напълно отстранени, ако не са засегнати критични структури на мозъка. Прагматичен подход, който като цяло е приемлив за общите случаи, е да се отстрани неоплазията, доколкото е възможно, за да се избегнат значителни неврологични дефицити.
Проучванията показват, че лъчетерапията, приложена веднага след диагностицирането, е удължила времето, през което пациентът е свободен от заболяване преди рецидив на тумора, в сравнение със ситуацията, при която курсът на лъчетерапията се забавя до момента на прогресия. Понастоящем обаче няма консенсус, че лъчетерапията малко след поставяне на диагнозата подобрява „общата преживяемост“ на пациента.
При пациенти с по-леки или никакви симптоми, или с гърчове, които могат да бъдат контролирани с лекарства против гърчове, е възможно да се отложи лъчетерапията, докато туморният растеж достигне критична фаза. Често има желание да се намали рискът от неврологични увреждания, причинени от самата лъчетерапия.
Две проспективни рандомизирани клинични проучвания не показват по-голяма полза от лъчетерапията с високи дози, отколкото от лъчетерапията с ниски дози. Обикновено общата доза е между 45 и 54 Грея с фракциониране от 1,8 до 2 Грея.
Ефектът от адювантната химиотерапия при пациенти с нискостепенни астроцитоми все още се изследва. Предварителните резултати от клинично изпитване, сравняващо само лъчетерапия с лъчетерапия, последвана от химиотерапия, съдържаща прокарбазин, ломустин и винкристин (PCV), показват по-дълъг период на „оцеляване без заболяване“ с комбинацията, но не и удължена „обща преживяемост“. Поради токсичността, свързана с PCV протокола, употребата на temozolomide се препоръчва както като начална терапия, така и след възстановяване.
Анапластични астроцитоми[редактиране | редактиране на кода]

Анапластичният астроцитом е злокачествен мозъчен тумор, характеризиращ се с дифузен растеж, повишена клетъчна плътност и фигури на ядрено делене. Той възниква от специфична клетъчна популация на централната нервна система, астроцитите. Според класификацията на СЗО за тумори на централната нервна система, туморът отговаря на III степен тумор.
Обикновено пациентите с анапластичен астроцитом се проявяват с епилептични припадъци, фокални неврологични дефицити, главоболие и промени в личността. Средната възраст на пациента е 45 години. Магнитно-резонансното изображение обикновено показва масивна лезия с повишен контрастен сигнал, който може да бъде и по-слаб. Диагнозата се поставя чрез хистологично изследване на лезията чрез биопсия или хирургична резекция.
По-лошата прогноза може да бъде свързана с напреднала възраст, лошо физическо състояние и значително неврологично увреждане. Като цяло, терапевтичният резултат е по-добър при пълна хирургична резекция (стандартно лечение) без увеличаване на неврологичния дефицит. Лъчевата терапия е стандартна, тъй като е доказано, че увеличава времето за оцеляване. Ролята на химиотерапията е спорна.
Глиобластом[редактиране | редактиране на кода]

Най-честите и злокачествени глиални тумори са глиобластомите. Те се състоят от хетерогенна маса от слабо диференцирани астроцитомни клетки главно при възрастни. Те обикновено се появяват в мозъчните полукълба, по-рядко в мозъчния ствол или гръбначния мозък. Освен в много редки случаи, като всички мозъчни тумори, те не се простират извън структурите на централната нервна система.
Глиобластомът може да възникне от дифузен (II. степен) или анапластичен астроцитом (III. степен) развивам. В последния случай се нарича вторичен. Въпреки това, когато се появи без предшественици или доказателства за предишно злокачествено заболяване, то се нарича първично. Глиобластомите се лекуват с операция, радиация и химиотерапия. Те са трудни за лечение и има малко случаи, оцелели след три години.
Олигодендроглиоми[редактиране | редактиране на кода]
Олигодендроглиомът е необичаен глиален мозъчен тумор, който възниква от олигодендроцити. Среща се главно при възрастни между 40 и 45 години, предимно в мозъчната кора и бялото вещество на мозъчните полукълба.
Олигодендроглиомите са относително необичайни, представляващи по-малко от около 5 процента от всички първични мозъчни тумори и не повече от около 10 до 15 процента от всички глиоми. Тези тумори се разделят на нискостепенни и анапластични лезии. Анапластичният олигодендроглиом се характеризира с повишена клетъчна плътност, митоза, ендотелна пролиферация и ядрен полиморфизъм и некроза.
Нискокачествени олигодендроглиоми и олигоастроцитоми[редактиране | редактиране на кода]
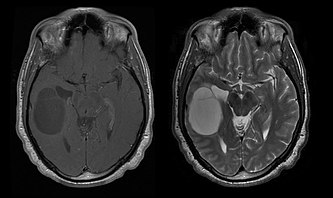
Средната преживяемост при пациенти с чист олигодендроглиом е около 10 години, с олигоастроцитом около 8 години. Удължаването в сравнение с чистите астроцитоми се дължи на делеция или транслокация на двойката 1p/19q в тумора.
Средната възраст на пациентите при поставяне на диагнозата е 35 години. Типичните симптоми са епилептични припадъци, но могат да бъдат докладвани и фокални неврологични дефицити, промени в личността или други симптоми на вътречерепно налягане, като главоболие и повръщане. Тези тумори обикновено не се виждат при компютърна томография, така че ЯМР е метод на избор за образна диагностика. На ЯМР те се разпознават като повишен интензитет на сигнала. На – изображения, от друга страна, сигналът може да бъде заглушен и подобрението на контраста може да бъде открито само от време на време. Може да липсва сигнал за калцификация.
Тези тумори прогресират по-бавно от нискостепенните астроцитоми и в литературата няма консенсус относно оптималното лечение. Първоначалното лечение включва контролиране на симптомите с антигърчови лекарства, радиация, химиотерапия или комбинация от последните две. Хирургията, лъчетерапията и химиотерапията играят важна роля при рецидивите. Резекциите могат да облекчат симптомите. На темозоломид показа 50 Процентът на пациентите, които имат рецидив след лъчетерапия, имат положителна реакция.
Анапластични олигодендроглиоми и олигоастроцитоми[редактиране | редактиране на кода]
Анапластичните олигодендроглиоми показват типични симптоми в резултат на масовия ефект и епилептичните припадъци. Въпреки тяхната химиочувствителност, средната преживяемост е само 3 до 5 години. Лечението включва максимално изрязване, последвано от лъчева терапия. По отношение на химиотерапията трябва да се отбележи, че две скорошни клинични изпитвания фаза III сравняват резултатите от лъчетерапията с тези от комбинираната лъчетерапия и химиотерапия с прокарбазин, ломустин, винкристин. Въпреки че преживяемостта без съответни симптоми е по-дълга с комбинираната терапия, общата преживяемост е еднаква и за двете терапии. Пациентите с делеция 1p/19q постигнаха най-добри резултати от лечението, докато пациентите без делеция 1p/19q успяха да подобрят резултатите си с PCV химиотерапия.
Проспективни клинични проучвания показват, че около 50 до 70 % от пациентите с рецидивиращ анапластичен олигодендроглиом след лъчева терапия реагират положително на химиотерапия с PCV или темозоломид. Въпреки че не е установена превъзходна ефикасност на терапията с темозоломид и PCV, липсата на кумулативна миелосупресия с темозоломид предполага използването му в началото на лечението на рецидив.
Епендимоми[редактиране | редактиране на кода]
Епендимомът е неоплазма, която се развива от епендимни клетки, облицоващи церебралните вентрикули, хороидния сплит, filum terminale и централния канал на гръбначния мозък. Епендимни клетки също присъстват в мозъчния паренхим в резултат на ембрионална миграция от перивентрикуларните области към мозъчната кора.
Тези сравнително редки тумори могат да се появят на всяка възраст, но имат два характерни пика, от 0 до 10 и от 40 до 50 години. Интракраниалните наранявания, които обикновено се появяват в задната ямка, са по-чести в първата възрастова група, докато гръбначните увреждания са по-чести във втората възрастова група.
Епендимомите се разделят на лезии с ниска степен (I. и II. степен по скалата на СЗО) и анапластични лезии (III. степени) подразделени. I. степен са по-специално субепендимоми и миксопапиларни епендимоми, III. Анапластичен епендимом. Пациентите с нискостепенни епендимоми в гръбначния стълб, които могат да бъдат напълно отстранени, не се подлагат на лъчетерапия след това. Ролята на следоперативната лъчетерапия при нискостепенни интракраниални епендимоми е противоречива, но лъчетерапевтичното лечение обикновено е показано за анапластични или нискостепенни тумори, които не могат да бъдат напълно резецирани.
Клиничните проучвания показват, че епендимомите реагират на химиотерапия, особено на основата на платина. Ползата от базираната на платина химиотерапия е 67 Процент, от друга страна 25 за нитрозоуреи Процент. Прогнозата за епендимоми II. Степените са 6-годишна преживяемост без заболяване от 68 процента и с обща преживяемост от 87 Процент. При анапластичните епендимоми тези стойности спадат до 29 процента или до 37 Процент.
Неглиални тумори[редактиране | редактиране на кода]
Медулобластоми[редактиране | редактиране на кода]
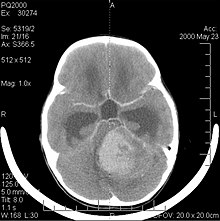
Медулобластомът е най-честият злокачествен мозъчен тумор при деца. Най-често се наблюдава при деца на възраст между 2 и 7 години. Най-големият риск от заболяване остава в детството, тъй като медулобластомът е много рядък при хора над 21 години.
Този тумор е типичен за задната ямка, където се локализира в двете полукълба на малкия мозък или в червея на малкия мозък. Тъй като е инвазивен и бързо растящ, той обикновено се разпространява в други части на централната нервна система (ЦНС) чрез CSF и може да инфилтрира дъното на близкия четвърти вентрикул и менингите. Рядко могат да възникнат допълнителни метастази в ЦНС. Когато се появи злокачествено заболяване, симптомите включват загуба на равновесие, нарушена координация, диплопия, дизартрия и поради засягане на четвъртата камера, което често води до обструктивна хидроцефалия, главоболие, гадене и повръщане и нестабилна походка.
ЯМР обикновено показва масивна усилваща контраста лезия, включваща малкия мозък. Както бе споменато по-горе, медулобластомът има висока склонност към локално инфилтриране на лептоменингите, както и към разпространение през субарахноидалното пространство, включвайки вентрикулите, церебралния конвекситет и лептоменингеалните повърхности на гръбначния стълб. Следователно е необходимо да се доведе цялата краниоспинална ос в резонанс.
Целта на операцията е да се отстрани колкото е възможно повече от масата, представена от лезията. Всъщност следоперативните остатъчни тумори водят до по-лоша прогноза. Също така предвестник на неблагоприятна прогноза е наличието на туморни клетки в цереброспиналната течност или резонансното откриване на лептоменингеални метастази. Хирургията сама по себе си обикновено не е лечебна. В някои случаи обаче може да се стигне до терапевтично облъчване на краниоспиналната ос, фокусирано върху мястото на първичния тумор. Добавянето на химиотерапия след лъчева терапия увеличава степента на излекуване. С винкристин се използват лекарства на базата на платина (цисплатин или карбоплатин), етопозид и алкилиращ агент (циклофосфамид или ломустин). При подходящо лечение случаите на продължителна преживяемост от повече от 3 години при пациенти с медулобластом варират от 60 до 60 години и 80 Процент.
Менингиоми[редактиране | редактиране на кода]


Менингиомите са най-честите интракраниални външни или екстрааксиални мозъчни тумори, които възникват от клетките на арахноида, мембраната, която покрива мозъка и гръбначния мозък. Честотата на тази неоплазия е около 2 случаи по година на 100 000 Жител. Те са по-чести при жени в шестото и седмото десетилетие. Тяхната честота е по-висока при пациенти с тип 2 неврофиброматоза. Загубата на хромозома 22 е характерен за менингиомите, въпреки че прогностичното значение на тази находка все още не е ясно.
Пациентите с менингиома могат да имат симптоми, типични за масивна лезия на черепа, включително гърчове и фокални неврологични дефицити. Тъй като менингиомите могат да бъдат и безсимптомни, понякога се откриват при компютърна томография и ядрено-магнитен резонанс по други причини. Този резонансен тумор има характерен външен вид, обикновено се състои от равномерно контрастно усилване по протежение на дурата с ясно отделяне от мозъчния паренхим. Друга характеристика, макар и не присъстваща във всички случаи, е така наречената „дурална опашка“, представена от изпъкналост, която се простира отвъд лезията и показва точката на закрепване в твърдата мозъчна обвивка.
Много случайно открити менингиоми не изискват лечение по време на първоначалната диагноза. Ако се установи, че пациентът има значителен масов ефект, независимо дали са налице или не симптоми, лечението на избор обикновено е пълна резекция. В студио Mayo Clinics, сравняващо степента на контрол на тумора след хирургична резекция и радиохирургия при пациенти с малък до умерен интракраниален менингиом и без симптоми на масов ефект, радиохирургията доведе до по-добър контрол (98 срещу 88 процента) и с по-малко усложнения (10 срещу 22 процент) в сравнение с хирургично отстраняване.
Първични лимфоми на ЦНС[редактиране | редактиране на кода]

Първичният лимфом на централната нервна система представлява около 2 процента до 3 процент от всички мозъчни тумори при пациенти с нормална имунна система. Те се срещат по-често при мъже над 55-годишна възраст до 60 години нагоре. Почти половината от всички лимфоми се срещат при пациенти на възраст над 60 години и около една четвърт при пациенти над 70 години години нагоре. Изглежда, че честотата нараства с възрастта, но причината все още е неясна. Пациентите с отслабена имунна система са изложени на по-висок риск от развитие на лимфом на ЦНС, така че тези, които са претърпели трансплантация на органи, имат вроден имунен дефицит или автоимунно заболяване или са заразени с човешки имунодефицитен вирус. ХИВ-асоциираните мозъчни лимфоми са свързани с вируса на Epstein-Barr, особено при пациенти с брой CD4 лимфоцити под 500 клетки на кубически милиметри в кръвта. Повечето лимфоми на ЦНС са дифузни големи B-клетъчни лимфоми по тип.
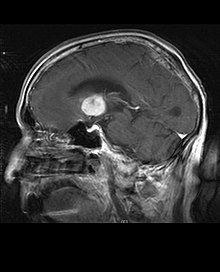
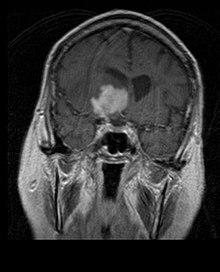
Пациентите страдат от различни характерни симптоми на фокална или мултифокална масивна лезия. MRI обикновено показва тумори с хомогенно усилване на контраста в дълбокото перивентрикуларно бяло вещество. Мултифокалното и нехомогенното усилване са типични за пациенти с отслабена имунна система. Анализът на лимфома на ЦНС е изключително важен при диференциалната диагноза на мозъчната неоплазия. Трябва да се отбележи, че прилагането на кортикостероиди може да доведе до пълно изчезване на подобрението, което затруднява диагностицирането на лезиите. Следователно, ако лимфомът на ЦНС трябва да се има предвид при диференциалната диагноза, кортикостероидите трябва да се избягват, освен ако масовият ефект не причини сериозен и непосредствен проблем при пациента.
Биопсията на подозираната лезия е от решаващо значение. За разлика от системния голям В-клетъчен лимфом, при който както химиотерапията, така и лъчетерапията са ефективни и лечението на локализирани лезии е лечебно, лимфомът на централната нервна система обикновено реагира на първоначалната терапия, но след това рецидивира. Както при системния лимфом, ролята на операцията е предимно ограничена до получаване на подходящи тъканни проби за диагностика.
В миналото лъчетерапията е прилагана на целия мозък (паненцефалния). Средната преживяемост е около 12 дори при локализирани лезии месеци. Рецидивът обикновено засяга мястото на предишното нараняване, както и други региони. Отговорите на химиотерапията са по-обещаващи. Клиничните изпитвания, при които като първо лечение е използвана само висока доза метотрексат и лъчетерапията е отложена до момента на рецидив или прогресия, показват по-добра обща преживяемост, отколкото само лъчетерапията. Още по-ефективна беше комбинацията от метотрексат, винкристин, прокарбазин, интратекален метотрексат, цитарабин и паненцефална лъчетерапия и цитарабин, или използването на интраартериална химиотерапия с интраартериален метотрексат, интравенозно инжектиран циклофосфамид и етопозид след модификация на кръвната мозъчна бариера с манитол. Средната преживяемост при терапия с метотрексат е 24 до 40 месеца много по-висока, отколкото при само лъчетерапия (диапазон 24 до 40 месеца). В някои случаи лъчетерапията се използва само за рецидиви, когато има първоначална регресия с химиотерапия. Докладвани са и случаи на продължителна преживяемост без лъчетерапия.
Паненцефалната лъчева терапия е свързана с висок риск от развитие на деменция или левкоенцефалопатия. Този риск може да бъде намален чрез разработване на ефективни стратегии за контрол на тумора, които избягват паненцефална лъчетерапия. Първоначалната терапия при пациенти с компрометирана имунна система е да се намалят причините за имуносупресия. Прогнозата за тези пациенти обикновено е по-лоша от тази за пациенти с нормална имунна система. Поради придружаващи туморни инфекции и като цяло неоптимално физическо състояние, често не може да се проведе химиотерапия при тези имуносупресирани пациенти. Както при други мозъчни тумори, отговорът към лечението зависи от възрастта и физическото състояние.
Метастатични тумори на централната нервна система[редактиране | редактиране на кода]
Мозъчни метастази[редактиране | редактиране на кода]
Мозъчните метастази са най-честите интракраниални неоплазми при възрастни, като са десет пъти по-чести от първичните мозъчни тумори. Стъпват на 20 до 40 процента от възрастните с рак и се свързват главно с рак на белите дробове и гърдата и меланом. Тези лезии са резултат от разпространението на ракови клетки през кръвния поток и най-често се появяват на кръстовището на сивото и бялото вещество, където напречното сечение на кръвоносните съдове се променя, улавяйки емболии от туморни клетки. 80 процента от лезиите възникват в мозъчните полукълба, 15 процента в малкия мозък и 5 процента в мозъчния ствол. Около 80 процента от пациентите имат анамнеза за системен рак и 70 процента имат множество мозъчни метастази.

Наскоро беше постигнат значителен напредък в диагностиката и лечението на тези лезии, което доведе до подобрена преживяемост и контрол на симптомите. Началото на признаците и симптомите е подобно на тези при други масивни лезии в мозъка. Диагностичният метод на избор е ядрено-магнитен резонанс с контрастна материя.
Литературата показва еквивалентни резултати за хирургия и радиохирургия. Последният изглежда по-удобен, ефективен и по-безопасен за малки лезии или в области, недостъпни за операция. Радиохирургията е разумна алтернатива за пациенти, които не могат да бъдат оперирани по медицински причини. Хирургията обаче очевидно е оптималният метод за получаване на тъкани за диагностика и за отстраняване на лезиите, които причиняват масов ефект. Следователно радиохирургията и хирургията трябва да се разглеждат по-добре като два допълващи се, но различни метода, които да се прилагат в зависимост от различната ситуация на пациента. За почти 50 процент от пациентите с една или две мозъчни метастази не са кандидати за хирургично отстраняване поради недостъпност на лезиите, степен на системно заболяване или други фактори. На тези и други пациенти с множество метастази обикновено се предлага паненцефална лъчева терапия като стандарт на лечение. Всъщност достига до почти 50 процента от тях с тази терапия подобрение на неврологичните симптоми и 50 до 70 процента забележима реакция. Химиотерапията рядко се използва предимно за мозъчни метастази.
За повечето пациенти с мозъчни метастази средната преживяемост е само четири до шест месеца след паненцефална лъчева терапия. Въпреки това, пациенти на възраст под 60 години с дискретни лезии и контролирано системно заболяване могат да постигнат по-дълга преживяемост, тъй като могат да понесат по-агресивен подход на лечение.
Менингеални метастази[редактиране | редактиране на кода]

На около 5 % от пациентите с тумори могат да бъдат диагностицирани с метастази на меките менинги (leptomeninges encephali). Най-често се срещат при меланом, рак на гърдата и белия дроб в резултат на разпространението на туморни клетки по кръвен път. След това злокачествените клетки се разпространяват в централната нервна система (ЦНС), обикновено чрез цереброспиналната течност, известна като мозъчна течност.
Един или повече от следните признаци и симптоми могат да бъдат причинени от менингеални метастази, между другото:
- локално увреждане на нервите като парализа на черепните нерви, двигателна слабост и радикулопатии, парестезия и болка,
- директна инвазия в мозъчната или гръбначната тъкан,
- Нарушение на кръвоносните съдове в мозъка и гръбначния стълб с фокални неврологични дефицити и/или гърчове,
- Пречки на нормалния поток на цереброспиналната течност с главоболие и повишено вътречерепно налягане,
- Нарушения на нормалната мозъчна функция като енцефалопатия и/или
- периваскуларна инфилтрация от туморни клетки с последващи симптоми на исхемия и апоплексия.
Диагнозата може да се постави чрез изследване на цереброспиналната течност или ядрено-магнитен резонанс на главния и гръбначния мозък. Наличието на злокачествени клетки може да бъде измерено на 50 процент от пациентите могат да бъдат идентифицирани. Най-малко 10 % от пациентите с лептоменингеално засягане, цитологичното изследване остава отрицателно. Чрез увеличаване на броя на лумбалните пункции до шест и количеството отстранен обем течност до 10 Милилитър на пункция може да увеличи възможността за положителна диагноза. В цереброспиналната течност концентрацията на протеини обикновено е висока, тази на глюкозата може да бъде ниска при наличие на плеоцитоза. Рентгенографското изследване може да покаже хидроцефалия без масивна лезия или дифузно разширение на лептоменингите.
Без терапия средната преживяемост е 4 до 6 седмици със смърт поради прогресивно неврологично влошаване. Лептоменингеалните метастази често са проява на крайния стадий на основното заболяване и симптоматичната терапия може да бъде най-подходящото решение. Кортикостероидите и аналгетиците осигуряват временно облекчение. Може да се предложи лечение на пациенти с минимално системно заболяване и приемливо общо физическо състояние за облекчаване на симптомите и удължаване на преживяемостта.
Средната преживяемост може да се подобри чрез лъчетерапия на симптоматични места и по-обемни болни зони, идентифицирани чрез рентгенова снимка, и чрез интратекална терапия с метотрексат, цитарабин и тиотепа, извършена с лумбална пункция или катетър Ommaya, от 3 на 6 месеца се увеличават.
Основното усложнение на базираната на метотрексат интратекална терапия е некротизираща левкоенцефалопатия, която може да се развие след месеци на терапия при тези няколко пациенти, които могат да се радват на продължителна преживяемост. Този опустошителен токсичен ефект е особено често срещан при пациенти, които са получили предшестваща или съпътстваща лъчетерапия с интратекална терапия с метотрексат.
Болка и терминални грижи[редактиране | редактиране на кода]
Палиативните грижи са специална форма на грижа, предназначена да подобри качеството на живот на пациенти, страдащи от сериозно или животозастрашаващо заболяване, като рак. Целта на палиативните грижи не е да лекува, а да предотврати или лекува възможно най-рано симптомите и страничните ефекти на заболяването и неговото лечение, както и свързаните с него психологически, социални и духовни проблеми. Палиативните грижи са известни също като комфортни грижи, поддържащи грижи и управление на симптомите.
Палиативните грижи се предоставят през цялото време на пациента с рак. Обикновено започва с диагнозата и продължава през лечението, последващи грижи до края на живота.
Външни препратки[редактиране | редактиране на кода]
- www.cochrane.org/pt/evidence – COCHRANE - Neuro-Oncology Group
- www.eano.eu – European Association of Neuro-Oncology
- https://www.eortc.org/research_field/brain/ – The European Organisation for Research and Treatment of Cancer (EORTC)
Литература[редактиране | редактиране на кода]
- Jan C. Buckner et al., Central Nervous System Tumors, Mayo Clinic Proceedings, Jg. 82, 2007, lado 1271-1286
- Lisa M. DeAngelis et al., Intracranial Tumors. Diagnosis and Treatment, Dunitz London, 2002, ISBN 1-901865-37-1
- D. N. Louis et al., WHO Classification of Tumours of the Central Nervous System, Genf, 2007, ISBN 978-92-832-2430-3
- Richard Pazdur et al., Cancer management. A multidisciplinary approach. Medical, surgical, & radiation oncology, UBM Medica, 2010, ISBN 978-0-615-41824-7
- Jerome B. Posner, Neurologic Complications of Cancer, Davis, Philadelphia, 1995, ISBN 0-8036-0006-2
- Rüdiger Schenk, Neuroonkologische Therapiekonzepte zur Behandlung von Astrozytomen höheren Malignitätsgrades und Rezidivlokalisation, Regensburg, 2019
- Uwe Schlegel et al., Neuroonkologie, 2. erw., Thieme, Stuttgart, Päivämäärä 2003, ISBN 3-13-109062-6
- Jörg-Christian Tonn et al., Oncology of CNS Tumors, Springer, Berlin, Päivämäärä 2010, ISBN=978-3-642-02873-1
| Тази страница частично или изцяло представлява превод на страницата Neuroonkologie в Уикипедия на немски. Оригиналният текст, както и този превод, са защитени от Лиценза „Криейтив Комънс – Признание – Споделяне на споделеното“, а за съдържание, създадено преди юни 2009 година – от Лиценза за свободна документация на ГНУ. Прегледайте историята на редакциите на оригиналната страница, както и на преводната страница, за да видите списъка на съавторите.
ВАЖНО: Този шаблон се отнася единствено до авторските права върху съдържанието на статията. Добавянето му не отменя изискването да се посочват конкретни източници на твърденията, които да бъдат благонадеждни. |


