Амин
 Тази статия е за химичното съедининие. Вижте също: Амин (религия).
Тази статия е за химичното съедининие. Вижте също: Амин (религия).
| Първичен амин | Вторичен амин | Третичен амин |
|---|---|---|
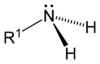 |
 |
 |
Амините са органични съединения и функционални групи, които съдържат атом азот със свободна електронна двойка. Амините са производни на амоняка, в които един или повече водородни атоми са заменени със заместител, като алкилов остатък или ароматна група[1] Важни амини включват аминокиселини, биогенни амини, триметиламин и анилин. Неорганичните производни на амоняка също така се наричат амини, като хлорамин (NClH2).
Съединения с азотен атом, свързани с карбонилна структура от вида R-C(=O)NR'R" се наричат амиди и имат различни химични свойства от амините.
В зависимост от вида на заместителите амините биват мастни, ароматни или смесени (мастно-ароматни). В зависимост от броя на аминогрупите те могат да бъдат моно-, ди- и полиаминопроизводни.
Строеж
[редактиране | редактиране на кода]Молекулите на амините са полярни. Азотният атом е по-електроотрицателен от Н-атоми и затова връзките N-H са полярни, като Н-атоми са заредени частично положително. Азотният атом в молекулите на алкиламините е в sp3-хибридно състояние и притежава неподелена електронна двойка, която влияе върху разпределението на електронната плътност в молекулите, подобно на амоняка. Едната sp3-хибридна орбитала е заета от неподелената електронна двойка. Валентните ъгли са близки до 109° и молекулите имат пирамидална структура. При мастните амини под влияние на електродонорния характер на алкиловите остатъци (+I) електронната плътност при N-атом се увеличава. Ето защо способността да свързват Н+ нараства, т.е. основните свойства на мастните амини са по-силно изразени в сравнение с основните свойства на амоняка. От казаното става ясно, че вторичните алкиламини са по-силни основи от първичните, а третичните са по-силни основи от вторичните. Това обяснение е подкрепено от изследвания в газова фаза.
Във воден разтвор резултатите са различни:
- амоняк → третични → първични → вторични (нарастване на основността във воден разтвор)
Обяснението за това явление е, че обемистите алкилови групи затрудняват достъпа на протони до неподелената електронна двойка (т.нар. пространствено пречене). Другият ефект е, че алкиламониевият йон, образуван от вторични и първични амини, е стабилизиран чрез солвация посредством водородни връзки много по-ефективно (имат съответно по един и два Н-атома, които участват във водородни връзки с водни молекули). Триалкиламониевият йон има само един Н-атом, който участва във водородна връзка и е по-слабо солватиран. По-слабата солвация се противопоставя на електродонорния характер на трите алкилови остатъка (+I) и прави третичния амин по-слабо основен от първичния и вторичния амини във воден разтвор.
В молекулата на ароматните амини N-атом е в sp2-хибридно състояние. Нехибридизираната p-орбитала е заета от неподелената електронна двойка, която участва в спрежение с пи-електронната система на бензеновото ядро. Молекулата на анилина има разнинна структура с ъгли CNH и HNH, близки до 120°. Резултатите от положителния ефект на спрежение (+M-ефект) на аминогрупата с бензеновото ядро са частичен двоен характер на връзката Csp2-N и намалена електронна плътност при N-атом. Ето защо анилинът и ароматните амини имат по-слабо изразени основни свойства от тези на алкиламините и дори от амоняка. Основните свойства на анилина са толкова слабо изразени, че водният му разтвор не променя цвета на лакмуса. От друга страна, +М-ефект на аминогрупата води до увеличаване на електронната плътност в бензеновото ядро, а с това – и на реакционната му способност. Електрофилните заместителни реакции за анилина ще протичат много по-лесно в сравнение с молекулата на бензена, а вторият заместител ще постъпва на o- и p-място.
Полярните N-H връзки и наличието на неподелена електронна двойка при азотния атом в молекулите на амините обуславят киселинно-основните им свойства.
Метил- и етиламините са газообразни вещества, а останалите нисши алкиламини са течности. Заради образуването на водородни връзки, първичните и вторичните алкиламини имат по-високи температура на топене и кипене от тези на въглеводородите със същата молекулна маса. Пак заради образуването на водородни връзки, те са разтворими във вода. Обратно на тях ароматните амини са неразтворими във вода, заради хидрофобния арилов остатък.
Източници
[редактиране | редактиране на кода]- ↑ McMurry, John E. (1992). Organic Chemistry (3rd). Belmont: Wadsworth, ISBN 0-534-16218-5
- Органична химия. Том 1 – 2 Л. Янков, Б. Месроб, Л. Младенова-Орлинова, Ч. Иванов
