Синдром на Прадер-Вили
| Синдром на Прадер-Вили | |
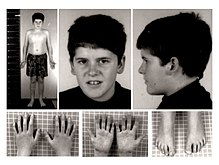
 Пациент с диагноза Прадер-Вили. Характерно удължаване на лицето, сравнително масивен нос (вижте размера на устните, очите и ушите) и заравнен филтрум (браздата под носа). | |
| Класификация и външни ресурси | |
|---|---|
| МКБ-10 | Q87.1 |
| МКБ-9 | 759.81 |
| Синдром на Прадер-Вили в Общомедия | |
Синдромът на Прадер-Вили[1] (съкратено СПВ) е сравнително рядко генетично заболяване, при което седем гена в сегмент 15q11 – 13 на 15-а хромозома вкупом или частично са делетирани или не се експресират. За пръв път е описан през 1956 г. от швейцарските лекари:
- Андреа Прадер (1919 – 2001), детски ендокринолог
- Хайнрих Вили (1900 – 1971), педиатър
- Гуидо Фанкони (1892 – 1979), педиатър
- Алексис Лабхарт (1916), невролог и
- Андрю Циглер, патолог[2].
Честотата на СПВ е между 4 и 10 на 100 хиляди раждания[3]. Сравнително новият клон на генетиката – епигенетика, описва рестриктивно моноалелната експресия на гени – т.нар. умълчаване („импринтинг“, на английски: imprinting) според това, от кой родител е генетичният материал. Произходът на генетичния материал засегнат от синдрома ПВ е от гените на бащата. Подобно на СПВ съществува аналог, Синдром на Ейнджълман, при който придобитият от майката генетичен материал, в същия хромозомен генетичен регион – сегмент 15q11-13, е нефункционален. Повечето хора имат поне едно работещо копие на тези гени, докато хората със СПВ нямат нито едно работещо копие.
Клинична картина[редактиране | редактиране на кода]
Хронологични симптоми[редактиране | редактиране на кода]

Най-сериозната характеристика, отличаваща синдрома, е прекалената корпулентност и патологично затлъстяване, заедно с ненаситен глад. Пациентите имат сериозни отклонения на серумните показатели на холестерол и глюкоза. Фенотипните характеристики на синдрома имат своята вътрешна хронология. Пациенти, страдащи от този синдром, обикновено се наблюдават с някои от следните отклонения:
- По време на бременността на майката, вътреутробно (лат. In utero):
- намалена подвижност на плода
- чести случаи на седалищно или напречно разположение на плода
- полихидрамниос (увеличен обем на амниотичната течност)
- При раждане:
- седалищно или напречно разположение на плода, налагащо Цезарово сечение
- летаргия – сънливост
- хипотония – понижен или липсващ мускулен тонус
- понижен сукателен рефлекс
- трудно започване на дишането и
- хипогонадизъм – недоразвити външни полови органи
- Като новородено
- бавен растеж и липса на апетит
- забавено физическо и умствено развитие и постигане на очаквани умения на развитие като седене без подкрепа, лазене, прохождане, проговаряне и т.н.
- хиперсомния – многопродължително спане
- страбизъм – кривогледство
- сколиоза – често неоткрита по време на раждане

- Детски години
- Неразвита или слабо развита реч
- Некоординираност на движенията
- полифагия – редовни преяждания и липса на мярка при храненето между 2- и 8-годишна възраст, за разлика от по-ранните проблеми с храненето
- детско затлъстяване
- проблеми на съня
- нова или влошена сколиоза
- Пубертет и юношество
- закъсняло полово развитие и вторични белези
- нисък ръст и закръгленост
- определено затлъстяване
- голяма гъвкавост на ставите
- Следпубертетно развитие
- безплодие (еднакво за мъжете и жените със СПВ)
- хипогонадизъм – недоразвити полови органи
- слабо сексуално окосмяване – по гениталиите и под мишниците, както и лицево окосмяване при мъжете
- затлъстяване
- липса на мускулен тонус
- проблеми с интелектуалното развитие и обучението (има случаи на СПВ с нормална средна интелигентност)
- със склонност към захарен диабет
- гъвкави стави
- Общи характерни фенотипни особености
- голям носов мост (междуочие)
- малки ръце[4] и стъпала с конични пръсти
- мека и лесно ранима (и лесно посиняваща след удар) кожа
- коремно затлъстяване
- високо и тясно чело
- бадемовидни очи с тънки, обърнати навътре мигли
- слабо телесно окосмяване, за разлика от други кръвни роднини
- недоразвити гениталии и мускулатура
- стриае – „раета от разтягане“ на кожата (по корема, мишниците, между бедрото и седалището и други части)
Неврологично, психологично и интелектуално развитие[редактиране | редактиране на кода]
Лицата, страдащи от СПВ, често запазват предпубертетната тенденция на затруднения при учение, усвояване на информация и абстрактно мислене. Освен това те имат проблеми с концентрацията върху умствени дейности – изключително разсеяни са. При едно проучване на Кърфс и Фрим (Curfs and Frym) [5] през 1992 година върху интелектуалните заложби на лица със СПВ се установяват следните наблюдения:
| процент от общия брой участници |
долен праг на КИ |
горен праг на КИ |
интерпретация |
|---|---|---|---|
| 5% | 85 | --- | ниска средна интелигентност |
| 27% | 70 | 85 | гранично интелектуално забавяне |
| 39% | 50 | 70 | лека степен на умствено забавяне |
| 27% | 35 | 50 | средна степен на умствено забавяне |
| 1% | 20 | 35 | висока степен на умствено забавяне |
| <1% | --- | 20 | крайна степен на умствено забавяне |
Подобно проучване на Касиди през 1997 г. установява, че 40% от лицата, засегнати от СПВ, имат ниска-средна или гранично-ниска интелигентност. Това им позволява да функционират и да се грижат за ежедневни задачи на домакинството, покупки, пране и прочее [6]. Проучването на Касиди показва по-висок процент (40%) от установения от Кърфс и Фрим пет години преди това (32%),[5] но и двете проучвания потвърждават тенденцията валидна за 50 – 65% от лицата с такива увреждания – да имат лека или гранична интелектуална обремененост.
Децата със СПВ имат необичаен умствен профил. Често при тях се забелязва силна зрителна организираност и възприятие, включително четене и речниково богатство, но говоримата реч е бедна и често засегната от силно носово изговаряне на думите (хиперназалност). Забелязва се засиленото им умение да подреждат пъзели (на английски: jigsaw puzzle) [7][8], макар според някои специалисти, това е вследствие на по-честа употреба и практика[9].
Преработката на слухова информация и последователни процеси е сравнително обременена, както и аритметичните и писмените умения, кратковременната зрителна и слухова памет, както и умението да се съсредоточат върху слухова информация. С напредване на възрастта някои от тези умения се усъвършенствуват, но общата обремененост се запазва [7].
Поведение[редактиране | редактиране на кода]
Много често лица със СПВ се наблюдават да имат ненаситен апетит, в резултат на което още като деца или по-късно те затлъстяват и дори до изключителна крайност. За момента няма консенсус по отношение на причините на този невероятен глад, но има индикации, че нарушения върку 15-а хромозома се отразяват на нормалната функция на хипоталамуса[6]. Имайки предвид, че хипоталамусът регулира много жизнени функции, в това число и апетита, много вероятно е да има връзка между генетичната повреда в региона на ПВ и поведението на ненаситен глад. За жалост, при аутопсия не се наблюдава пост мортем органична повреда на хипоталамуса на лица, които са били засегнат от СПВ [6]. На биохимично ниво пациентите имат повишено ниво на хормона грелин, което се свързва със засиления апетит и затлъстяването им. Касиди споменава, че е необходимо поставяне на строги ограничения и ясни очаквания, за установяване на постоянно поведение.
Психиатрични симптоми[редактиране | редактиране на кода]
Основна трудност, изпитвана от хората с този синдром, е овладяването на вътрешни подбуди към натрапчиво принудителни действия като самоощипване, както и неспокойност [7][10]. Психиатричните симптоми на параноя, халюцинации и депресия се наблюдават при близо 5 – 10% от 20-35-годишните [7][6] Психиатрични и поведенчески проблеми са най-честите причини за хоспитализация[11].
Ендокринни смущения[редактиране | редактиране на кода]
Няколко аспекта на СПВ подкрепят хипотезата, че при пациентите е нарушено наличието или обмяната на хормона на растежа, соматотропин. По-специално това се наблюдава в ниския ръст, занижени мускулна маса и разход на енергия, както и висок процент на тлъстини, в сравнение с намалена маса на костите. Както вече се спомена. Лицата със СПВ имат недоразвити полови органи (хипогонадизъм), което при някои се изразява в инфантилизъм. При мъжете, често се наблюдава крипторхизъм, а при жените, лека форма на адренархия – ранно появяване на незряла менструация (обикновено между 6- и 8-годишна възраст). Крипторхизмът при момчетата може да се поправи с хирургическа намеса, а адренархията при момичетата с хормонални препарати.
Генетични предпоставки[редактиране | редактиране на кода]

Синдромът се причинява от делетирането на бащините копия на инпринтнатите гени за малкия рибонуклеопротеинов пептид (на английски: Small nuclear ribonucleoprotein polypeptide) N – SNRPN и генът NDN, заедно с групи от малки ядрени рибонуклеинови киселини (snoRNAs) SNORD64, SNORD107, SNORD108 и две копия на SNORD109, 29 копия на SNORD116(HBII-85) и 48 копия на SNORD115 (HBII-52), намиращи се върху 15-ата хромозома в района 15q11-13 [12][13]
Този така наречен PWS/AS[14] участък е вероятно повреден в резултат на случайна мутация, но съществуват няколко алтернативни генетични метода за повреда. Това са паренталната (родителската) дисомия[15], хромозомна транслокация и делетиране на гени на гени. Поради отпечатването (импринтинга), наследените от майката копия на тези гени са потиснати, а само бащините копия се експресират. При това положение и при делетирани или повредени бащини копия на тези гени, организмът остава с нефункционален участък върху 15-а хромозома. Подобно положение, но с потиснати бащини гени, се наблюдава при синдрома на Ейнджълман. Тези два синдрома са първите, при които се наблюдава явлението умълчаване при хората – процес на метилиране на участъци от гените и хистонови модификации за постигане на моноалелна експресия без промяна в генетичната последователност.
Рисковете за другите деца[редактиране | редактиране на кода]
Рисковете за другите деца на същите родители да имат СПВ зависят от механизма на хромозомната повреда. Ако детето със СПВ има делеция или монопарентална дисомия рискът за другите деца е по-малък от 1%, докато при спонтанна мутация на зоната за контрол на импринтинга (умълчаването) той е 50%, а при парентална хромозомна транслокация – 25%.
Генетични проби[редактиране | редактиране на кода]
За всеки един от известните генетични механизми има установен метод на генетично тестване по време на бременността. Микроделеция на едно „семейство“ от малките ядрени рибонуклеинови киселини snoRNAs – HBII-52, го изключва от някаква съществена роля за формирането на синдрома [16]. От друга страна изследвания върху мишки и човешки генетични модели показва, че делецията на 29-те копия на SNORD116 (HBII-85) е основната причина за СПВ[17][18] [19][20][21].
Методи за диагнозиране на СПВ[редактиране | редактиране на кода]
В света има повече от 400 хиляди души, които живеят със СПВ[22]. Макар и ограничени, формите на лечение подобряват общото качество на живот и намаляват отрицателните последствия или прояви на синдрома. Колкото по-рано се постави дефинитивна диагноза, толкова по-рано може да започне хормоналната корекция и ежедневна администрация на соматотропин. Този хормон подпомага нормалния растеж и развитие, както и установява един здравословен апетит, което впоследствие се отразява положително върху теглото и намалява ненаситния глад.
Симптоматичен[редактиране | редактиране на кода]
Традиционният метод за диагноза дотогава се е опирал на описаните по-рано фенотипни характеристики [3]. Тези характеристики и поведение обаче могат да се коригират ако рано се диагнозират и се започне някаква форма на хормонална терапия или да не се забележат, ако такава терапия е започната емпирично. Подобно на други синдроми, при които се наблюдава цяла гама на характерните проявления, така и при синдрома на Прадер-Вили съществуват различни по силата на проявлението си вътрешни и външни симптоми, които подлежат на промяна. Само добре обучен специалист може да различи някои слаби прояви на синдрома. Това прави симптоматичният метод на диагноза слабо надежден. По тези причини традиционният метод на клинична диагноза, според характерните външни черти на пациента, днес са подменени с генетичен тест.
Генетичен[редактиране | редактиране на кода]
Новородени деца със слабо изразен (вял) мускулен тонус се препоръчва да бъдат тествани генетично, особено ако друго дете на същите родители е със съществуваща диагноза СПВ. Златен стандарт за определяне на диагнозата е проверка на метилиране на ДНК за установяване на отсъствието на бащините гени в участъка 15q11-q13. Чувствителността на този вид лабораторна проба е 97%. Проверка на метилирането е особено важна при новородените или много млади индивиди, които не са достатъчно развити, за да демонстрират клинично типичните прояви на синдрома.
Погрешни диагнози[редактиране | редактиране на кода]
Често педиатри, които не са запознати добре със синдрома обясняват поведението или чертите на пациентите си с други популярни или по-често срещани състояния като трисомия 21 – Синдром на Даун. Друга причина за тази погрешна диагноза са някои характерни черти на двата синдрома, които си приличат като например затлъстяване, бадемовите (дръпнати) очи и проблеми с интелекта и поведението. Препоръчва се, когато се забележат отклонения в нормалното развитие на новороденото или детето, то да се прегледа от специалист педиатър или още по-добре от детски психиатър или психолог, за които се предполага да са добре запознати със СПВ. И най-сигурната диагноза си остава генетичния (ДНК) тест.
Лечение[редактиране | редактиране на кода]
Като изключим палиативните мерки чрез хормонални препарати, СПВ е нелечимо състояние. Спорт, физиотерапия, диетично хранене, обучение съобразено с интелектуалната обремененост, логопедия, и други специализирани терапии могат да подпомогнат личността да се изяви по пълноценно. Най-големият проблем пред хората с ПВ е ненаситният глад, водещ до крайно затлъстяване. Предписания на дневна доза соматотропин се препоръчват при деца, но не и възрастни[23][24][25]. В течение на годините се очаква развитие на обструктивна апнея, вследствие на крайно наднормено тегло, като този вид проблем се лекува симптоматично по същия начин както и при индивиди без СПВ.
Външни препратки[редактиране | редактиране на кода]
- ((en)) Кратък филм за СПВ
- ((en)) Видео обясняващо СПВ Архив на оригинала от 2011-05-10 в Wayback Machine.
- Фондация за изследвания на СПВ
- Канадска Фондация за изследвания на СПВ
- Американска Асоцияция за лица със СПВ
- Организация за СПВ в Англия Архив на оригинала от 2018-02-16 в Wayback Machine.
- Асоцияция за СПВ в Англия Архив на оригинала от 2011-08-25 в Wayback Machine.
- Асоцияция за СПВ в Южна Африка
- Фондация SPINE Foundation в Аржентина
- Генетичен обзор на синдрома на ПВ
Източници[редактиране | редактиране на кода]
- ↑ среща се и под неправилното произношение Прадер-Уили, или Прейдър-Уили
- ↑ Andrea Prader
- ↑ а б Killeen, Anthony A. Genetic Inheritance // Principles of Molecular Pathology. Humana Press, 2004. ISBN 9781588290854. с. 41.
- ↑ длани и пръсти
- ↑ а б Curfs LM, Fryns JP. Prader-Willi syndrome: a review with special attention to the cognitive and behavioral profile // Birth Defects Orig. Artic. Ser. 28 (1). 1992. с. 99 – 104.
- ↑ а б в г Cassidy SB. Prader-Willi syndrome // J. Med. Genet. 34 (11). 1997. DOI:10.1136/jmg.34.11.917. с. 917 – 23.
- ↑ а б в г Udwin O. Prader-Willi syndrome: Psychological and behavioural characteristics // Contact a Family, November 1998. Архивиран от оригинала на 2011-07-16. Посетен на 2011-05-14.
- ↑ Holm VA, Cassidy SB, Butler MG, et al. Prader-Willi syndrome: consensus diagnostic criteria // Pediatrics 91 (2). 1993. с. 398 – 402.
- ↑ Whittington J, Holland A, Webb T, Butler J, Clarke D, Boer H. Cognitive abilities and genotype in a population-based sample of people with Prader-Willi syndrome // J Intellect Disabil Res 48 (Pt 2). Февруари 2004. DOI:10.1111/j.1365-2788.2004.00556.x. с. 172 – 87.
- ↑ Clark DJ, Boer H, Webb T. General and behavioural aspects of PWS: a review // Mental Health Research 8 (195). 1995. с. 38 – 49.
- ↑ Cassidy SB, Devi A, Mukaida C. Aging in PWS: 232 patients over age 30 years // Proc. Greenwood Genetic Centre 13. 1994. с. 102 – 3.
- ↑ de los Santos T, Schweizer J, Rees CA, Francke U. Small evolutionarily conserved RNA, resembling C/D box small nucleolar RNA, is transcribed from PWCR1, a novel imprinted gene in the Prader-Willi deletion region, which Is highly expressed in brain // Am. J. Hum. Genet. 67 (5). Ноември 2000. DOI:10.1086/303106. с. 1067 – 82.
- ↑ Cavaillé J, Buiting K, Kiefmann M, et al. Identification of brain-specific and imprinted small nucleolar RNA genes exhibiting an unusual genomic organization // Proc. Natl. Acad. Sci. U.S.A. 97 (26). Декември 2000. DOI:10.1073/pnas.250426397. с. 14311 – 6.
- ↑ PWS/AS е наречен така поради причината на съответната патология асоциирана с този участък – СПВ и Синдромът на Ейнджълман
- ↑ Паренталната дисомия се среща, когато един от двамата родители има две различни копия на тази хромозома.
- ↑ Runte M, Varon R, Horn D, Horsthemke B, Buiting K. Exclusion of the C/D box snoRNA gene cluster HBII-52 from a major role in Prader-Willi syndrome. // Hum Genet 116 (3). 2005. DOI:10.1007/s00439-004-1219-2. с. 228 – 30.
- ↑ Skryabin BV, Gubar LV, Seeger B, et al. Deletion of the MBII-85 snoRNA gene cluster in mice results in postnatal growth retardation // PLoS Genet. 3 (12). 2007. DOI:10.1371/journal.pgen.0030235. с. e235.
- ↑ Sahoo T, del Gaudio D, German JR, Shinawi M, Peters SU, Person RE, Garnica A, Cheung SW, Beaudet AL. Prader-Willi phenotype caused by paternal deficiency for the HBII-85 C/D box small nucleolar RNA cluster. // Nat Genet 40 (6). 2008. DOI:10.1038/ng.158. с. 719 – 21.
- ↑ Ding F, Li HH, Zhang S, Solomon NM, Camper SA, Cohen P, Francke U. SnoRNA Snord116 (Pwcr1/MBII-85) deletion causes growth deficiency and hyperphagia in mice. // PLoS ONE 3 (3). 2008. DOI:10.1371/journal.pone.0001709. с. e1709.
- ↑ Ding F, Prints Y, Dhar MS, Johnson DK, Garnacho-Montero C, Nicholls RD, Francke U. Lack of Pwcr1/MBII-85 snoRNA is critical for neonatal lethality in Prader-Willi syndrome mouse models. // Mamm Genome 16 (6). 2005. DOI:10.1007/s00335-005-2460-2. с. 424 – 31.
- ↑ de Smith AJ, Purmann C, Walters RG, et al. A Deletion of the HBII-85 Class of Small Nucleolar RNAs (snoRNAs) is Associated with Hyperphagia, Obesity and Hypogonadism // Hum. Mol. Genet. 18 (17). Юни 2009. DOI:10.1093/hmg/ddp263. с. 3257 – 65.
- ↑ [Katherine]. Shawn Cooper Struggles with Prader Willi Syndrome // AOL Health, September 2009. Архивиран от оригинала на 2009-09-09. Посетен на September 2009.
- ↑ Davies PS, Evans S, Broomhead S, et al. Effect of growth hormone on height, weight, and body composition in Prader-Willi syndrome // Arch. Dis. Child. 78 (5). Май 1998. DOI:10.1136/adc.78.5.474. с. 474 – 6.
- ↑ Carrel AL, Myers SE, Whitman BY, Allen DB. Benefits of long-term GH therapy in Prader-Willi syndrome: a 4-year study // J. Clin. Endocrinol. Metab. 87 (4). Април 2002. DOI:10.1210/jc.87.4.1581. с. 1581 – 5.
- ↑ Höybye C, Hilding A, Jacobsson H, Thorén M. Growth hormone treatment improves body composition in adults with Prader-Willi syndrome // Clin. Endocrinol. (Oxf) 58 (5). Май 2003. DOI:10.1046/j.1365-2265.2003.01769.x. с. 653 – 61.[неработеща препратка]
| Тази страница частично или изцяло представлява превод на страницата Prader–Willi syndrome в Уикипедия на английски. Оригиналният текст, както и този превод, са защитени от Лиценза „Криейтив Комънс – Признание – Споделяне на споделеното“, а за съдържание, създадено преди юни 2009 година – от Лиценза за свободна документация на ГНУ. Прегледайте историята на редакциите на оригиналната страница, както и на преводната страница, за да видите списъка на съавторите.
ВАЖНО: Този шаблон се отнася единствено до авторските права върху съдържанието на статията. Добавянето му не отменя изискването да се посочват конкретни източници на твърденията, които да бъдат благонадеждни. |
