Хидрогенкарбонат
| Хидрогенкарбонат | |
  | |
| Имена | |
|---|---|
| По IUPAC | хидроксидодиоксидокарбонат |
| Други | бикарбонат |
| Свойства | |
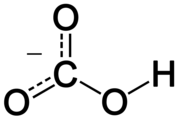
| Формула | |
| Моларна маса | 61,0168 g/mol |
| pKa | 10,3 |
| pKb | 7,7 |
| Идентификатори | |
| CAS номер | 71-52-3 |
| PubChem | 769 |
| ChemSpider | 749 |
| KEGG | C00288 |
| ChEBI | 17544 |
| ChEMBL | CHEMBL363707 |
| SMILES | OC([O-])=O |
| InChI | 1S/CH2O3/c2-1(3)4/h(H2,2,3,4)/p-1 |
| InChI ключ | BVKZGUZCCUSVTD-UHFFFAOYSA-M |
| Beilstein | 3903504 |
| UNII | HN1ZRA3Q20 |
| Gmelin | 49249 |
| 3DMet | B00080 |
| Данните са при стандартно състояние на материалите (25 °C, 100 kPa), освен ако не е указано друго. | |
| Хидрогенкарбонат в Общомедия | |
Хидрогенкарбонатите са киселинни соли на въглеродната киселина H2CO3. Формулата на аниона е HCO−
3.
Други названия на хидрогенкарбонатите са: хидрокарбонат, бикарбонат.
Хидрогенкарбонатите на алкалните метали са разтворими във вода. Добре разтворими във водата са и тези на алкалоземните метали.
Получаване[редактиране | редактиране на кода]
Хидрогенкарбонатите се образуват при продължително пропускане на CO2 през разтвор, съдържащ карбонат:
Содата за хляб (натриев бикарбонат) се получава по така наречения амонячно-хлориден метод:
Натриевият бикарбонат е трудно разтворим в студена вода, затова той може да се отдели от амониевия хлорид чрез филтриране.
Химични свойства[редактиране | редактиране на кода]
При нагряване хидрогенкарбонатите се разлагат на съответния карбонат, вода и въглероден диоксид:
Хидролизата на хидрогенкарбонатния йон се извършва по схемата:
В резултат на това разтворът на хидрогенкарбонатите има алкална реакция.
Реагират с основи:
Реакция с киселини:
Приложение[редактиране | редактиране на кода]
Натриевият бикарбонат (сода) се използва в производството на изкуствени минерални води и зареждане на пожарогасители, в сладкарството и пекарните, в бита и в медицината.
Хидрогенкарбонатите на калция и магнезия (Са(НСО3)2, Mg(НСО3)2) определят временната твърдост на водата.[1]
Физиологично действие[редактиране | редактиране на кода]
В организма хидрогенкарбонатите са буферни вещества, регулиращи постоянството на кръвната реакциия.[1]
Литература[редактиране | редактиране на кода]
- Кнунянц И. Л. и др. – Химическая энциклопедия, т. 3 Мед-Пол, Москва, издат. „Большая Российская Энциклопедия“, 1992, стр. 639, ISBN 5-85270-039-8, тираж 50 000.
- Ф. Н. Капуцкий, В. Ф. Тикавый – Пособие по химии для поступающих в вузы, Минск, издат. „Высшая школа“, 1979, стр. 384
- Г. П. Хомченко – Химия для поступающих в вузы, Москва, издат. „Высшая школа“, 1994, стр. 447







