Циклопропан
| Циклопропан | |
 | |
| Свойства | |
|---|---|
| Формула | C3H6 |
| Моларна маса | 42,08 g/mol |
| Външен вид | безцветен газ |
| Плътност | 1,879 g/L (0 °C) |
| Точка на топене | −128 °C |
| Точка на кипене | −33 °C |
| pKa | ~46 |
| Магнитна възприемчивост | -39,9·10−6 cm3/mol |
| Диполен момент | 0 D |
| Опасности | |
| NFPA 704 |
|
| Идентификатори | |
| CAS номер | 75-19-4 |
| PubChem | 6351 |
| ChemSpider | 6111 |
| DrugBank | DB13984 |
| KEGG | D03627 |
| MeSH | C030797 |
| ChEBI | 30365 |
| ChEMBL | 1796999 |
| SMILES | C1CC1 |
| InChI | 1S/C3H6/c1-2-3-1/h1-3H2 1/C3H6/c1-2-3-1/h1-3H2 |
| InChI ключ | LVZWSLJZHVFIQJ-UHFFFAOYSA-N LVZWSLJZHVFIQJ-UHFFFAOYAL |
| UNII | 99TB643425 |
| Gmelin | 635 |
| Данните са при стандартно състояние на материалите (25 °C, 100 kPa), освен ако не е указано друго. | |
| Циклопропан в Общомедия | |
Циклопропанът е циклоалканова молекула с молекулярна формула C3H6. Съдържа три въглеродни атома, свързани един с друг в пръстен, като всеки въглероден атом е свързан и с два водородни атома, при което се образува D3h молекулярна симетрия. Малкият размер на пръстена създава значително напрежение в молекулярната структура.
Циклопропанът действа като анастетик при вдишване. В съвременната анестезиология е заменен от други агенти. Поради високата му реактивност, смесите на циклопропан с кислород са взривоопасни.
История
[редактиране | редактиране на кода]Циклопропанът е открит през 1881 г. от Август Фройнд, който предлага правилната структура на веществото в първия си труд.[1] Той обработва 1,3-Дибромопропан с натрий, като по този начин предизвиква междумолекулна реакция на Вюрц, произвеждаща директно циклопропан.[2] Добивите от реакцията са подобрени през 1887 г. чрез употребата на цинк вместо натрий.[3] Съединението няма комерсиални приложения до 1929 г., когато са открити анестетичните му свойства.[4] Промишленото му производство започва през 1936 г.[5]
Синтез
[редактиране | редактиране на кода]Циклопропанът се произвежда чрез реакция на Вюрц, при която 1,3-Дибромопропан се циклизира посредством натрий.[1] Добивът от тази реакция може да се увеличи чрез използването на цинк като дехалогениращ агент и натриев йодид като катализатор.[6]
- BrCH2CH2CH2Br + 2 Na → (CH2)3 + 2 NaBr
Реакции
[редактиране | редактиране на кода]Поради π-характерът на C-C връзките си, циклопропанът може да реагира като алкен в определени случаи. Така например, той претърпява хидрохалогенация с неорганични киселини, при което се получават линейни алкилни халиди. Заместените циклопропани също реагират, следвайки правилото на Марковников.[7] Освен това, заместените циклопропани могат да реагират с преходни метали чрез окислително присъединяване в хода на процес, наречен C-C активация.
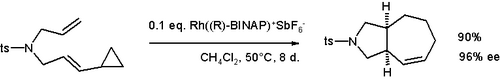
Циклопропилните групи в съседство с винилни групи подлежат на разширение на пръстените. Тази реактивност може да се използва, за да се създадат необичайни циклични съединения, като например циклобутен[8] или циклохептен.[9]
Анестетик
[редактиране | редактиране на кода]Циклопропанът е въведен за клинична употреба от американския анестезиология Ралф Уотърс, който използва затворена система с абсорбиращ въглероден диоксид, за да икономисва от скъпото по това време съединение. Циклопропанът е относително ефикасен, недразнещ и със сладка миризма.[10] Има минимална алвеоларна концентрация от 17,5% и коефициент на разпределение кръв/газ от 0,55. Това означава, че настъпването на анестезията чрез вдишване на циклопропан и кислород е бързо и не е неприятно. Все пак, при продължителна анестезия с циклопропан пациентът може да започне да изпитва внезапно покачване на кръвното налягане, което от своя страна може да доведе до аритмия.[11] Поради тази причина, както за това че е скъпо и взривоопасно,[12] съединението вече се използва само за започване на анестезия, като не е налично за клинична употреба от средата на 1980-те години.
Източници
[редактиране | редактиране на кода]- ↑ а б August Freund. Über Trimethylen // Journal für Praktische Chemie 26 (1). 1881. DOI:10.1002/prac.18820260125. с. 367 – 377.
- ↑ August Freund. Über Trimethylen // Monatshefte für Chemie 3 (1). 1882. DOI:10.1007/BF01516828. с. 625 – 635.
- ↑ G. Gustavson. Ueber eine neue Darstellungsmethode des Trimethylens // Journal für Praktische Chemie 36. 1887. DOI:10.1002/prac.18870360127. с. 300 – 305.
- ↑ A New Anesthetic: Cyclopropane : A Preliminary Report // Can Med Assoc J 21 (2). 1 август 1929. с. 173 – 5.
- ↑ Synthesis of Cyclopropane // Industrial & Engineering Chemistry 28 (10). 1936. DOI:10.1021/ie50322a013. с. 1178 – 81.
- ↑ Anesthetics, General // Ullmann's Encyclopedia of Industrial Chemistry. 2000. DOI:10.1002/14356007.a02_289.
- ↑ Advanced organic Chemistry, Reactions, mechanisms and structure 3ed. Jerry March ISBN 0-471-85472-7
- ↑ Fürstner, Alois. PtCl-Catalyzed Rearrangement of Methylenecyclopropanes // Journal of the American Chemical Society 128 (19). 2006. DOI:10.1021/ja061392y. с. 6306 – 6307.
- ↑ Wender, Paul A. и др. Asymmetric Catalysis of the [5 + 2] Cycloaddition Reaction of Vinylcyclopropanes and π-Systems // Journal of the American Chemical Society 128 (19). май 2006. DOI:10.1021/ja058590u. с. 6302 – 6303.
- ↑ Eger, Edmond I. Equipotent Alveolar Concentrations of Methoxyflurane, Halothane, Diethyl Ether, Fluroxene, Cyclopropane, Xenon and Nitrous Oxide in the Dog // Anesthesiology 26 (6). 1965. DOI:10.1097/00000542-196511000-00012. с. 771 – 777.
- ↑ JOHNSTONE, M. Cyclopropane anesthesia and ventricular arrhythmias. // British Heart Journal 12 (3). July 1950. DOI:10.1136/hrt.12.3.239. с. 239 – 44.
- ↑ MacDonald, AG. A short history of fires and explosions caused by anaesthetic agents. // British Journal of Anaesthesia 72 (6). June 1994. DOI:10.1093/bja/72.6.710. с. 710 – 22.