Аденозинтрифосфат
Тази статия се нуждае от подобрение. Необходимо е: форматиране, изчистване на машинен превод, правилно структуриране на разделите. Ако желаете да помогнете на Уикипедия, използвайте опцията редактиране в горното меню над статията, за да нанесете нужните корекции. |
| Аденозинтрифосфат | |
   | |
| Имена | |
|---|---|
| По IUPAC | [(2R,3S,4R,5R) -5-(6-аминопурин-9-ил)-3,4- дихидроксиоксолан-2-ил]метил (хидроксифосфонооксифосфорил) хидроген фосфат |
| Други | аденозин 5'-(тетрахидроген трифосфат) |
| Свойства | |
| Формула | C10H16N5O13P3 |
| Моларна маса | 507,18 g/mol |
| Плътност | 1,04 g/cm3 |
| Точка на топене | 187 °C |
| pKa | 6,5 |
| Идентификатори | |
| CAS номер | 56-65-5 |
| PubChem | 5957 |
| ChemSpider | 5742 |
| DrugBank | DB00171 |
| KEGG | C00002 |
| MeSH | D000255 |
| ChEBI | 15422 |
| ChEMBL | CHEMBL14249 |
| SMILES | O=P(O)(O)OP(=O)(O)OP(=O)(O)OC [C@H]3O[C@@H](n2cnc1c(ncnc12)N) [C@H](O)[C@@H]3O |
| InChI | 1S/C10H16N5O13P3/c11-8-5-9 (13-2-12-8)15(3-14-5)10 – 7(17)6 (16)4(26 – 10)1-25-30(21,22)28 – 31 (23,24)27 – 29(18,19)20/h2-4,6-7,10, 16-17H,1H2,(H,21,22)(H,23,24) (H2,11,12,13)(H2,18,19,20) /t4-,6-,7-,10-/m1/s1 |
| InChI ключ | ZKHQWZAMYRWXGA-KQYNXXCUSA-N |
| UNII | 8L70Q75FXE |
| Gmelin | 34857 |
| Данните са при стандартно състояние на материалите (25 °C, 100 kPa), освен ако не е указано друго. | |
| Аденозинтрифосфат в Общомедия | |
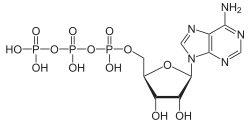
Аденозин трифосфорната киселина (също аденозинтрифосфат или АТФ) представлява химично макроергично съединение, което съдържа богати на енергия връзки. Изграден е от 3 основни съставки: азотна база аденин, рибоза и 3 остатъка от фосфорна киселина, обозначени като алфа- (α), бета- (β), и за последния гама- (γ) фосфатен остатък. В неутрален разтвор йонизираният АТФ съществува предимно като ATP4− и малка част като ATP3−.
АТФ съдържа в молекулата си 2 макроенергични връзки, които при разкъсването си освобождават енергия за нуждите на организма (между α- и β-, и β- и γ- фосфатен остатък).
Свързване на метални катиони към АТФ[редактиране | редактиране на кода]
Като полион, и притежаващ потенциално хелираща фосфатна група, АТФ свързва метални катиони с висок афинитет. Свързващата константа за Mg2+ е 9554.[1] Свързването на двувалентения катион (почти винаги магнезиев) силно повлиява взаимодействието на АТФ с различни протеини. Поради силата на ATФ-Mg2+ взаимодействието, ATФ съществува в клетките почти изцяло в комплекс с Mg2+, свързан с фосфатните кислородни центрове.[2][3]
Втори магнезиев йон е важен за АТФ свързването в киназните домени. Наличието на Mg2+ регулира киназната активност.
Химични характеристики[редактиране | редактиране на кода]
Солите на ATФ могат да бъдат изолирани като безцветни твърди (не течни) вещества. Циклите на синтез и разграждане на АТФ 2 и 1 представляват внасяне и освобождаване на енергия, съответно АТФ е стабилен във воден разтвор при pH между 6,8 и 7,4, в отсъствието на катализатори. При по-екстремни pH стойности, бързо хидролизира до АДФ и фосфат. Живите организми поддържат съотношение на АТФ към АДФ в порядъка от 1:10. В контекста на биохимичните реакции, P-O-P връзките са връзки с висок групов потенциал (макроенергични връзки).
Хидролизата на АТФ до АДФ и неорганичен фосфат освобождава 30,5 kJ/mol енталпия, с промяна в свободната енергия 3,4 kJ/mol. Енергиите, освободени при разграждането на фосфат (Pγ) или пирофосфат (PPi) от АТФ, при стандартни условия за 1 М, са:
- ATP + H2O → ADP + Pi ΔG° = −30,5 kJ/mol (−7.3 kcal/mol)
- ATP + H2O → AMP + PPi ΔG° = −32,2 kJ/mol (−7,7 kcal/mol)[4]
Тези съкратени уравнения могат да бъдат написани по-подробно (R = аденозил):
- [RO-P(O)2-O-P(O)2-O-PO3]4− + H2O → [RO-P(O)2-O-PO3]3− + [PO4]3− + 2 H+
- [RO-P(O)2-O-P(O)2-O-PO3]4− + H2O → [RO-PO3]2− + [O3P-O-PO3]4− + 2 H+
Получаване[редактиране | редактиране на кода]
АТФ може да се получи при разграждането на мазнини, белтъци (по-малко) и въглехидрати в основния метаболизъм на клетката. Основното количество АТФ се получава при окислителното фосфорилиране в митохондриите.
Синтезиране[редактиране | редактиране на кода]
АТФ се синтезира в клетката при различни метаболитни пътища като (1) гликолиза, (2) цикъл на Кребс, дихателна верига/окислително фосфорилиране и бета-окисление. Като цяло процесът на окисление на глюкозата до въглероден диоксид се, комбинацията н апът 1, 2 и 3 се нарича аеробна гликолиза, продуцираща 30 (32) М АТФ по Hinkle за всяка молекула глюкоза, или още окислително фосфорилиране.[4] В по-тесен смисъл на терминът окислително фосфорилиране означава фосфорилиране/синтез на АТФ от АДФ и Фн в присъствието на О2 в дихателните вериги на митохондриите, при пренос на редуциращи ексвиваленти Н2 от НАДН.Н и ФАДН2, субстрати на дихателната вериги и продукти на гликолиза (в тесен смисъл до пируват) и Цикъл на Кребс.
АТФ продукцията от не-фотосинтезиращите аеробни еукариоти се наблюдава основно в митохондриите, продуциращи около 90% от АТФ в клетките.[4]
За едно денонощие в човешкия организъм се получават и използват около 100 – 150 мола АТФ (за 50 – 75 кг, т.е. колкото средното женско/мъжко тегло), като една молекула се ресинтезира стотици пъти в денонощие, моментното количество е около 250 грама, времето на съществуване на една молекула АТФ е минута.
Окислително фосфорилиране[редактиране | редактиране на кода]
Всички биохимични реакции в организма се извършват с участие на ензим или ензимни комплекси и енергия, която се предоставя от макроергичните връзки на АТФ. АТФ е универсалният енергиен акумулатор в живите клетки. Част от ензимните реакции, свързани с използването на енергията на макроергичните връзки на АТФ, водят до хидролиза на фосфоанхидритната връзка, поради която ензимите, катализиращи реакцията, притежават АТФ хидролазна активност. Такива са например Na+, K+ – АТФаза, Ca++ – АТФаза на саркоплазматичния ретикулум, АТФазата на молекулата на миозина и др. АТФазна активност проявяват АТФсинтетазните комплекси на енергопреработващите биологични мембрани, АТФсинтетазния комплекс на плазматичната мембрана на някои прокариоти. В този случай хидролизата на АТФ от АТФсинтетазните комплекси, изолирани фактори F1 се разглежда като пълно или частично обръщане на реакцията на фосфорилиране на АДФ.
В мускулната клетка биохимията на процеса съкращение се осъществява най-общо по следната схема:
- АТФ + М → М – АДФ.Ф – М – АДФ.Ф + А → (А – М – АДФ.Ф) → А – М + АДФ + Ф
При наличие на АТФ:
- АТФ + М – А → А + М – АТФ
Методика за регистрация на АТФ[редактиране | редактиране на кода]
Независимо от конкретния случай, регистрацията на АТФазната реакция се свежда до определянето на концентрацията на неорганичния фосфат в определен обем разтвор. Известни са различни методи за определяне регистрацията на неорганичен фосфат, но във всички случаи се използва реакция, водеща до образуване на оцветен продукт, концентрацията на който се определя чрез измерване на екстенцията.
Пробите се подготвят, като разтворите се добавят в определен ред. След внасяне на изследвания разтвор, съдържащ Ф, пробите се инкубират в продължение на 30 мин при стайна температура, след което се измерва екстинцията при дължина на вълната 750 нанометра. Концентрацията на неорганичен фосфат се определя по екситнцията на стандартната проба, или по-добре, по предварително построена стандартна крива. Стандартната крива се построява като в пробите се внася от 0,01 до 0,1 М разтвор на (от 0,01 до 0,1 М фосфат в проба).
АТФсинтетазният комплекс на митохондриите, след разпрягане на окислителното фосфорилиране (в присъствие на динитрофенол, след разрушаване на митохондриите, изолиране на субмитохондриални частици), катализира хидролизата на АТФ. Тази активност може да бъде регистрирана в среда, съдържаща 0,2 М захароза, 10 М KCI; 1 М АТФ, 1 М MgCI, 50 M трис-HCI (pH 7,5). Ако обемът на добавките в реакционната среда е голям и надвишава 1 – 2 %, реакционната среда се приготвя по-концентрирана, така че след внасяне на добавките с известно количество вода крайната концентрация на разтвора да съответства на изчисленията.
Към 4,9 мл реакционна среда при непрекъснато разбъркване с магнитна бъркалка се прибавя 0,1 мл ензим. Едновременно с добавянето се отчита началото на реакцията със секундомер. След определен интервал от време (15 сек, 30 сек, 1 мин, 2 мин, 3 мин) от реакционната среда с помощта на автоматична пипета (тип Епендорф) се взима 0,75 мл разтвор, който се пренася в предварително приготвени пластмасови епруветки, поставени в лед, всяка от които съдържа 0,15 мл 3 М HCIO
Продукция от АМФ и АДФ[редактиране | редактиране на кода]
Продукция, аеробни условия[редактиране | редактиране на кода]
Типичната вътреклетъчна концентрация на АТФ е трудно да се определи, но докладите показват, че има различни от 1 – 10 μМ на грам тъкан в различни еукариоти. Дефосфорилирането на АТФ и рефосфорилирането на АДФ и АМФ се появяват многократно в хода на аеробния метаболизъм.
ATP може да бъде продуциран чрез редица различни клетъчни процеси; трите основни пътя в еукариотите са (1) гликолиза, (2) Цикъл на лимонена киселина / окислително фосфорилиране и (3) бета-окисление. Общият процес на окисляване на глюкозата до въглероден диоксид, комбинацията от пътища 1 и 2, известен като аеробна гликолиза, произвежда около 30 (32) еквивалента АТФ от всяка молекула глюкоза. Друг процес, в който се синтезира АТФ от АДФ и Ф, е гликолизата. Самият процес протича с участие на ензими – кинази (фосфофруктокиназа). АТФазна активност имат и ензими, които участват в процесите на окислително фосфорилиране в дихателните – електрон пренасящи вериги при хлоропласти и митохондрии. Процесът може да се изрази по следния начин: фосфорилиране на АДФ + Ф до АТФ в светлинната фаза на фотосинтезата при пренасянето на електрон от пластхинони на цитохроми. Отделената енергия се акумулира в АТФ; фосфорилиране на АДФ + Ф до АТФ в гликолитичния път на две места; 1,3 фосфоглицерат → 3 фосфоглицерат. В този процес участва ензимът глицератфософкиназа и при превръщането на фосфоенолпирувата в пируват участва ензима пируваткиназа.
Производството на АТФ от не-фотосинтезиращ аеробен еукариот се осъществява главно в митохондриите, които съставляват близо 25% от обема на типичната клетка.
С подобни фосфокинази се синтезира АТФ и при други процеси в живите организми като отделни фермантации. Емблематичен процес в биохимизма на живите аеробни еукариоти е окислителното фосфорилиране в митохондриите или по-точно върху вътрешната мембрана. Субстрати на биохимичната реакция са: НАДH.Н, ФАД.Н2 – крайни продукти от цикъла на Кребс, О2 и с участието на сложна верига от ензими. Хидролизата на АТФ се описва от уравнението: ензим АТФ + Н2О → АДФ + Ф + Н+
В зависимост от възможностите и конкретната поставена задача АТФазната активност може да бъде регистрирана чрез определяне на концентрацията на един от продуктите – АДФ, неорганичен фосфат или Н+. Методически най-лесно и може би по този начин най-често, АТФазната активност се регистрира чрез определяна нарастването на концентрацията на неорганичния фосфат в хода на реакцията.
В гликолизата глюкозата и глицеролът се метаболизират до пируват. Гликолизата генерира два еквивалента/М АТФ чрез субстратно фосфорилиране, катализирано от два ензима, (1,3-бис)фосфоглицерат киназа (ФГК) и пируват киназа. Произвеждат се също два еквивалента/М на НАДН.Н, които могат да бъдат окислени чрез електрон-транспортната верига и да генерират допълнителен АТФ от ATP синтаза. Пируватът, генериран като краен продукт на гликолиза, е субстрат на Цикъла на Кребс (Цикъла на Лимонена Киселина, Цикъл на Трикарбоксиловите Киселини).[5]
Гликолизата се разглежда като състояща се от две фази с по пет стъпки всяка. Фаза 1, „подготвителната фаза“, глюкозата се превръща в 2 d-глицералдехид -3-фосфат (Г3Ф). Един АТФ се използва в Реакция 1, а друг АТФ се използва в Реакция 3. Реакции 1 и 3 от гликолиза се наричат „Активираща фаза“ („Подготвителна фаза“). Във фаза 2 два еквивалента/М на Г3Ф се превръщат в два М пируват. В реакция 7 се произвеждат две молекули АТФ. В допълнение, реакция 10 се получават още две молекули АТФ. В реакции 7 и 10 АТФ се генерира от АДФ. В гликолизата (в тесен смисъл на терминът, до пируват) се образуват общо две молекули АТФ. Пътят на гликолизата се свързва с Цикъла на Лимонена Киселина впоследствие/ при аеробни условия, който произвежда допълнителни еквиваленти/М АТФ (20 – 10 за всяка молекула пируват по Hinkle).
Регулация[редактиране | редактиране на кода]
В гликолизата хексокиназата директно се инхибира от своя продукт, глюкозо-6-фосфат, а пируват киназата се инхибира от самия Аланин, цАМФ (глюкагон). Ключовата реакция на гликолитичния път е фосфофруктокиназата (ФФК), която алостерично се инхибира от високи концентрации на АТФ, цитрат, цАМФ (цикличен АМФ) (глюкагон) и се активира от високи концентрации на фруктозо-2,6-бисфосфат (продукт на ФФК2), АМФ, фруктозо-6-фосфат и Фн. Инхибирането на ФФК от АТФ е необичайно, тъй като АТФ също е субстрат в реакцията, катализирана от ФФК; активната форма на ензима е тетрамер, който съществува в две конформации, само една от които свързва втория субстрат фруктоза-6-фосфат (Ф6Ф). Протеинът има две свързващи места за АТФ – активният център е достъпен и при двете конформации R- и T-, но свързването на АТФ към алостеричният (инхибиторен) център стабилизира Т-конформацията, която свързва слабо Ф6Ф.[5] При ниски конценрации на АТФ гликолизата се усилва и се синтезира АТФ. Редица други малки молекули могат да компенсират индуцираното от АТФ изместване на конформацията и да реактивират отново ФФК, включително цикличен АМФ, амониеви йони, неорганичен фосфат и фруктозо-1,6- и -2,6-бифосфат.[4][5][6]
Цикъл на Кребс[редактиране | редактиране на кода]
Основна статия: Цитратен Цикъл и Окислително фосфорилиране
В митохондрионът пируватът се окислява от пируват дехидрогеназния комплекс до ацетилна група, активирана с макроергична връзка с КоА (коеннзим А), която се окислява напълно до въглероден диоксид чрез Цикъла на Лимонената Киселина (известен също като Цикъл на Кребс). Всеки Цикъл на Лимонена Киселина продуцира две молекули въглероден диоксид, една молекула АТФ (гуанозин трифосфат (ГТФ)) чрез фосфорилиране на субстратно ниво, катализирано от сукцинил-CoA синтетаза, като сукцинил-CoA се превръща в Сукцинат, три еквивалента на НАДН.Н и един еквивалент на ФАДH2. НАДН.Н и ФАДH2 се рециклират (съответно до НАД+ и ФАД), генерирайки допълнително АТФ чрез окислително фосфорилиране в дихателните вериги. Окисляването на НАДН.Н води до синтеза на 2,5 (3) еквивалента АТФ, а окисляването на един ФАДH2 до 1,5 (2) еквивалента АТФ.[7] По-голямата част от клетъчните АТФ се генерират от този процес. Въпреки че самият Цикъл на Лимонената Киселина не включва молекулен кислород, той е задължително аеробен процес, тъй като O2 се използва за окисление на НАДН.Н и ФАДH2. При липса на кислород Цикълът на Лимонената Киселина се инихибира.[8]
Генерирането на АТФ от митохондриите от цитозолния НАДН.Н разчита на малат-аспартатната совалка (и в по-малка степен на глицерол-фосфатната совалка), тъй като вътрешната митохондриална мембрана е непроницаема за НАДН.Н и НАД+. Вместо да прехвърля генерирания НАДН.Н, ензимът малат дехидрогеназа превръща оксалоацетатът в малат, който трамслокира в митохондриалния матрикс. Друга реакция, катализирана от малат дехидрогеназа, протича в обратна посока, продуцира оксалоацетат и НАДН.Н от транспортирания в митохондриите малат и митоходриалният НАД+. Трансаминазата превръща оксалоацетата в аспартат за транспортиране обратно през мембраната и в междумембранното пространство.[8]
При окислително фосфорилиране преминаването на електрони от НАДН.Н и ФАДH2 през електрон-пренасящите вериги изпомпва протони от митохондриалния матрикс в междумембранното пространство. Това изпомпване генерира протонна движеща сила, която е нетният ефект на pH градиент и градиент на електрически потенциал през вътрешната митохондриална мембрана. Потокът на протони по този потенциален градиент – тоест от интермембранното пространство към матрикса води до синтеза на АТФ от АТФ синтаза.[9] Три АТФ се произвеждат на оборот от НАДН.Н (2,5 по Hinkle) и 2 АТФ от ФАДН2 (1,5 по Hinkle).
Въпреки че консумацията на кислород изглежда фундаментална за поддържането на протонната движеща сила, в случай на недостиг на кислород (хипоксия), вътреклетъчната ацидоза (медиирана от повишени гликолитични нива и ATP хидролиза) допринася за потенциала на митохондриалната мембрана и директно задвижва синтеза на АТФ.[10]
Повечето от АТФ, синтезирана в митохондриите, ще се използва за клетъчни процеси в цитозола; затова той трябва да бъде изнесен от мястото на синтез в митохондриалния матрикс. АТФ движението към цитоплазмата се благоприятства от електрохимичния потенциал на мембраната, тъй като цитозолът има относително положителен заряд в сравнение с относително отрицателния матрикс. За всеки транспортиран АТФ се изразходва 1 H+. Следователно, за продукцията и транспорта на един АТФ се изразходват 4H+. Вътрешната мембрана съдържа антипортер, АДФ/ АТФ транслоказа, който е интегрален мембранен протеин, използван за обмен на ново синтезиран АТФ в матрикса за АДФ в междумембранното пространство.[11] Този транслоказа се задвижва от мембранния потенциал, тъй като води до движение на около 4 отрицателни заряда вън от митохондриалната мембрана в замяна на 3 отрицателни заряда, преместени навътре. Необходимо е обаче също така да се транспортира фосфат в митохондриона; фосфатният транспортер придвижва протон с всеки фосфат, частично разсейващ протонния градиент. След завършване на гликолизата, цикъла на лимонена киселина, електронната транспортна верига (дихателната верига) и окислителното фосфорилиране се получават приблизително 30 (32) –36 (38) М ATP за молекула глюкоза.
Регулация[редактиране | редактиране на кода]
Цикълът на лимонената киселина се регулира главно от наличието на ключови субстрати, по-специално съотношението на НАД+ към НАДН.Н и концентрациите на калций, неорганичен фосфат, АТФ, АДФ и АМФ. Цитрат – йонът, който дава името си на цикъла – е инхибитор на обратната връзка на цитрат синтазата (АТФ и дълговерижни мастни киселини) и също така инхибира ФФК, осигурявайки пряка връзка между регулирането на цикъла на лимонената киселина и гликолизата.[5]
Бета-окисление[редактиране | редактиране на кода]
В присъствието на въздух и различни кофактори и ензими, мастните киселини се превръщат в ацетил-КоА. Пътят се нарича бета-окисление. Всеки цикъл на бета-окисляване съкращава веригата на мастните киселини с два въглеродни атома и продуцира по един еквивалент ацетил-КоA, НАДH.Н и ФАДH2 на всеки цикъл. Ацетил-CoA се метаболизира от цикъла на лимонената киселина за генериране на АТФ, докато НАДН.Н и ФАДH2 се използват чрез окислително фосфорилиране за генериране на АТФ. Десетки АТФ еквиваленти се генерират от бета-окислението на една дълга ацилова верига, в зависмост о т дължината на веригата и броят на циклите.[12]
Регулация[редактиране | редактиране на кода]
При окислителното фосфорилиране ключовата контролна точка е реакцията, катализирана от цитохром с оксидаза, която се регулира от наличието на нейния субстрат – редуцираната форма на цитохром c. Количеството на наличния редуциран цитохром с е пряко свързано с количествата на други субстрати.
По този начин, високото съотношение на [НАДН.Н] към [НАД+] или високото съотношение [АДФ] [Фн] към [АТФ] предполага голямо количество редуцирана цитохром с и високо ниво на активност на цитохром с оксидаза.[5] Допълнително ниво на регулиране се въвежда от нивата на транспорт на АТФ и НАДН.Н между митохондриалният матрикс и цитоплазмата.[5]
Кетоза[редактиране | редактиране на кода]
Основна статия: Кетонови тела
Кетоновите тела могат да се използват като гориво, като се получават 20 (24) АТФ Цилъл на Кребс и 2,5 (3) АТФ молекули 3ХБДХ на ацетоацетатна молекула, когато се окисляват в митохондриите. Кетоновите тела се транспортират от черния дроб до други тъкани, където ацетоацетатът и бета-хидроксибутиратът могат да бъдат разградени до ацетил-КоА, за да се получат редуциращи еквиваленти (НАДН.Н и ФАДH2) чрез Цикъла на Лимонената Киселина. Кетоновите тела не могат да се използват като гориво от черния дроб, тъй като в черния дроб липсва ензим β-кетоацил-КоА трансфераза, наричан още тиофораза. Ацетоацетатът в ниски концентрации се приема от черния дроб и се подлага на детоксикация по метилглиоксалния път, който завършва с лактат. Ацетоацетатът във високи концентрации се абсорбира от клетки, различни от тези в черния дроб и навлиза по различен път чрез 1,2-пропандиол. Въпреки че пътят следва различна серия от реакции, изискващи ATP, 1,2-пропандиол може да бъде превърнат в пируват.[13]
Продукция, анаеробни условия[редактиране | редактиране на кода]
Ферментацията е метаболизм на органичните съединения при липса на въздух. Тя включва фосфорилиране на субстратно ниво при липса на респираторна електроно-транспортна верига. Уравнението за окисляване на глюкозата до млечна киселина е:
- C6H12O6 → 2 CH3CH(OH)COOH + 2 ATP
Анаеробното дишане е дишане при липса на O2. Прокариотите могат да използват различни акцептори на електрони. Те включват нитрати, сулфати и въглероден диоксид.
АТФ заместване с нуклеосид дифосфат кинази[редактиране | редактиране на кода]
АТФ може да се синтезира и чрез няколко така наречени реакции на „попълване“, катализирани от ензимните семейства нуклеозид дифосфат кинази (NDKs), които използват други нуклеозид трифосфати като високоенергийни фосфатни донори и семейството на АТФ: гуанидо-фосфотрансфераза.
АТФ продукция по време на фотосинтеза[редактиране | редактиране на кода]
В растенията ATP се синтезира в тилакоидната мембрана на хлоропласта. Процесът се нарича фотофосфорилиране. „Машината“ е подобна на тази в митохондриите, с изключение на това, че светлинната енергия се използва за изпомпване на протони през мембрана, за да произведе протонно-движеща сила.[14] АТФ синтазът след това се получава точно както при окислително фосфорилиране. Някои от АТФ, произведени в хлоропластите, се консумират в Цикъла на Калвин, който произвежда триозни захари.
АТФ рециклиране[редактиране | редактиране на кода]
Общото количество АТФ в човешкото тяло е около 0,2 мола. По-голямата част от АТФ се рециклира от АДФ чрез гореспоменатите процеси. По този начин, във всеки един момент, общото количество АТФ + АДФ остава доста постоянно.
Енергията, използвана от човешките клетки, изисква хидролизата на 100 до 150 мола АТФ дневно, което е около 50 до 75 кг. Обикновено човек използва количество равно на телесното си тегло на АТФ през деня. Всеки еквивалент на АТФ се рециклира 500 – 750 пъти за един ден (100 / 0,2 = 500).[citation needed]
Пример за гънката на Росман, структурен домен на декарбоксилазен ензим от бактерията Staphylococcus epidermidis (PDB: 1G5Q) със свързан кофактор флавин мононуклеотид.
Биохимична функция[редактиране | редактиране на кода]
Интрацелуларен сигнал[редактиране | редактиране на кода]
АТФ участва в пренасянето на сигнала, като служи като субстрат за кинази, ензими, които пренасят фосфатни групи. Киназите са най-често срещаните ATP-свързващи протеини. Те споделят малък брой общи гънки.[15] Фосфорилирането на протеин от киназа може да активира каскада като митоген активируемата протеин киназна каскада.[16]
АТФ е също субстрат на аденилат циклаза, най-често в G протеин-свързан рецепторен сигнален трансдукционен път и се трансформира във вторичен посредник, цикличен АМФ, който участва в задействане на калциеви сигнали чрез освобождаването на калций от вътреклетъчните складове.[17] Тази форма на сигнална трансдукция е особено важна за мозъчната функция, въпреки че участва в регулирането на множество други клетъчни процеси.[18]
ДНК и РНК синтез[редактиране | редактиране на кода]
АТФ е един от четирите „мономера“, необходими при синтезът на РНК. Процесът се стимулира от РНК полимерази.[19] Подобен процес протича при образуването на ДНК, с изключение на това, че ATP първо се превръща в дезоксирибонуклеотид дАТФ. Подобно на много реакции на кондензация в природата, ДНК репликация и ДНК транскрипция процесите също консумират АТФ.
Амино-киселини – активация в протеиновия синтез[редактиране | редактиране на кода]
Основна статия: Активиране на аминокиселина
Аминоацил-тРНК синтетаза ензимите консумират АТФ в свързването на аминокиселините с тРНК, образувайки аминоацил-тРНК комплекси. Аминоацил трансферазата свързва АМФ-аминокиселината с тРНК. Реакцията на свързване протича в два етапа:
aa + ATP ⟶ aa-AMP + PPi
aa-AMP + tRNA ⟶ aa-tRNA + AMP
Аминокиселината е свързана с предпоследния нуклеотид в 3'-края на тРНК (А в последователността CCA) чрез естерна връзка (преобръщане в илюстрация).
АТФ свързващ касетен транспортер[редактиране | редактиране на кода]
Транспортирането на вещества от клетка срещу концентрационният градиент е често свързано с АТФ хидролиза. Транспортът се медиира от АТФ свързващи касетни транспортери. Човешкият геном кодира 48 ABC преносители, които се използват за експорт на лекарства, липиди и други съединения.[20]
Екстрацелуларен сигнал ли невротрансмисия[редактиране | редактиране на кода]
Клетките отделят АТФ за комуникация с други клетки в процес, наречен пуринергична сигнализация. АТФ служи като невротрансмитер в много части на нервната система, модулира цилиарното биене, влияе върху съдовото снабдяване с кислород и др. АТФ се секретира директно през клетъчната мембрана протеини – канали[20][21] или се изпомпва във везикули,[22] които след това се сливат с мембраната. Клетките детектират АТФ, използвайки пуринергичните рецепторни протеини P2X и P2Y.
Протеин разтворимост[редактиране | редактиране на кода]
Беше предложено че ATP действа като биологичен хидротроп[23] и е доказано, че влияе на разтворимостта в протеома.[24]
АТФ аналози[редактиране | редактиране на кода]
Биохимичните лаборатории често използват In Vitro изследвания за изследване на АТФ-зависими молекулуни процеси. АТФ аналозите се използватсъщо в Х-рентгеновата кристалография за определяне на протеинова структура в комплекс с АТФ, често заедно с други субстрати.
Ензимните инхибитори на АТФ-зависимите ензими като кинази са необходими за изследване на местата на свързване и състояния на преход, участващи в АТФ-зависими реакции.
Повечето полезни ATP аналози не могат да бъдат хидролизирани, както би бил ATP; вместо това те улавят ензима в структурата, тясно свързана със свързването на АТФ. Аденозин 5 '- (у-тиотрифосфат) е изключително често срещан АТФ аналог, при който един от гама-фосфатните оксигени е заменен от серен атом; този анион се хидролизира с драстично по-ниска скорост от самия АТФ и функционира като инхибитор на АТФ-зависимите процеси. При кристалографските проучвания преходните състояния на хидролизата се моделират от свързания ванадатен йон.
Обосновано е предпазливостта при интерпретирането на резултатите от експериментите, използващи АТФ аналози, поради това че някои ензими могат да ги хидролизират при значителни скорости при висока концентрация.[25]
История[редактиране | редактиране на кода]
ATP е открит през 1929 г. от Карл Лохман[26] и Джендрасик[27] и независимо от Сайръс Фиске и Йелапрагадада Суба Рао от Медицинското училище в Харвард,[28] двата екипа се състезават един срещу друг, за да намерят тест за фосфор.
Фриц Алберт Липман през 1941 г. беше предложен да бъде посредник между енергодобивните и енергоемките реакции в клетките.[29]
За първи път е синтезиран в лабораторията от Александър Тод през 1948 година.[30]
Нобеловата награда за химия за 1997 г. беше разделена, едната половина съвместно с Пол Д. Бойер и Джон Е. Уокър, „за тяхното изясняване на ензимния механизъм, стоящ в основата на синтеза на аденозин трифосфат (АТФ)“, а другата половина на Йенс С. Скуу " за първото откриване на ензим, транспортиращ йони, Na +, K + -ATPase."[31]
Виж също[редактиране | редактиране на кода]
- Аденозин дифосфат (АДФ)
- Аденозин монофосфат (АМФ)
- Аденозин-тетрафосфат
- Аденозин метилен трифосфат
- АТФази
- АТФ тест
- АТФ хидролиза
- Цикъл на Кребс
- Креатин
- Цикличен аденозин монофосфат (цАМФ)
- Нуклеотид обменящ фактор
- Фосфаген
- Фотофосфорилиране
Източници[редактиране | редактиране на кода]
- ↑ . Anal. Biochem. 1991: 193 (1): 16 – 19. doi:10.1016/0003-2697(91)90036-S. PMID 1645933.
- ↑ . Biochem. J. 1976: 159 (1): 1 – 5. doi:10.1042/bj1590001.
- ↑ . J. Mol. Cell. Cardiol. 1986: 18 (10): 1003 – 1013. doi:10.1016/S0022-2828(86)80289-9.
- ↑ а б в г Rodwell VW, Bender DA, Botham KM, Weil PA. Harper's Illustrated Biochemistry, 31st Edition.
- ↑ а б в г д е . Biochemistry. 1 (3rd ed.). Hoboken, NJ: Wiley.2004: ISBN 978-0-471-19350-0.
- ↑ Косекова Г, Митев В, Алексеев А, Медицински Университет – София, 2016. Лекции по медицинска Биохимия.
- ↑ . Biochem. Soc. Trans. 2003: 31 (6): 1095 – 1105. doi:10.1042/BST0311095. PMID 14641005.
- ↑ а б . Molecular Cell Biology (5th ed.). New York, NY: W. H. Freeman. I2004: SBN 978-0-7167-4366-8.
- ↑ . Nature. 1994: 370 (6491): 621 – 628.
- ↑ . Front Physiol. (January 2019): 9, 1914.
- ↑ . Physiology. 2006: 21 (4): 242 – 249.
- ↑ . Physiol. Behav. 2005: 85 (1): 25 – 35. doi:10.1016/j.physbeh.2005.04.014.
- ↑ . 2013-03-15. Archived (PDF) from the original on 2015-09-24. Посетен на 1 февруари 2019 г.
- ↑ . Cell. 2002: 110 (3): 273 – 276. doi:10.1016/S0092-8674(02)00870-X. PMID 12176312.
- ↑ . PLoS Comput. Biol. 2005: 1 (5): e49. doi:10.1371/journal.pcbi.0010049. PMC 1261164. PMID 16244704.
- ↑ . Arch. Biochem. Biophys. 2006: 452 (1): 55 – 68. doi:10.1016/j.abb.2006.05.001. PMID 16806044.
- ↑ . J. Mol. Biol. 2006: 362 (4): 623 – 639. doi:10.1016/j.jmb.2006.07.045. PMC 3662476. PMID 16934836.
- ↑ . Annu. Rev. Pharmacol. Toxicol. 2001: 41: 145 – 174. doi:10.1146/annurev.pharmtox.41.1.145. PMID 11264454.
- ↑ . J. Bacteriol. 1995: 177 (22): 6321 – 6329. doi:10.1128/jb.177.22.6321-6329.1995. PMC 177480. PMID 7592405.
- ↑ а б . Science Signaling. 2018: 11 (529): eaao1815. doi:10.1126/scisignal.aao1815. ISSN 1945 – 0877. PMC 5966022. PMID 29739879.
- ↑ . Philosophical Transactions of the Royal Society B: Biological Sciences. 2015: 370 (1672): 20140191. doi:10.1098/rstb.2014.0191. ISSN 0962 – 8436. PMC 4455760. PMID 26009770.
- ↑ . Cerebral Cortex. 2012: 22 (5): 1203 – 1214. doi:10.1093/cercor/bhr203. ISSN 1460 – 2199. PMID 21810784.
- ↑ . Science. 2017-05-19: 356 (6339): 753 – 756. doi:10.1126/science.aaf6846. ISSN 0036 – 8075. PMID 28522535.
- ↑ . Nature Communications. 2019-03-11: 10 (1): 1155. doi:10.1038/s41467-019-09107-y. ISSN 2041 – 1723. PMC 6411743. PMID 30858367.
- ↑ . Biochemistry. 1995: 34 (49): 16039 – 16045. doi:10.1021/bi00049a018. PMID 8519760.
- ↑ . Naturwissenschaften (in German). August 1929: 17 (31): 624 – 625. doi:10.1007/BF01506215.
- ↑ . Journal of Biological Chemistry. 2002: 277 (32): e21. Archived from the original on 2017-08-08. Посетен на 24 октомври 2017 г.
- ↑ . J. Hist. Biol. March 1991: 24 (1): 145 – 154. doi:10.1007/BF00130477.
- ↑ . Adv. Enzymol. 1941: 1: 99 – 162. ISSN 0196 – 7398.
- ↑ . The Nobel Prize in Chemistry 1997. Nobel Foundation. Archived from the original on 2010-01-23. Посетен на 26 май 2010 г.
- ↑ . www.nobelprize.org. Archived from the original on 24 October 2017. Посетен на 21 януари 2018 г.
Външни препратки[редактиране | редактиране на кода]
- ((en)) АТФ и биологичната енергия Архив на оригинала от 2007-12-01 в Wayback Machine.
| Тази страница частично или изцяло представлява превод на страницата Adenosine triphosphate в Уикипедия на английски. Оригиналният текст, както и този превод, са защитени от Лиценза „Криейтив Комънс – Признание – Споделяне на споделеното“, а за съдържание, създадено преди юни 2009 година – от Лиценза за свободна документация на ГНУ. Прегледайте историята на редакциите на оригиналната страница, както и на преводната страница, за да видите списъка на съавторите.
ВАЖНО: Този шаблон се отнася единствено до авторските права върху съдържанието на статията. Добавянето му не отменя изискването да се посочват конкретни източници на твърденията, които да бъдат благонадеждни. |
| ||||||||||||||||||||||||||||||
