Β-окисление
Бета-окислението е процес, при който мастните киселини под формата на ацил-КоА, се разграждат в митохондиите и/или в пероксизомите до молекули ацетил-КоА, който се включва по-нататък в цикъла на Кребс.
Бета-окислението на мастните киселини включва три етапа:
- Активиране на мастните киселини в цитозола
- Транспортирането им в митохондиите (карнитинова совалка)
- Същинско бета-окисление в митохондриалния матрикс
Мастните киселини, получени в резултат на липолиза – разграждане на триацилглицериди (ТАГ) от мастните депа, се транспортират в кръвта като свободни мастни киселини (СМК). Свободни мастни киселини (FFAs) – също така се наричат неестерифицирани (UFA) или неестерифицирани (NEFA) мастни киселини – са мастни киселини, които са в нестерифицирано състояние. В плазмата, дълго-верижните СМК се свързват с албумин, а в клетката те се свързват с протеин, свързващ мастните киселини, така че всъщност те никога не са „свободни“. По-късо верижни мастни киселини са по-водо-разтворими и съществуват като нейонизирани киселини или като на мастно киселинен анийон.
Мастните киселини се катаболизират в повечето тъкани от човешкото тяло. Все пак мозъка не ги усвоява (не могат да преминат кръвно-мозъчната бариера), а еритроцитите (не притежават митохондрии) и медулата на надбъбречната жлеза не са способни да ги окислят.
Активиране на мастните киселини
[редактиране | редактиране на кода]Мастните киселини могат да преминат през клетъчната мембрана, поради своята хидрофобност. Попаднали в цитозола, те се активират под действието на ензима ацил-КоА синтетаза (тиокиназа). Първо мастната киселина се свързва с АТФ, като се отделя фосфат и се получава ациладенилат, който реагира с коензим А и се получава ацил-КоА и се отделя АМФ. Отделеният пирофосфат (ФФн) се хидролизира от неорганична пирофосфатаза със загубата на допълнителен високоенергитична връзка, осигуряваща цялостната реакция. Ацил-КоA синтетазите се намират на мембраната на ендоплазмата ретикулум, пероксизоми и върху външната мембрана на митохондриите.
Дълговерижните мастни киселини преминават през вътрешната митохондриална мембрана чрез карнитиновата совалка
[редактиране | редактиране на кода]Карнитин (β-хидрокси-у-триметиламониев бутират), (CH3) 3N + —CH2 —CH (OH) —CH2 – COO− е широко разпространен и в особено количество в мускули. Дълговерижният ацил-КоA (или СМК) не може да проникне през вътрешна мембрана на митохондриите. Активирания ацил-КоА се свързва с карнитин и се получава ацилкарнитин, който се прехвърля през вътрешната митохондиална мембрана с помощта на натриев глутамат.
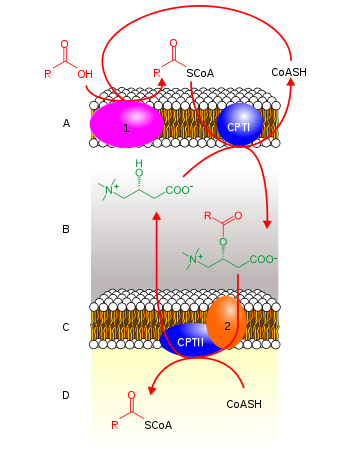
1. В присъствието на карнитин обаче, карнитин палмитоилтрансфераза-I, разположена във външната митохондриална мембрана, прехвърля ациловият остатък с дълга верига от КоA на карнитин, свързано с образуване на ацилкарнитин и отделянето на КоA.
2. Ацилкарнитинът е способен да проникват във вътрешната мембрана и получи достъп до ензимите на β-окислинието чрез вътрешно мембранен обменен транспортер – карнитин-ацилкарнитин транслоказа, разположен във вътрешната митохондриална мембрана. Транспортерът свързва ацилкарнитина и го транспортира през мембраната в замяна на карнитин.
3. Ациловата група впоследствие се прехвърля върху КоA, така че ацил-КоА се реформира в митохондриалния матрикс и карнитинът се освобождава за преносът от 2-рия ензим на совалката. Тази реакция се катализира от карнитин палмитоилтрансфераза-II, която се намира от вътрешната страна на вътрешната митохондриална мембрана.
Същинско окисление
[редактиране | редактиране на кода]На всеки цикъл на пътя за окисление на мастни киселини, два въглеродни атома (С2), под формата на ацетил-КоА сеотделят от ацил-КоA молекулите, започвайки от карбоксилния край ( -СОО- – край). Веригата се прекъсва между α (2) – и β (3) -въглеродни атоми – следователно процесът се нарича β-окисляване. Образуваните две въглеродни единици са на ацетил-СоА; по този начин, палмитоил (C16) -КоA образува осем молекули ацетил-CoA молекули. Ако n- е браоят на С-атоми на дадена мастна киселина, то броят образувани мол. ацетил-КоА, ще бъде Cn/2.
Попаднал в митохондриите ацил-КоА се скъсява с два въглеродни атома (под формата на ацетил-КоА), при всеки цикъл на бета-окислението, извършващо се в четири стъпки:
| Описание | Схема | Ензим | Продукт |
| Дехидрогениране през ФАД: Първата стъпка е окислението на мастната киселина от ензима ацил-КоА-дехидрогеназа. Той катализира образуването на двойна връзка между C-2 и C-3. |  |
Ацил-КоА дехидрогеназа | транс-Δ2-еноил-КоA |
| Хидратиране: При следващата стъпка, към двойната връзка между C-2 и C-3 се включва молекула вода. Реакцията е стероспецифична и встъпват само L изомерите. |  |
Еноил-КоА хидратаза | L-β-хидроксиацил-CoA |
| Окисление от НАД+: Третата стъпка е окислението на L-β-хидроксиацил-КоА от НАД+. При това хидроксилната група се превръща в кето-група. |  |
L-β-хидроксиацил-КоA дехидрогеназа | β-кетоацил-КоA |
| Тиолиза: Последната стъпка е откъсването на β-кетоацил-КоA от тиоловата група, чрез включване на друга молекула коензим А между C-2 и C-3. |  |
β-кетотиолаза | Ацетил-КоА (Сn-2) и ацил-КоА по-къс от изходния с два въглеродни атома |
| Образуваната по-къса верига на ацил-КоА, образуван в тиолазната реакцията, се въвежда отново в окислителния път при реакция 1. |
Процесът продължава, докато цялата молекула се разгради до ацетил-КоА (С2) единици. При последния цикъл се получават две молекули ацетил-КоА. Равносметката от всеки цикъл е по-къса с два атома въглеродна верига и по една молекула ФАД2, НАДН и ацетил-КоА. Например, след седем цикъла, С16 мастната киселина, палмитат, би се превърнал в осем молекули ацетил-КоА. (Броят на циклите се изчислява по формолата (Cn/2 – 1), поради това че в последния цикъл се образуват 2 мол. ацетил-KoA Тъй като ацетил-КоА може да се окислява до CO2 и вода чрез Цикъла на Лимонената Киселина (който също се намира в митохондриалния матрикс) се постига пълно окисляване на мастните киселини.
Мастните киселини с нечетен брой въглеродни атоми
[редактиране | редактиране на кода]Мастните киселини с нечетен брой въглеродни атоми се окисляват от пътя на β-окислението, описан по-горе, като в последния цикъл се получава ацетил-КоA и остатък, изграден от три въглеродни атома (С3 – пропионил-КоА). Това съединение се превръща в сукцинил-КоА, метаболит от Цикъла на Лимонената Киселина. Следователно, пропиониловият остатък от мастни киселини с нечетен брой въглеродни атоми е единствената част на мастната киселина, която е глюкогенна (от нея може да се синтезира глюкоза в глюконеогенезата, поради това че не се разгражда напълно в ЦТК, подобно на ацетил-КоА).
Енергиен добив
[редактиране | редактиране на кода]Всеки цикъл на β-окисляване генерира една молекула ФАДH2 и една от НАДH. Разграждането на 1 мол от С16 мастната киселина, палмитат, най-често синтезираната мастна киселина в нашия организъм и съответно най-често разгражданата, изисква седем цикъла, в които се получават 8 мол. ацетил-CoA. Окисляване на редуциращите еквиваленти през дихателната верига води до синтеза на 28 мол АТФ (по Hinkle) и окисляване на ацетил-CoA през Цикълът на Lимонената Kиселина продуцира 80 мол АТФ. Следователно разграждането на 1 мол палмитат дава общо бруто 108 мол ATP. Въпреки това, в началото са използвани две високоенергийни макроергични връзки за активиране на мастната киселина (въпреки само една мил. АТФ), като по този начин има нетна печалба от 106 мол ATP на мол използван палмитат, или 106 × 30.5 * = 3233 kJ. Това представлява 33% от свободната енергия при изгаряне на палмитинова киселина (и опредля кпд-то (коефициент на полезно действие на организмът ни, енергия съсържаща се в окисляваното съединение/енергие съхранени в макроергичните връзки на синтезирания АТФ).
Или обща формула:
Бр. синтезирани мол АТФ = [Cn/2x 4 (5) + Cn/2 – 1 x 10 (12)] -2
| Източник | ATФ | Общо |
| 1 ФАДH2 | x 1.5 ATФ | = 1.5 ATФ |
| 1 НАДН | x 2.5 ATФ | = 2.5 ATФ |
| 1 ацетил-КоА | x 10 ATP | = 10 ATФ |
| Общо за 1 цикъл | = 14 АТФ |
Генериране на АТФ от пълното окисление на С16 мастни киселини
| Стъпка | Продукт | Количество синтезиран продукт (mol)/mol палмитат | Синтезиран АТФ (mol)/mol продукт | Общо синтезиран АТФ (mol)/mol палмитат | АТФ използван (mol)/mol палмитат |
| Активация | - | 2 | |||
| β-окисление | ФАДН2 | 7 | 1.5 | 10.5 | - |
| β-окисление | НАДН | 7 | 2.5 | 17.5 | - |
| Цикъл на Кребс | Ацетил-КоА | 8 | 10 | 80 | - |
| Общо АТФ (mol)/mol палмитат | 108 | ||||
| Общ АТФ използван (mol)/mol палмитат | 2 | ||||
| Крайна равносметка бр. АТФ mol | 106 | ||||
Таблицата показва как окислението на 1 mol C16 мастна киселина, генерира 106 mol АТФ (108 общо синтезирани -2 използвани за активирането на мастната киселина (2 макроергични връзки в състава на 1 молекула АТФ)).
Пероксизомите окисляват много-дълго верижните мастни киселини
[редактиране | редактиране на кода]Модифицирана форма на β-окисление се намира в пероксизомите и води до разграждане на много-дълго верижни мастни киселини (напр. C20, C22) с образуването на ацетил-КоA и H2O2, който се разгражда чрез ензимът каталаза. Тази система не е свързана директно с фосфорилирането и генериране на АТФ, а също така не атакува мастните киселини с по-къса верига; на β-окислителната последователност завършва до образуването на октаноил-CoA (С18). Октаноилови и ацетилови групи се окисляват допълнително в митохондриите. Пероксизомните ензими са индуциран от диети с високо съдържание на мазнини и в някои видове от хиполипидемични лекарства, като клофибрат.
Друга роля на пероксизомалното β-окисление е скъсяването на страничната верига на холестеролът при образуването на жлъчни киселини.
Пероксизомите участват също в синтеза на етерни глицеролипиди, холестерол и долихол.
Окислението на ненаситени мастни киселини възниква чрез модифициран път на β-окислението
[редактиране | редактиране на кода]β-окислението на ненаситените мастни киселини представлява проблем, тъй като местоположението на цис-връзката може да предотврати образуването на транс-Δ2 връзка. Тези ситуации се обработват от допълнителни два ензима.
β-окислението протича по описания начин, докато двойната връзка не застане на 3-то или 4-то място и субстрата не е подходящ за действието на ацил-КоА дехидрогеназата или еноил-КоА хидратазата:
- Ако ацил-КоА съдържа cis-Δ3 двойна връзка (на трето място), тогава cis-Δ3-еноил-КоА изомераза конвертива връзката като транс-Δ2 и се получава нормалният за хидратазата субстрат.
- Ако ацил-КоА има цис-Δ4 двойна връзка, при дехидрогенирането се получава 2,4-диеноил, който не е субстрат за еноил-КоА хидратазата. Тук се включва ензима 2,4 диеноил-КоА редуктаза който редуцира субстрата с помощта на НАДФH, в транс-Δ3-еноил-КоА. След това се конвертира до подходящ субстрат от 3,2-еноил-КоА изомереза.
На β-окисление могат да се подлагат само природните цис-киселини. Транс-киселините не са подходящи субстрати за ензимите и не могат да бъдат усвоени, а се натрупват в мастните депа.
Заболявания
[редактиране | редактиране на кода]Карнитинов дефицит може да настъпи в новородени и особено в преждевременно родени бебета, поради неадекватен синтез или бъбречна загуба. Загуби могат да настъпят също при хемодиализа. Това предполага, че може да съществува витамин-подобни нужди от доставянето на карнитин с храната в някои индивиди. Симптомите на дифицит включват хипогликемия, последица наувредено мастно киселино окисление, и липидни акумолиране с мускулна слабост. Лечението е приемът на карнитин като хранителна добавка.
Наследствен КПТ-I дефицит засяга само черният дроб, резултиращ в намалено мастнокиселинно окисление и кетогенеза, с хипогликемия. CPT-II дефицитът засяга основно скелетната мускулатура и когато е тежък, черният дроб. Сулфонилурейните лекарства (глибурид, (глибенкламид и толбутамид) използвани при лечение на тип II диабет, редуцират окислението на мастни киселини и, следователно, хипергликемията чрез инхибране на КПТ-I.
Наследствени дефекти в ензимите на β-окислението и кетогенезата водят също до некетична хипогликемия, кома и мастен черен дроб. Дефекти са установени в дълго- и късо-верижните 3-хидроксиацил-КоА дехидрогеназа (дефицит на дълго-верижния ензим може да е причина за остър мастен черен дроб на бременността). 3-кетоацил-КоА тиолаза и ХМГ-КоА лиаза дефицит засяга също разграждането на левцин, кетогенна аминокиселина.
Ямайска болест с повръщане се причинява от яденето на незряли плодове на дървото аки (Blighia sapida), съдържащи токсинът хипоглицин. Той инактивира средно- и късо-верижни ацил-КоА дехидрогеназа, инхибирайки β-окислението и причиняващо хипогликемия. Дикарбоксилната ацидурия се характеризира с екскреция на С6-С10 ω-дикарбоксилна киселина и чрез некетонова хипогликемия, и се причинява от липсата на митохондриална средно-верижни ацил-КоА дехидрогеназа. Заболяването на Refsum е рядко неврологично заболяване причинено от метаболитен дефектрезултиращ в акумолирането на фитанова киселина, намираща се в хранителни продукти и сланината и месото на преживни. Фитановата киселина се смята че притежава патологични ефекти върху мембранната функция, протеиново прениларане, и генна експресия.
Zellweger (цереброхепаторенален) синдром се наблюдава в индивиди с рядка налседсвена липса пероксизоми във всички тъкани. Те акумолират С26-С38 оилиенични киселини в мозъчни тъкани и също проявяват генерализирана загуба на пероксизмални функции. Заболяването причинява тежки неврологични симптоми, и повечето пациенти умират в първата година от живота си.[1]
Източници
[редактиране | редактиране на кода]- ↑ Rodwell VW, Bender DA, Botham KM, Kennelly PJ, Weil PA. Harpers’ Illustrated Biochemistry, 31 st Edition.
