Масспектрометрия
Масспектрометрията (мас-спектроскопия, мас-спектрография, мас-спектрален анализ) е метод за анализ на веществото чрез определяне на отношението на масата към заряда (качествен анализ) и количеството заредени частици (количествен анализ), образуващи се при въздействие върху веществото с цел йонизация. Първоначално детектирането на заредените частици е било с помощта на фотоплаки (мас-спектроскопия и мас-спектрография), а с преминаването към електрическо измерване на йонния ток методът получава окончанието „-метрия“.
Първият инструмент на този принцип е изобретен от Джоузеф Джон Томсън. С негова помощ той открива електрона, за което получава Нобелова награда за физика през 1906 г. Апаратът, използван от Томсън за първия опит за разделяне по маси, е бил тип спектрометър, регистриращ сигналите върху флуоресциращ екран. Dempster конструира усъвършенстван инструмент с отклоняващо магнитно поле под ъгъл 180°. За да се регистрират различните маси, той е бил оборудван с фотографска плака – т.нар. масспектрограф (mass spectrograph) – също така се е използвало променливо магнитно поле за регистриране на различните маси чрез последователното им фокусиране върху електрически детектор. По-късно терминът масспектрометър бил използван за по-късните модели инструменти със сканиращо магнитно поле [1].
Най-често се използва за определяне на състава на проба, чрез генериране на масспектър, отговарящ на масите на компонентите в пробата.
Масспектър[редактиране | редактиране на кода]
Масспектърът е двумерно представяне на интензивността на сигнала (ордината) към m/z (абсциса). Интензивността на пика, както се нарича обикновено сигналът, е в пряка зависимост от количеството йони от съответното m/z, които са образувани от пробата в йонния източник. Отношението маса/заряд (чете се „m върху z“) е безразмерна величина, защото по дефиниция се определя от масовото число m на йона и броя елементарни заряди z. Зарядът обикновено, но не задължително, е единица. В повечето случаи се работи с йони със заряд единица (z = 1), в този случай зависимостта m/z се преобразува в m.
Често, но не винаги, пикът с най-голяма стойност на m/z е резултат от детектирането на заредена молекула (или атом) на пробата или т. нар. молекулен йон М+●. Пикът на молекулния йон обикновено е съпътстван от няколко пика с по-ниско m/z, дължащи се на фрагментирането на молекулния йон на получени фрагментни йони.
Най-интензивният пик в масспектъра се нарича базов пик. В повечето случаи данните за интензитета в масспектрите се представят като нормализирани спрямо базовия пик, чийто интензитет се приема за 100%. Това улеснява сравняването на масспектрите.
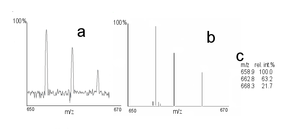
Най-често срещаният начин за представяне на масспектри е чрез хистограма (означена с b).
Интензитетът на пика се определя от измерването на неговата височина или – за по-голяма точност – на неговата площ. Позицията или m/z отношението на сигнала се определя от неговия центроид. Шумът под определено ниво, зададено от оператора, се изключва от масспектъра при представянето му като хистограма. В случаите, когато е от значение щирочината или формата на пика, т.е. при измервания с голяма разделителна способност или при високомолекулни проби, спектърът се представя профилно (означено с a), както обикновено се извлича първоначално от масспектрометъра. Табличното представяне (означено с c) се използва, когато е нужно по-точното представяне на данните за интензивност и m/z отношение на пиковете.
Апаратура[редактиране | редактиране на кода]
Масспектрометър[редактиране | редактиране на кода]

Очевидно почти всяка техника, която постига йонизиране, разделяне и детектиране на йоните в газова фаза, може да бъде приложена в масспектрометрията. Това води до една сравнително проста основна принципна схема, която имат всички масспектрометри. Масспектрометърът е изграден от: йонен източник, масов анализатор и детектор, които работят при условия на висок вакуум. В процедурата има стъпки на въвеждане на пробата, изпаряване, и последвала подходяща йонизация или десорбция/йонизация, но в повечето случаи не е лесно да се различат отделните стъпки. Също така след 1990 г. вече в апаратите се поставят и системи за съхранение и обработка на данните от детектора.
Йонен източник[редактиране | редактиране на кода]
Йонният източник е част от масспектрометъра, в която се извършва йонизирането (превръщането на молекулите в йони) на пробата. Масспектрите на едно и също вещество могат силно да се различават в зависимост от използвания метод на йонизация и поради това за различните вещества, както и за различните изследователски задачи, се използват различни начини на йонизация.
Йонизация с електронен удар (EI)[редактиране | редактиране на кода]
Това е първият метод за йонизация, използван в масспектрометрията. Остава един от най-широко използваните методи при анализа на атоми, от слабо – до среднополярни, нейонни органични съединения с молекулна маса над Mr ≈ 1000. Йонизацията на изпарените молекули от пробата се осъществява чрез сблъскването им с електрони. Те се получават от термокатод (нагрята жичка), най-често от волфрам или рений, ускоряват се от електрическо поле между катода и камерата и влизат в нея през тесен процеп. Енергията на тези йони е zV, където V е напрежението, ускоряващо електроните, а z – електронният заряд. Чрез промени в напрежението енергията на електроните варира обикновено между 5 и 100 eV. Стандартните масспектри се снемат при 70 eV, защото при тези условия се получава максимално количество йони, няма атоми и молекули, които да не могат да се йонизират, и спектрите са най-повторими. Когато изпарената молекула се срещне с електрон, имащ енергия по-голяма от йонизационната енергия на изследваното вещество, част от енергията на електрона се отдава на атома или молекулата, при което настъпва елиминиране на един електрон от него/нея и се получава положително зареден йон-радикал (молекулен йон)
M + e- → M+● + 2e-
Освен получаването на молекулен йон в йонизационната камера се извършват и редица други процеси, при които могат да се получат фрагментни йони, метастабилни йони, полизаредени йони и т.н. Повечето от процесите на получаване на тези частици са много бързи, от порядъка на fs, при което времето на живот на частиците след йонизацията им е около 1 микросекунда. За да се увеличи времето им на живот, е необходимо да се забавят процесите, т.е. да се намали сблъсъкът на частиците помежду им или с други часици. Това се постига, като йонизацията се извършва в силноразредена газова фаза, което означава, че свободният пробег на частиците е достатъчно дълъг, за да се сведе до минимум възможността им да се сблъскват с други частици и да рекомбинират или образуват бимолекули. Това е причината, поради която йонизацията с електронен удар се извършва при условия на висок вакуум от порядъка на 10-5 – 10-4 Pa [1].
Химическа йонизация (CI)[редактиране | редактиране на кода]
В масспектрометрията се търсят и методи за йонизация, които са по-меки от EI, защото молекулната маса е от ключово значение при изучаването на структурата на пробите. Химическата йонизация (Chemical ionization (CI)) е такъв „мек“ метод на йонизация.
При нея новите йонизирани форми се образуват, когато газови молекули взаимодействат с йоните. Химическата йонизация може да включва пренос на електрон, протон или други заредени частици между реагентите. Реагентите са неутралните молекули на пробата М и йоните на реакционния газ.
В химическата йонизация се използват бимолекулните реакции за образуването на йони на пробата. Наличието на бимолекулни реакции изисква значително голям брой йон-молекулни сблъсквания по време на времето на живот на реагентите в йонния източник. Това се постига с увеличаване на парциалното налягане на реакционния газ. Приема се, че за 1 µs време за пребиваване на частиците в йонен източник с налягане на газа около 2,5 х 102 Pa се извършват около 30 – 70 реакционни удара [2].
Четири са основните начини за получаване на йони от неутралните проби М при химическата йонизация (CI):
- M + [BH]+ → [M+H]+ + B Протонен преход
- [M] + B → [M-H]- + [BH]+ Протонен преход
- M + X+ → [M+X]+ Електрофилно присъединяване
- M + X+ → [M-A]+ + AX Отделяне на анион
- M + X+● → M+● + X Обмяна на заряд
Йонизация в електрическо поле[редактиране | редактиране на кода]
Макар и да се използва отдавна, този метод никога не е придобил широко разпространение в масспектрометрията главно поради експерименталните трудности, свързани с неговото прилагане. В редица случаи той дава извънредно ценна информация и неговото използване е необходимо.
Ако се приложи висок електрически потенциал върху силно огънат електрод, в мястото на огъване се получава много мощен градиент на потенциала. Това може да доведе до промени в молекулните орбитали на органичните молекули, намиращи се в съседство с електрода. Отнемането на електрон от молекулата чрез тунелен ефект към положително заредения електрод води до превръщането на молекулата в положително зареден йон, който може да се регистрира масспектрално. Поради ниската енергия, която той получава, неговата фрагментация е слаба.
Съществуват два варианта на описания метод. В единия от тях пробата в газова фаза преминава непосредствено близо до електричното поле, което е достатъчно да предизвика йонизацията. Този метод се нарича йонизация в поле. Още по-меки условия се постигат при десорбцията в поле, при която пробата се нанася върху електрода, така че йонизацията да става в кондензираната фаза или близко до повърхността на електрода. Повечето молекули първо се йонизират и после положително заредените йони се отблъскват от положително заредения електрод. Това прави метода на десорбция в поле много подходящ за труднолетливи и термично нестабилни съединения – както се вижда, йонизацията става практически без изпаряване и това изключва топлинното разпадане.
Приложение на масспектрометрията[редактиране | редактиране на кода]
Масспектрометрията намира приложение в химията, биохимията, физиката, астрофизиката, фармацията, медицината, вакуумната техника за:
- идентифициране на непознати вещества по масата на съставящите ги молекули и техните фрагменти
- определяне на изотопното съдържание на елементите в компонента
- определяне на структурата на веществата чрез изследване на тяхната фрагментация
- определяне на количеството на компонента в пробата (чрез използването на добре разработен за целта метод)
- изучаване на фрагментацията на вещества в газова фаза
- определяне на други физични, химични и биологични свойства на веществата
Основният принцип на масспектрометрията е да се превърнат атомите на органичното или неорганично вещество в йони чрез подходящ метод, да се разделят според тяхното отношение маса-заряд (m/z) и да се детектират качествено и количествено съответно чрез определяне на m/z и количеството йони. Образецът може да бъде йонизиран термично, под въздействието на електрическо поле или чрез бомбардирането му с ускорени частици – електрони, йони или фотони. Получените „йони“ могат да бъдат единично йонизирани атоми, атомни клъстери, молекули или техните фрагменти. Разделянето на йоните се извършва с помощта на статично или динамично електрическо и магнитно поле. При методите за йонизация с ускорени частици освен йони, електрони и фотони могат да бъдат добавени и неутрални атоми и големи клъстери от йони.
Източници[редактиране | редактиране на кода]
- ↑ а б Gross. J. Mass Spectrometry. Germany, Springer, 2004. ISBN 3-540-40739-1.
- ↑ Field, F.H.; Munson, M.S.B. Reactions of Gaseous Ions. XIV. Mass Spectrometric Studies of Methane at Pressures to 2 Torr. // J. Am. Chem. Soc. 87. 1965. с. 3289 – 3294.
