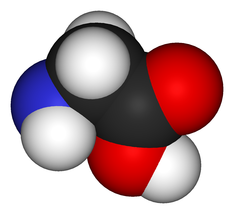
Глицин
| Глицин | |
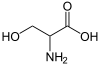
 Химична структура | |
| Имена | |
|---|---|
| Други | аминоетанова киселина аминооцетна киселина |
| Свойства | |
| Формула | C₂H₅NO₂ |
| Моларна маса | 75,032 u[1] |
| Плътност | 1,607 g/cm³ |
| Точка на топене | 233 °C |
| pKa | 2,35 |
| Идентификатори | |
| CAS номер | 56-40-6 |
| PubChem | 750 |
| ChemSpider | 730 |
| DrugBank | DB00145 |
| KEGG | D00011 |
| MeSH | D005998 |
| ChEBI | 15428 |
| ChEMBL | CHEMBL773 |
| ATC | B05CX03 |
| SMILES | C(C(=O)O)N |
| InChI | InChI=1S/C2H5NO2/c3-1-2(4)5/h1,3H2,(H,4,5) |
| InChI ключ | DHMQDGOQFOQNFH-UHFFFAOYSA-N |
| UNII | TE7660XO1C |
| Gmelin | 1807 |
| Данните са при стандартно състояние на материалите (25 °C, 100 kPa), освен ако не е указано друго. | |
| Глицин в Общомедия | |
Глицинът е една от двадесетте канонични аминокиселини. Той е най-простата аминокиселина, като страничното му разклонение е един водороден атом. Кодиращите го кодони са GGU, GGC, GGA, GGG.
Биосинтеза
[редактиране | редактиране на кода]Глицинът не е незаменима аминокиселина за човека и може да бъде синтезиран от аминокиселината серин, която на свой ред се синтезира от 3-фосфоглицерат – метаболит на гликолизата. В повечето организми тази трансаминазна реакция се катализира от ензима серин хидроксиметилтрансфераза, опериращ с кофактора пиродоксал фосфат:[2]
| Серин | FH4 | серин хидроксиметилтрансфераза | Глицин | N5,N10-метилен тетрахидрофолат | |||
|
+ | 
|

|
+ | 
| ||
| H2O | |||||||

| |||||||
| H2O | |||||||
| серин хидроксиметилтрансфераза | |||||||
В черния дроб на гръбначните глициновата синтеза се катализира от ензима глицин синтаза (известен и като глицин-разделящ ензим). Реакцията е обратима и равновесна.:[2]
| N5,N10-метилен тетрахидрофолат | глицин синтаза | Глицин | |

|

| ||
| CO2 NH+ 4 НАДН2 |
FH4 НАД+ | ||

| |||
| CO2 NH+ 4 НАДН2 |
FH4 НАД+ | ||
Глициновите аминотрансферази могат да катализират синтеза на глицин от глиоксилат и глутамат или аланин. За разлика от останалите аминотрансферазни реакции, глициновите аминотрансферази силно облагоприятстват глициновия синтез. Важни пътища за образуване на глицин при бозайници са от холин и серин.[3]
Комплексът, свързан с разграждането на глицин в чернодробните митохондрии, разгражда глицина до CO2 и NH+
4 и образува N5, N10-метилен тетрахидрофолат. Системата за разграждане на глицин се състои от три ензима и Н-протеин, който има ковалентно прикрепен дихидролипоилен остатък. При некетотична хиперглицинемия (рядко вроден недостатък в глициновото разграждане), глицинът се акумулира във всички тъкани на тялото, включително в централната нервна система. Дефектът в първичната хипероксалурия е неспособността да се катаболизира глиоксилатът, образуван при дезаминирането на глицин. Последващото окисление на глиоксилата до оксалат води до уролитиаза, нефрокалциноза, хипертония или смърт, вследствие на бъбречна недостатъчност. Дефект в бъбречната тубуларна реабсорбция причинява глицинурия.[3]
В повечето белтъци глицинът е слабо застъпен, като забележително изключение прави колагена, който е изграден от над 35% глицин.[2][4] Притежава най-късата странична верига (със само един водороден атом), което определя позицията и в молекулата на колагена – на местата на усукване на трите вериги, аминокиселинните радикали си пречат пространствено.
Глицинът участва в биосинтеза на хем, пурини, креатин и сакрозин.[3]
Източници
[редактиране | редактиране на кода]- ↑ glycine // PubChem. Посетен на 19 октомври 2016 г. (на английски)
- ↑ а б в Nelson, David L.; Cox, Michael M. (2005), Principles of Biochemistry (4th ed.), New York: W. H. Freeman, pp. 127, 675 – 77, 844, 854, ISBN 0-7167-4339-6
- ↑ а б в Rodwell VW, Bender DA, Botham KM, Kennelly PJ, Weil PA. Harpers’ Illustrated Biochemistry, 31 st Edition.
- ↑ Szpak, Paul. Fish bone chemistry and ultrastructure: implications for taphonomy and stable isotope analysis // Journal of Archaeological Science 38 (12). 2011. DOI:10.1016/j.jas.2011.07.022. с. 3358 – 3372.
| |||||