Треонин
| Треонин | |
  | |
| Имена | |
|---|---|
| По IUPAC | Треонин |
| Други | 2-амино-3-хидроксибутанова киселина |
| Свойства | |
| Формула | C4H9NO3 |
| Моларна маса | 119.12 g/mol |
| Точка на топене | 256 °C |
| Разтворимост във вода | (H2O, g/dl) 10.6(30°),14.1(52°),19.0(61°) |
| pKa карбокси | 2.63 |
| pKb амино | 10.43 |
| Идентификатори | |
| CAS номер | 80-68-2, 72-19-5 |
| PubChem | 6288 |
| ChemSpider | 6051 |
| DrugBank | DB00156 |
| KEGG | D00041 |
| MeSH | D013912 |
| ChEBI | 57926 |
| ChEMBL | CHEMBL291747 |
| SMILES | C[C@H]([C@@H](C(=O)O)N)O |
| InChI | 1S/C4H9NO3/c1-2(6)3(5)4(7)8/h2-3,6H,5H2,1H3,(H,7,8)/t2-,3+/m1/s1 |
| InChI ключ | AYFVYJQAPQTCCC-GBXIJSLDSA-N |
| UNII | TFM6DU5S6A |
| Gmelin | 82510 |
| Данните са при стандартно състояние на материалите (25 °C, 100 kPa), освен ако не е указано друго. | |
| Треонин в Общомедия | |
Треонин (съкратено Thr или T)[1] е α-аминокиселина с химическа формула HO2CCH(NH2)CH(OH)CH3. Нейните кодони са ACU, ACA, ACC и ACG. Тя представлява полярна незаменима аминокиселина. Треонинът заедно със серина и тирозина са единствените три аминокиселини, съдържащи хидроксилна група. Също така тя е и една от двете протеиногенни аминокиселини, притежаващи хирална странична верига, другата от които е изолевцин.
Треониновият остатък в състава на полипептидните вериги е обект на множество посттранслационни модификации. Хидроксилната група в страничната верига може да бъде O-гликозилирана. В допълнение треониновите остатъци могат да бъдат фосфорилирани под действието на серин- и треонин киназите. В своята фосфорилирана форма се нарича фосфотреонин.
История[редактиране | редактиране на кода]
Треонинът е последната от 20-те протеиногенни аминокислеини, открита през 30-те години на 20 век от Уилям Къминг Роуз.[2]
Стереоизомерия[редактиране | редактиране на кода]
  |
| L-Треонин (2S,3R) и D-Треонин (2R,3S) |
 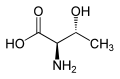 |
| L-ало-Треонин (2S,3S) и D-ало-Треонин (2R,3R) |
Метаболизъм[редактиране | редактиране на кода]
Треонинът се метаболизира по два пътя:
- Превръща се в пируват от треонин дехидрогеназа. Като междинен метаболит в този път, пируватът претърпява тиолиза с КоА до продуктите ацетил-КоА и глицин.
- При хората може да се доведе до α-кетобутират по по-малко използван метаболитен път, чрез ензима серин дехидратаза, като по-нататък стига до сукцинил-КоА.
- Треонин алдолазата (EC 4.1.2.5) разцепва треонина на глицин (NH3, CO2 и въглеводороден остатък 5,10-CH2-H4-фолат) и ацеталдехид. Окисляването на ацеталдехида до ацетат е последвано от образуване на ацетил-CoA.
Чрез декарбоксилиране води до образуването на биогенния амин пропаноламин, участващ в състава на витамин В12.[2]
Хранителни източници[редактиране | редактиране на кода]
Храни богати на треонин са сиренето, птичето месо, рибата, леща и др.
Рацемичен треонин може да се приготви от кротонова киселина, чрез алфа-функционализиране с живачен ацетат.[3]
Източници[редактиране | редактиране на кода]
- ↑ Nomenclature and symbolism for amino acids and peptides (IUPAC-IUB Recommendations 1983). – Pure Appl. Chem., 56(5), 595–624, 1984, doi:10.1351/pac198456050595
- ↑ а б Rodwell VW, Bender DA, Botham KM, Kennelly PJ, Weil PA. Harpers’ Illustrated Biochemistry, 31 st Edition.
- ↑ dl-Threonine // Org. Synth 20. 1940. с. 101.; Coll. Vol., 3, 813.
| |||||
| Тази страница частично или изцяло представлява превод на страницата Threonine в Уикипедия на английски. Оригиналният текст, както и този превод, са защитени от Лиценза „Криейтив Комънс – Признание – Споделяне на споделеното“, а за съдържание, създадено преди юни 2009 година – от Лиценза за свободна документация на ГНУ. Прегледайте историята на редакциите на оригиналната страница, както и на преводната страница, за да видите списъка на съавторите.
ВАЖНО: Този шаблон се отнася единствено до авторските права върху съдържанието на статията. Добавянето му не отменя изискването да се посочват конкретни източници на твърденията, които да бъдат благонадеждни. |

