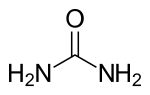
Карбамид
| Карбамид | |
| Имена | |
|---|---|
| По IUPAC | Карбамид |
| Други | Карбонилдиамид Диамид Урея Пиагран |
| Свойства | |
| Формула | CH₄N₂O |
| Моларна маса | 60,032 u[1] |
| Плътност | 1,32 g/cm³ |
| Точка на топене | 132,7 °C |
| Точка на кипене | 174 °C |
| pKa | 0,18[2] |
| Термохимия | |
| Стандартна енталпия на образуване | −333,3 kJ/mol |
| Идентификатори | |
| CAS номер | 57-13-6 |
| PubChem | 1176 |
| ChemSpider | 1143 |
| DrugBank | 03904 |
| KEGG | D00023 |
| MeSH | D014508 |
| ChEBI | 16199 |
| ChEMBL | CHEMBL985 |
| RTECS | YR6250000 |
| ATC | D02AE01 |
| SMILES | C(=O)(N)N |
| InChI | InChI=1S/CH4N2O/c2-1(3)4/h(H4,2,3,4) |
| InChI ключ | XSQUKJJJFZCRTK-UHFFFAOYSA-N |
| UNII | 8W8T17847W |
| Gmelin | 1378 |
| Данните са при стандартно състояние на материалите (25 °C, 100 kPa), освен ако не е указано друго. | |
| Карбамид в Общомедия | |
Карбамид (също урея или карбонилдиамид; да не се бърка с пикочна киселина) е органично съединение, краен продукт на обмяната на веществата при много животни, получен при разграждането на азотните съединения (напр. аминокиселини). Отделя се чрез урината. Чистият карбамид е бяло кристално вещество със слаб мирис на амоняк.
История[редактиране | редактиране на кода]
Карбамидът е първото синтетично получено органично съединение. Открит е през 1773 г. от френския химик Илер Руел (Hilaire Rouelle). През 1828 г. е синтезиран за първи път от Фридрих Вьолер при реакция на калиев цианат и амониев сулфат:[3]
Това противоречало на тогавашното схващане, че органичните съединения могат да се синтезират само от живи същества чрез така наречената „жива сила“ (vis vitalis).[4] Това поставя началото на органичната химия.
Физиология[редактиране | редактиране на кода]
Карбамид се получава при белтъчната обмяна на веществата. За да се избегне отделянето на амоняк (NH3) при разграждането на белтъците, техните аминогрупи се свързват в черния дроб към безвредната молекула на карбамида.
Приложение[редактиране | редактиране на кода]
Поради високото си съдържание на азот (46%) и сравнително по-ниските транспортни разходи карбамидът е най-значимият азотен тор в световен мащаб. От предимство е и сравнително бавното усвояване от растенията. За разлика от карбамида, повечето други азотни торове (нитратни, амониеви) са много добре разтворими във вода, бързо се измиват при обилни валежи и попадат в подпочвените води. По тази причина голяма част от произведения карбамид се използва като азотен тор.
В таблиците по-долу са дадени данни за износа и вноса на карбамид по страни (най-големите вносители, съответно износители за 2018 г.):
| Страна | Износ 2018 милиона тона |
Износ 2005 милиона тона |
|---|---|---|
| Русия | 6,96 | 4,57 |
| Катар | 4,98 | 1,97 |
| Египет | 4,11 | 0,016 |
| Оман | 3,43 | 0,82 |
| Саудитска Арабия | 3,41 | 1,81 |
| Китай | 2,45 | 1,57 |
| Страна | Внос 2018 милиона тона |
Внос 2005 милиона тона |
|---|---|---|
| Бразилия | 5,53 | 1,56 |
| Индия | 5,46 | 1,58 |
| САЩ | 3,12 | 5,62 |
| Тайланд | 2,45 | 1,59 |
| Турция | 2,20 | 0,81 |
| Австралия | 1,86 | 1,15 |
Тъй като основната суровина за производството на карбамид е природен газ, страните с големи запаси на газ са обикновено и най-големите износители.
Друго значимо приложение е производството на карбамидформалдехидни смоли (аминопласти). Освен това той се прилага в медицината в различни козметични смеси за омекотяване на кожата, ноктите и др.
Карбамидът може да се използва като хранителна добавка (E927b) при производството на дъвка. В различни фуражни смеси се добавя като източник на азот, което ускорява образуването на белтъци/мускулна маса.
Карбамидът е основната съставка на AdBlue, реагент, който се използва за редуциране на емисиите на азотни оксиди при дизеловите двигатели.
Свойства[редактиране | редактиране на кода]
При нагряването на карбамид може да се получи биурет:

При тази реакция се отделя една молекула амоняк. Биуретът е отровен за някои растения, затова съдържанието му в карбамида, използван като тор, се редуцира.
Индустриален синтез[редактиране | редактиране на кода]
Карбамидът се произвежда индустриално в големи количества, около 100 млн. тона годишно.[4] Например през 2004 г. в света са произведени 127 млн. тона карбамид.
Уравнения:
- от амоняк и въглероден диоксид се получава амониев карбамат
- амониевият карбамат се разпада до карбамид и вода
Това е т. нар. процес на Бош – Майзер, разработен през 1922 г. Сумарният топлинен ефект е положителен.
Амонякът и въглеродният диоксид за производството на карбамид се получават при непълно изгаряне на природен газ. При това първо се получават водород и въглероден монооксид. Водородът реагира с азота от въздуха до получаване на амоняк, а въглеродният монооксид с кислорода – до получаване на въглероден диоксид. По тази причина основните суровини за производството на карбамид са природен газ, въздух и вода.
Източници[редактиране | редактиране на кода]
- ↑ urea // PubChem. Посетен на 19 октомври 2016 г. (на английски)
- ↑ chemanalytica.com
- ↑ Kyriacos Nicolaou, Montagnon, „Molecules That Changed The World“, Wiley-VCH, isbn = 978-3-527-30983-2
- ↑ а б Galatzer-Levy, R. M. (1976) „Psychic Energy, A Historical Perspective“. Ann Psychoanal 4:41 – 61.
- ↑ knoema.com; Посетен на 12.04.2021 г.
- ↑ knoema.com; Посетен на 12.04.2021 г.
|