Множествена склероза
| Множествена склероза | |
 | |
| Класификация и външни ресурси | |
|---|---|
| МКБ-10 | G35-G37 G35 Множествена склероза G36 Друга форма на остра дисеминирана демиелинизация G36.0 Оптиконевромиелит, болест на Девик G36.1 Остър и подостър хеморагичен левкоенцефалит [болест на Hurst] G36.8 Друга уточнена форма на остра дисеминирана демиелинизация G36.9 Остра дисеминирана демиелинизация, неуточнена G37 Други демиелинизиращи болести на централната нервна система G37.0 Дифузна склероза G37.1 Централна демиелинизация на corpus callosum G37.2 Централна понтинна миелинолиза G37.3 Остър трансверзален миелит при демиелинизираща болест на централната нервна система G37.4 Подостър некротизиращ миелит G37.5 Концентрична склероза на Бало G37.8 Други уточнени демиелинизиращи болести на централната нервна система G37.9 Демиелинизираща болест на централната нервна система, неуточнена |
| МКБ-9 | 340 |
| МКБО | 126200 |
| Множествена склероза в Общомедия | |
Множествената склероза (Encephalomyelitis disseminata, известна още и като Дисиминативна склероза или съкратено МС) е автоимунно възпалително невродегенеративно хронично заболяване с неизяснена етиология и вероятна генетична предразположеност. Като ключов фактор в развитието ѝ могат да бъдат факторите на околната среда и инфекциозни причинители. МС засяга мастната миелинова обвивка на аксоните на човешкия главен и гръбначен мозък. Това причинява демиелинизация и образуването на лезии в мозъка, което води до широк спектър от признаци и симптоми.[1] Заболяването се развива най-често в ранните години на зрелостта, като се среща по-често при жените.[1] Разпространението му варира в широки граници между 2 до 150 болни на 100 000 души.[2] МС е описана за първи път през 1868 г. от Жан Шарко.[3]
Множествената склероза засяга способността на нервните клетки на главния и гръбначния мозък да комуникират помежду си. Нервните клетки комуникират като си изпращат електрически сигнали наречени потенциал на действие по своите дълги израстъци наречени аксони, които са обгърнати от изолираща субстанция – миелин. При МС собствената имунна система атакува и унищожава миелиновото покритие. Когато миелинът бъде загубен, аксоните не могат да провеждат ефективно сигналите.[4] Името Multiple sclerosis идва от склеротирането (образуването на плаки или лезии) в бялото мозъчно вещество на главния и гръбначния мозък, което е изградено предимно от миелин.[3] Въпреки обширните познания за протичането и прогресирането на заболяването пусковият механизъм остава неизвестен. Различни теории предлагат като причини генетичната предиспозиция или инфекция, както и влиянието на рискови фактори от обкръжаващата среда.[4][5]
Почти всички неврологични симптоми могат да съпровождат заболяването, като често се стига до физическа и ментална инвалидизация.[4] МС има няколко форми. Новите симптоми се появяват като дискретни атаки (пристъпна форма) или бавно се натрупват с времето (прогресивна форма).[6] В периодите между пристъпите симптомите може да изчезват напълно, но често се явяват трайни неврологични проблеми, особено с напредване на болестта.[6]
Не съществува познато лекарство за множествена склероза. Лечението е насочено към възстановяване на функциите след пристъп, превенция от нови пристъпи и предотвратяване на трайната инвалидизация.[4] Медикаментите използвани за лечение на МС могат да имат негативен ефект или да са слабо поносими от пациентите. Въпреки липсата на подкрепящи научни изследвания много от заболелите се насочват към алтернативни методи на лечение. Трудно е да се прави прогноза. Тя зависи от формата на заболяването, индивидуалните характеристики и особености на болния, от началните симптоми, както и от степента и темпа на развитие и инвалидизация.[7] Средната продължителност на живот при засегнатите пациенти е с 5 до 10 години по-ниска от останалата част на населението.[1]
Класификация[редактиране | редактиране на кода]

Съществуват няколко вида или модела на прогресиране на множествената склероза. Определянето на вида ѝ се базира на последните тенденции в развитието на болестта и се използва за прогнозиране на бъдещото развитие. То е важно не само за прогнозирането, но и за назначаването на подходящо лечение. През 1996 г. Националното дружество по множествена склероза на САЩ стандартизира четири форми на заболяването:[6]
- Пристъпно-ремитентна;
- Вторично прогресивна;
- Първично прогресивна;
- Пристъпно-прогресивна.
Пристъпно-ремитентната форма се характеризира с рецидиви, които не могат да се предвидят, следвани от относително спокойни периоди от няколко месеца и дори години на ремисия, без нови симптоми и патофизиологична активност. Симптомите появили се по време на кризата може да отшумят или да оставят трайни последствия, като вторият случай зачестява с напредване на болестта.[1] Пристъпно-ремитентната форма е началната форма на болестта при 80% от пациентите.[1] Когато симптомите винаги отшумяват след рецидив, някои автори говорят за доброкачествена МС,[8] въпреки че с течение на времето се натрупват някои от симптомите.[1] Понякога пристъпно-ремитентната форма започва с клинично изолиран синдром (КИС). При КИС пациентите симптоматиката сочи към демиелинизация, но не покрива критериите за множествена склероза.[1][9] Все пак само 30 до 70% от хората претърпели КИС развиват МС впоследствие.[9]

Вторично прогресивната форма на МС (наричана още скоротечна или галопираща) се развива при около 65% от пациентите с пристъпно-ремитентната форма. Характеризира се с постепенно влошаване на неврологичното състояние, като не се наблюдават ясно отличими периоди на ремисия.[1][6] Понякога се наблюдават случайни рецидиви или слаби ремисии.[6] Средно периодът между началото на заболяването под пристъпно-ремитентната форма до достигане на вторично прогресивна форма е 19 години.[10]
Първично прогресивната форма се среща при приблизително 10 – 15% от индивидите и се характеризира с липсата на ремисии след началните симптоми на МС.[11] Типично за тази форма е постепенното засилване на симптомите от началото на болестта, липсата или наличието на спорадични и съвсем слаби ремисии и подобрение на състоянието.[6] Възрастта на разболяване от първично прогресивна форма е по-висока от тази за пристъпно-ремитентната форма, но близка до средната възраст на преминаване на пристъпно-ремитентната форма във вторично прогресивна. И в двата случая това се случва на възраст около 40 години.[1]
Пристъпно-прогресивната форма е най-рядко срещаната и се характеризира с прогресивно влошаване на клиничната картина, но и наличието на релапси.[6]
Срещат се и редица атипични форми на МС, които нямат стандартната клинична картина. Такива са оптикомиелит, концентрична склероза на Бало, дифузна миелокластна склероза (болест на Шилдер) и остра множествена склероза наричана и злокачествена множествена склероза. Съществува спор между учените дали това са форми на МС или отделни заболявания.[12] МС се развива и по различен начин при децата като е необходимо повече време за достигане на прогресивната фаза.[1] Въпреки това те я достигат при по-ниска средна възраст от възрастните.[1]
Епидемиология[редактиране | редактиране на кода]

Основните критерии за оценка при епидемиологията на МС са два: заболеваемост и разпространение.
Заболеваемостта представлява количеството нови случаи на определен брой хора за даден период от време (обикновено нови случаи на сто хиляди души за една година).
Разпространението представлява общия брой болни в популацията в даден момент. Зависи не само от количеството нови случаи, но и от степента на преживяемост и миграцията на засегнатите индивиди. МС има разпространение, което силно варира, 2 до 150 на 100 000, в зависимост от държавата и спецификите на популацията.[2] Изследванията на популационните и географските особености на епидемиологичния профил на МС са широко застъпени[13] и са довели до създаването на различни теории за етиологията на болестта.[5][13][14][15]
МС обичайно се появява в периода на ранната зрелост, около тридесетте, но може да се развие и още в детството.[1] Първично прогресивната форма е по-обичайна за хора навлезли в петдесетте години на живота си.[11] Както при повечето автоимунни заболявания и МС покосява по-често жените, като тази тенденция може да се засилва.[1][16] При децата половият фактор е още по-силно изразен,[1] докато при хора преминали петдесет години МС засяга двата пола почти с еднаква честота.[11]
Наблюдава се силно изразен градиент на заболеваемостта по отношение на географската ширина. Така при екватора МС се среща най-рядко като честотата се увеличава по посока на полюсите.[1][16] Климат, слънчева светлина и витамин D са сред потенциалните фактори изследвани като вероятни причини за наличието на този географски градиент.[15] Съществуват и изключения от зависимостта север-юг, както и изменения в нивото на разпространения във времето,[1] като е възможно тази тенденция изобщо да изчезне.[16] Това показва, че другите фактори като обкръжение и генетични особености трябва да се вземат предвид при обяснението за причините за МС.[1] МС е много по-често срещана при популации от северно-европейци.[1] Даже в области, където МС е по-често срещана някои етнически групи са в нисък риск от развитие на болестта: саами, туркмени, индианци, канадски хутерити, африканци и маори.[14]
Факторите на средата по време на детството могат да окажат съществена роля в развитието на МС по-нататък в живота. Няколко изследвания на мигранти показват, че ако миграцията е осъществена преди петнадесетата годишнина, мигрантът придобива предразположението, характерно за новия регион. Ако миграцията е осъществена след петнадесетата година обаче, мигрантът запазва податливостта, характерна за родния му регион.[1][14] Установена е връзка между сезона на раждане и развиването на МС, което подкрепя теорията за връзка със слънчевата светлина и витамин D. Така например през ноември са родени по-малко хора с МС отколкото през май.[17]
Причини[редактиране | редактиране на кода]
Множествената склероза вероятно е резултат от комбинацията на различни фактори: генетична предиспозиция, инфекциозни процеси и влияние на средата.[1] Много вероятно и други предпоставки като съдови проблеми също да допринасят за развитието ѝ.[18]
Генетични[редактиране | редактиране на кода]

Множествената склероза не е генетично заболяване, но различни генетични вариации определят по-висок риск от развитието на болестта.[19]
Рискът за развитие на заболяването е по-висок при роднини на болни, в сравнение с общата популация, особено в случаите, когато става въпрос за брат/сестра, родители или деца.[4] 20% от заболелите имат пряка роднинска връзка.[1] При еднояйчни близнаци само в 35% от случаите и двата заболяват, като този процент пада до 5% при обикновените братя и сестри и е по-нисък при полубратята (-сестрите). Това сочи за полигенно обусловена податливост.[1][4]
Изглежда МС е по-разпространена при определени етнически групи, най-вече от европеидната раса.[20]
Освен наличието на фамилна обремененост са установени определени гени свързани със заболяването от МС. Вариации със системата на човешкия левкоцитен антиген (HLA) (група от гени в хромозома шест, обуславящи главния комплекс за тъканна съвместимост при човек) повишават шанса за развитие на МС.[1] Най-достоверното откритие е за връзка между множествената склероза и алелите за MHC HLA-DR15 и HLA-DQ6.[1] Установено е, че други локуси като HLA-C554 и HLA-DRB1*11 имат протективен ефект.[1]
Външни фактори[редактиране | редактиране на кода]
Различни фактори на средата, инфекциозни и неинфекциозни, се явяват рискови по отношение развитието на МС. Въпреки че някои от тях са манипулируеми, са необходими още много изследвания, особено клинични изпитания, за да се установи, дали тяхното отстраняване може да спомогне за превенцията на МС.[14]
- МС е по-често срещана с отдалечаване от екватора, макар да има и изключения.[1]
- Намаленото излагане на слънчева светлина повишава риска от заболяване.[14] Предполага се, че биологичният механизъм на повишения риск е обусловен от намалената продукция на витамин D при намалено излагане на слънце.[14][15][21]
- Силният и перманентен стрес също е фактор, макар доказателствата в тази насока да са немного.[14]
- Пушенето е рисков фактор за развитие на МС.[15]
- Установена е връзка с различни професионални вредни среди и излагането на токсини (най-вече разтворители).[14]
- Ваксинирането може да бъде фактор повлияващ развитието на МС, макар че повечето изследвания отричат такава връзка.[14][22][23][24][25]
- Хронична гръбначномозъчна венозна недостатъчност.[26][27]
- Диета.[28]
- Прием на хормони.[15]
При болни от МС се наблюдава статистически значимо (в сравнение с общата популация) по-ниска заболеваемост от подагра, като са установени по-ниски нива на пикочна киселина при пациентите с МС в сравнение със здравите индивиди. Това води до хипотезата, че пикочната киселина протектира от развитие на МС, но точният механизъм остава неизвестен.[29]
Инфекции[редактиране | редактиране на кода]
За много микроорганизми има сведения, че е възможно да имат отношение към развитието на МС, но няма твърди доказателства в тази насока[4]
Генетичните фактори са в състояние да обяснят някои от географските и епидемиологични особености в разпространението на МС, като високата честота при някои семейства и намаляването на риска с увеличаване на генетичната дистанция. Те обаче не дават обяснение на други феномени, като промяната на риска от заболяване при миграция в ранна възраст.[5] Обяснение на този епидемиологичен факт може да бъде инфекция причинена по-скоро от широко разпространен патоген отколкото от рядко срещан.[5] Съществуват различни хипотези обясняващи как точно се случва това.
- Хигиенната хипотеза предлага, че излагането на някои инфекциозни агенти в ранна възраст има предпазващ ефект, докато развитието на МС е следствие на срещата на организма с тези агенти в по-късен етап от развитието.[1]
- Хипотезата за често срещания патоген предлага, че заболяването се отключва от патоген широко разпространен в регионите с повишено ниво на МС. Този патоген е често срещан и при повечето индивиди присъства асимптомно за дълго време. При много малък брой от случаите и след много години предизвиква започването на процес на демиелинизация.[5][13]
Хигиенната теория се радва на повече поддръжници и е по-добре приета.[5]
Съществуват известни доказателства подкрепящи теорията за участие на вируси като иницииращи фактори: (1) наличие на олигоклонални клъстери от антитела в мозъка и ликвора на повечето пациенти, (2) връзка на някои вируси с процеса на демиелинизация, (3) инициация на демиелинизацията при опитни животни чрез вирусна инфекция.[30] Групата на човешките херпес вируси (Herpesviridae) е кандидат за вируси свързани с развитието на МС. При индивиди, които никога не са били инфектирани с вирус на Епщайн – Бар, има намален риск от заболяване, а при тези инфектирани в ранните години на зрелостта рискът е значително по-висок отколкото при заразените по време на детството.
Други вируси, за които съществуват данни, че имат отношение към развитието на МС, са вирусите на морбили, заушка и рубеола.[1]
Патофизиология[редактиране | редактиране на кода]
Увреждане на кръвно-мозъчната бариера[редактиране | редактиране на кода]
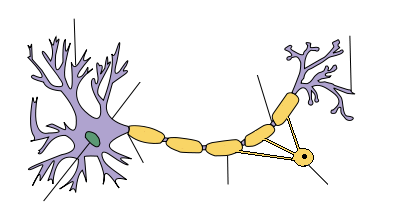
| Неврон с миелинов слой около аксона |
|---|
Кръвно-мозъчната бариера е капилярна система, която възпрепятства нахлуването на компоненти на имунната система в нервната система.[4] Кръвно-мозъчната бариера нормално е непропусклива за T-клетките, освен при вирусни инфекции, които намаляват целостта на плътните клетъчни контакти (zonula occludens) образуващи бариерата.[4] Когато бариерата бъде възстановена, след отстраняване на инфекцията и вирусите, T-клетките се оказват хванати в мозъка.[4]
Автоимунитет[редактиране | редактиране на кода]
Понастоящем е прието, че МС е имуномедиирано заболяване, последствие от сложни взаимодействия на индивидуални генетични особености и все още не напълно идентифицирани фактори от обкръжаващата среда.[4] Уврежданията са резултат от дейността на собствената имунна система на пациента. Имунната система атакува нервната, като това може да е следствие от експозицията на молекула със структура подобна на тази на собствена молекула (молекулна мимикрия).[4]
- Лезии
Лезиите при МС най-често засягат бялото мозъчно вещество в зоните близо до мозъчните стомахчета на малкия мозък, ствола, базалните ганглии и гръбначния мозък, както и оптичния нерв. Функцията на бялото мозъчно вещество е да предпазва аксоните на невроните, както и да осигурява изолация при протичането на нервния импулс. Периферната нервна система се засяга по-рядко.[4]
При МС се унищожават олигодендроцитите, клетките отговорни за изграждането и поддържането на мастния миелинов слой, който спомага за пренасянето на електрическите импулси по невроните.[4] МС води до изтъняване, а впоследствие и на загуба на миелиновия слой, което е последвано и от загубата на аксоните с напредване на болестта. След разрушаването на миелиновата покривка невроните не могат да провеждат ефективно нервните сигнали.[4] В ранните фази от болестта съществува процес на регенерация, наричан ремиелинизация, но олигодендроцитите не са в състояние да възстановят миелиновия слой напълно.[31] Повтарящите се атаки водят до все по-слаба ремиелинизация, докато не се образуват плаки (лезии) около увредените аксони.[31] Съществуват различни модели на формиране на лезиите.[32]
- Възпаление
Освен от демиелинизацията друг патологичен отличителен белег на болестта е възпалението. Според имунологичното обяснение на МС възпалителният процес е причинен от T-клетките, вид лимфоцити. Лимфоцитите са клетки, които играят важна роля в защитните сили на организма.[4] При МС, T-клетките влизат в мозъка през кръвно-мозъчната бариера. Данните от животински модели също така сочат и известна роля на B-клетки в допълнение на T-клетките в развитието на болестта.[33]
T-клетките разпознават миелина като чужд за организма антиген и го атакуват така, сякаш е вирус. Това води до възпалителни процеси, стимулиране на други имунни клетки и разтворими фактори като цитокини и антитела. Пробивът в кръвно-мозъчната бариера от своя страна води до редица други вредни ефекти като оток, активирането на макрофаги и цитокини и други деструктивни протеини.[4]
Признаци и симптоми[редактиране | редактиране на кода]

Множествената склероза може да има най-различни неврологични симптоми: промени в сензитивността (хипестезия), мускулна слабост, мускулни спазми, затруднено движение; трудности при координация и баланс; проблеми с говора (дизартрия) и преглъщането (дисфагия), зрителни проблеми (нистагмус), възпаление на очния нерв, фосфен или диплопия), лесна уморяемост, остър или хроничен болков синдром, проблеми с уринирането и дефекацията, намаляване на познавателната способност или емоционална нестабилност (най-вече депресия). Основният начин за оценка на прогреса на инвалидизация и засилване на симптомите е Скалата за оценка на инвалидния статус.[34]
Началните симптоми обикновено са преходни, слаби и ограничени. Те често не са повод за търсене на медицинска помощ и обикновено се установяват ретроспективно едва след няколко атаки, когато диагнозата е вече поставена. Най-честите начални симптоми са: промени в осезанието на ръцете, краката или лицето (33%), частична или пълна загуба на зрение (възпаление на очния нерв) (20%), слабост (13%), двойно виждане (7%), нестабилност при вървене (5%), проблеми с баланса (3%); в много редки случаи като начални симптоми са установени афазия или психоза.[35][36] Петнадесет процента от пациентите имат множество симптоми когато търсят за пръв път медицинска помощ.[37]
Пикочна система[редактиране | редактиране на кода]
Проблеми с пикочната система и уринирането имат 70 – 80% от пациентите с МС. Тези проблеми оказват съществено влияние както върху хигиенните навици, така и върху социалния живот.[38][39]Основните проблеми са увеличената честота и неотложност на уринирането. Паралелно с тях се появяват и затруднения в започването на уриниране, запъване, изпускане, усещане за незавършеност, като понякога се наблюдава и задържане. При наличие на задържане се развиват и вторични инфекции на проводните пътища.
В процеса на уриниране са въвлечени множество корови и подкорови структури,[40] така че симптомите се проявяват в зависимост локацията на лезиите в ЦНС.
Лечението е насочено в няколко насоки: облекчаване на симптомите на уринарната дисфункция, лечение на вторичните инфекции, редукция на фактори водещи към усложнения и превенция на бъбречната функция. Лечението може да се насочи в две насоки: медикаментозно и немедикаментозно.
Медикаментозното лечение силно зависи от произхода и вида на дисфункцията. Няколко примера за използвани медикаменти са:[41] алфузозин при задържане,[42] троспиум и флавоксит при невъзможност за задържане и неотложност,[43][44] десмопресин при ноктурия.[45][46]
Немедикаментозната терапия включва тренировки и стимулация на мускулатурата на тазовото дъно, песари, а понякога периодична катетеризация.[47]
Познавателна способност[редактиране | редактиране на кода]
Някои от най-често срещаните проблеми засягат краткосрочната памет, вниманието, способността за пространствено виждане, способността и скоростта за извършване на всякаква дейност.[48] Други свързани симптоми са емоционална нестабилност, лесна физическа уморяемост, както и прострация (неврологична умора). Познавателният дефицит е независим от физическата неспособност и може да се срещне и при липсата на неврологична дисфункция.[49] Тежките увреди са значима предпоставка за влошаване на качеството на живот, загуба на работа, стрес за околните,[50] неспособност за шофиране;[51] ограничения в социалния живот и трудовата активност. Тези фактори от своя страна водят до значително влошаване на състоянието и обостряне на симптоматиката на пациентите.[49]
Познавателни увреждания се установяват при 40 – 60% от болните от МС,[52] като най-нисък процент се наблюдава при пациенти лекувани в комунални условия, а най-висок при хоспитализирани. Понякога когнитивна дисфункция може да се появи още в началото на заболяването.[53] Вероятността за наличие на МС след първата когнитивна атака, но преди втората, е 50%.[54] Рядко се среща деменция, като се установява само при 5% от пациентите.[49]
Степента на тъканна атрофия добре корелира с когнитивната дисфункция и може да се използва за предвиждането ѝ. Неврофизиологичните последствия са в линейна корелация с подкоровата атрофия. Познавателните проблеми са резултат не само на тъканната увреда, но и на регенерацията и адаптивната функционална реорганизация.[50] Неврофизиологичните тестове са важни за определяне на обхвата на когнитивните нарушения. Рехабилитацията може да помогне за спиране или възстановяване от когнитивните увреждания, макар че изследванията в тази област са все още незадоволителни.[55] Инхибиторите на ацетилхолинестеразата са основните медикаменти при лечението на деменцията съпровождаща болестта на Алцхаймер, като вероятно имат потенциал за лечението на когнитивните разстройства. Установено е, че са ефективни при проведените предварителни клинични изпитвания.[55]
Емоционални[редактиране | редактиране на кода]
Емоционалните симптоми често съпътстват заболяването, като е прието, че те са последствие както на инвалидизацията на пациентите, така и на увреждания на специфични области от ЦНС отговорни за емоциите.
Депресията е най-често срещаното невропсихично състояние. Перманентна депресия се установява при 40 – 50% и 12-месечна при около 20% като това са стойности типични за болни от МС и са значително по-високи от средните за популацията, както и от тези на хора страдащи от други хронични заболявания.[56][57] Изследвания чрез образна диагностика установяват известна корелация между депресията и лезиите в определени области на мозъка, като е установена връзка с невропатологията в левия преден слепоочно-теменен регион.[58]
Често срещани са и агресия, тревожност, фрустрация, отчаяние. Реална опасност за пациентите представлява възможността за самоубийство, което е и причината за смъртта на 15% от страдащите от множествена склероза.[59]
Прострация[редактиране | редактиране на кода]
Прострацията е често срещата и една от причините за инвалидизация при МС, като същевременно е в тясна връзка с депресивната симптоматика.[60] При редукция на депресията прострацията също намалява, като е препоръчително пациентите да бъдат извадени от депресията преди да се започнат други терапевтични мероприятия.[61] Също така други фактори като лош сън, хронична болка, еднообразна храна и дори някои медикаменти могат да спомогнат за засилване на прострацията.[62] Съществуват различни медикаменти за лечение на прострацията като амантадин[63][64] или пемолин;[65][66] както и енергощадящи физиологични интервенции.[67][68] Тази терапия обаче не е особено ефективна и прави прострацията трудна за контрол. Чрез използването на ядрен магнитен резонанс са установени специфични области от мозъка, имащи отношение към прострацията.[69]
Интернуклеарна офталмоплегия[редактиране | редактиране на кода]
Интернуклеарна офталмоплегия е разстройство на координираното насочване на погледа. Увреденото око изпитва затруднения при аддукцията (завъртане навътре, привеждане). Другото око се отклонява при връщането си чрез абдукция (завъртане навън), което води до диплопия; при екстремна абдукция, може да се наблюдава компенсаторен нистагъм при партниращото око. Диплопията е двойно виждане, докато при нистагмус има неволево трептене на погледа.
Интернуклеарна офталмоплегия се появява, когато МС засегне част от мозъчния ствол наречен Fasciculus longitudinalis medialis, която е отговорна за координацията на двете очи, като свързва отвеждащото ядро с окуломоторното ядро. Това води до неспособност на вътрешния прав мускул да се съкращава правилно и така очите не се движат синхронно.
За подобряване на симптомите могат да се използват различни медикаменти и компенсаторни механизми като призматични стъкла.[70][71][72][73] В някои случаи подходяща е и оперативна интервенция.[74]
Ограничения в подвижността[редактиране | редактиране на кода]
Ограниченията в подвижността са чести при пациенти с МС. За десет години от началото на заболяването една трета от пациентите достигат ниво 6 от Скалата за оценка на инвалидния статус (СОИС), изискващо едностранна помощ при ходене. За 30 години този процент достига 83 на 100 от болните. При пациентите с прогресивна форма на МС за 5 години СОИС достига ниво шест при половината от пациентите.[75]
Съществува широка област от увреждания при страдащите от МС, които самостоятелно или в комбинация въздействат върху баланса, функционалността и подвижността на болните. Тези увреждания включват прострация, мускулна слабост, хипертония, нарушен баланс, атаксия и тремор.[76]
Възпаление на очния нерв[редактиране | редактиране на кода]
До 50% от пациентите с МС претърпяват епизод с възпаление на очния нерв. Освен това през 20% от времето на развитие на болестта се наблюдава очен неврит. Наличието на лезии в бялото мозъчно вещество, видими с ЯМР, едновременно с наличието на очен неврит, е най-силният предвестник за развитие на клиничната диагноза множествена склероза. Почти половината от пациентите с очен неврит имат лезии в бялото мозъчно вещество, дължащи се на МС.
30% от пациентите развиват МС през следващите пет години независимо от наличието на лезии. Пациенти с нормален ЯМР профил все пак заболяват (16%), но рискът е значително по-малък в сравнение с пациентите имащи три или повече лезии (51%). От друга страна 44% от пациентите с каквито и да е лезии от демиелинизация не развиват МС през следващите 10 години.[77][78]
Възпалението на очния нерв е съпроводено от болка при движение на окото, следвана от замъглено зрение в част или в цялото зрително поле. Понякога може да има светкавички и отблясъци.[79] Възпалението на оптичния нерв води до загуба на зрението най-често чрез оток и разрушаване на миелиновата обвивка, покриваща Nervus opticus.
Замъгленото зрение обикновено отшумява в рамките на десетина седмици, но често пациентите остават с намалено цветно зрение, особено за червено.
Системното лечение с кортикостероиди може да ускори възстановяването на очния нерв, предотвратявайки пълната загуба на зрение и забавяйки развитието на другите симптоми.
Болка[редактиране | редактиране на кода]
Болката е обичаен симптом при МС срещащ се при 55% от пациентите през някои етапи от развитието на болестта, като честотата нараства с напредване на заболяването.[80] Болката е силна и пречеща и има пагубен ефект върху качеството на живот и менталното здраве на болните.[81] Обикновено се появява при наличието на лезии на възходящите и низходящите пътища, пренасящи сигналите за болка.[72] Най-често се съобщава за главоболие (40%), дизестезна болка на крайниците (19%), болки в гърба (17%) и болезнени спазми (11%).[82] Острата болка се дължи на възпаление на очния нерв, невралгия на троичния нерв, Лермитови симптоми или дизестезия.[83] Подострата болка е вторична при МС и може да е последствие от прекарването продължително време в една поза, задържане на урина или инфектирани кожни язвички. Хроничната болка е често срещана и по-трудна за лечение.
Невралгия на троичния нерв[редактиране | редактиране на кода]
Невралгия на троичния нерв е разстройство в троичния нерв (N. trigeminus), което води до епизоди на интензивна болка в очите, устните, скалпа, челото, челюстта, като засяга около 1 – 2% от пациентите.[84][85] Епизодът на болка се появява внезапно, като пациентите описват как части от лицето им стават толкова чувствителни, че всяко докосване и дори движение на въздуха около тях води до болка. Обикновено се лекува успешно с антиконвулсанти като карбамазепин[86] или фенитоин,[87] макар че и други като габапентил[88] също могат да бъдат използвани.[89] Когато медикаментите не са ефективни, може да се прибегне до хирургична намеса. Извършени са експерименти чрез глицеролова ризотомия (оперативно инжектиране на глицерол в нерва),[90] макар че има спор около позитивите и възможните рискове за пациентите при подобна интервенция.[91][92]
Лермитови симптоми[редактиране | редактиране на кода]
Лермитови симптоми са чувство на „мравучкане“ протичащо надолу по гърба, като достига крайниците. Получава се при навеждане на главата напред. Тези признаци предполагат наличието на лезии в задните колони на шийния дял на продълговатия мозък, значително корелиращи с шийни аномалии при ЯМР.[93] Между 25 и 40% от пациентите с МС имат Лермитови симптоми по време на развитие на болестта.[94][95][96]
Дизестезия[редактиране | редактиране на кода]
Дизестезия е неприятно усещане породено от обикновени стимули. Ненормалната сензитивност се предизвиква от лезии в периферните или централните пътища и се описва като болезнени и неприятни чувства като изгаряне, мокрота, сърбеж, електрошок или убождане. Дизестезията, както и Лермитовите симптоми, обикновено се повлияват благотворно при лечение с карбамазепин, хлоразепам или амитриптилин.[97][98][99]
Сексуални смущения[редактиране | редактиране на кода]
Сексуалните смущения са сред многото симптоми проявяващи се при хора с диагноза МС. Сексуалните смущения при мъжете се изразяват в еректилни и еякулационни нарушения. Разпространението им сред мъжете с МС варира от 75 до 91%.[100] Сексуалните нарушения може да се дължат на промяна в рефлекса на еякулация, резултат от неврологичното състояние при множествена склероза.[101]
Спастичност[редактиране | редактиране на кода]
Спастичността се характеризира с нарастваща скованост и забавяне на движенията на крайниците и затруднения при заемане на определени пози. Наблюдават се и слабост при волевите мускулни движения, както и болезнени спазми на крайниците.[62] Физиотерапията може да помогне за намаляване на спастичността на мускулите и избягване на развитието на контрактури чрез пасивно разтягане.[102] Има доказателства, макар и ограничени, за клиничен ефект на екстракти от тетрахидроканабинол и канабидиол,[103] баклофен,[104] дантролен,[105] диазепам[106] и тиназидин.[107][108][109] При усложнени случаи се използват интратекални инжекции с баклофен.[110]
Трансверзален миелит[редактиране | редактиране на кода]
Трансверзалният миелит е патологичен процес на възпаление на гръбначния мозък.[111] Някои от пациентите с МС бързо развиват симптоматика с мускулна вкочаненост, слабост, ректална и пикочна дисфункция и/или загуба на мускулната функция, обикновено в долната част на тялото. Това състояние е следствие от атаката на МС върху гръбначния мозък. Симптомите се проявяват от мястото (нивото) на засягане по протежение надолу по гръбначния мозък.
Прогнозата не е особено благоприятна и рядко се достига до пълно възстановяване. Възстановяването от трансверзален миелит обикновено започва от две до дванадесет седмици след развитието му и може да продължи до две години. Приблизително 80% от пациентите не успяват да се възстановят напълно и остават с частични увреждания.[112]
Тремор и атаксия[редактиране | редактиране на кода]
Треморът и атаксията са често срещани при пациентите с МС, с честота от порядъка на 25 до 60%. Тези симптоми са силно смущаващи и затрудняващи дейността на пациентите, като в същото време почти не се подават на контрол и лечение.[113] Трудно е да бъде определен произходът на тремора при МС, но най-вероятно се дължи на комбинация от различни фактори като увреждане на връзките в малкия мозък, мускулната слабост, спастичност и други.
Много и различни медикаменти са изпробвани за лечение на тремора, но успехът е частичен и незадоволителен. Съобщава се за няколко медикамента, чрез които се постига известно облекчение на симптомите. Сред тях са: изониазид,[114][115][116][117] карбамазепин,[86] пропранолол,[118][119][120] глутетимид,[121] като публикуваните доказателства за успешно лечение са ограничени.[122] Физиотерапията не помага за лечение на тремора и атаксията, но употребата на ортопедични пособия може да помогне в известна степен. Като пример може да се посочи употребата на накитници с тежести, които придават инерция на движението и редуцират тремора.[123]
При липса на успех при консервативните начини на лечение, пациентите могат да бъдат подложени на хирургическа интервенция на таламуса. Тази интервенция може да бъде таламотомия (отстраняване на част от таламуса) или имплантирането на таламичен стимулатор. Усложненията и влошаването на атаксията, дизартрията или хемипарезата са нерядко срещани (30% при таламотомия и 10% при дълбока мозъчна стимулация).[124]
Диагностициране[редактиране | редактиране на кода]

Множествената склероза е трудно за диагностициране заболяване, поради голямото сходство на признаците и симптомите ѝ с тези на други клинични състояния.[1][125] Създадени са критерии за диагностициране, с които процесът да бъде ускорен и улеснен, особено в началните етапи от протичането на болестта.[1] В ретроспективен план популярни са били критериите на Шумахер и критериите на Позер.[126]
Понастоящем се използват критериите на Макдоналд, които се фокусират върху установяването на клинични, лабораторни и радиологични данни за демиелинизация, бидейки неинвазивен метод за диагностициране. Някои специалисти отстояват мнението, че МС може да бъде доказана еднозначно само след аутопсия или понякога биопсия, където характерните за МС лезии могат да бъдат детектирани чрез хистологични техники.[1][127][128]
Клиничните данни сами по себе си могат да бъдат достатъчни за поставяне на диагноза МС, ако потърпевшите са имали епизоди със самостоятелни неврологични симптоми характерни за МС.[127] Когато хората потърсят медицинска помощ още след първата атака, специализирани тестове могат да ускорят и улеснят поставянето на акуратната диагноза. Най-често използваните методики за диагноза са невровизуализация, анализ на ликвор и индукционен потенциал. Чрез ЯМР могат да се видят зоните на демиелиниация (лезии) в главния и гръбначния мозък. Чрез интравенозно внасяне на гадолиний се визуализират активните плаки, а при елиминирането му се установяват и старите лезии, които нямат отношение към симптомите, проявени при изследването.[127][129] Изследването на ликвора, взет чрез лумбална пункция, може да индикира наличието на хронично възпаление в централната нервна система. Ликворът се изследва чрез електрофореза за наличие на олигоклонални клъстери от IgG, които са маркер за възпалителен процес и се откриват при 75 – 85% от пациентите с МС.[127][130] Нервната система на човек, покосен от МС, реагира по-слабо при стимулация на оптичния нерв и сетивните нерви, поради демиелинизацията на нервните пътища. Мозъчните реакции могат да се изпитат чрез измерване на визуалния индукционен потенциал и сензиторния индукционен потенциал.[131]
Прогноза[редактиране | редактиране на кода]

Прогнозата (очакваното бъдещо развитие на болестта) при засегнати от МС зависи от формата на заболяването, както и от пола, възрастта, началните симптоми и степента на инвалидизация на пациентите.[7] Болестта се развива и напредва в продължение на десетилетия, като средната продължителност на живот след заболяване е 30 години.[1]
Женски пол, пристъпно-ремитентна форма, възпаление на очния нерв или сензорни симптоми в началото, малко на брой рецидиви през началните години и ранна възраст на заболяване са свързани с по-благоприятна прогноза.[7][132]
Очакваната продължителност на живота при хора с МС е с 5 до 10 години по-ниска от тази при здравите.[1] Почти 40% от пациентите достигат 70 години.[132] Въпреки това две трети от причините за смърт при пациентите са свързани директно с последствия от болестта.[1] Самоубийствата са по-силно застъпени на фона на общата популация, а усложненията и инфекциите са особено рискови при по-засегнатите пациенти.[1]
Макар че повечето болни са загубили способността си да ходят при терминалната фаза, 90% са все още способни на самостоятелно придвижване десет години след като са покосени и 75% – след 15 години.[132][133]
Лечение[редактиране | редактиране на кода]
Въпреки че все още не е открит лек срещу множествената склероза, няколко вида терапии се ползват с доказан успех. Основните цели на тези терапии са да възстановят компрометираните след атака функции, да предотвратят нови атаки и да предпазят от инвалидизация потърпевшите. Както много други медикаменти, така и тези, използвани при лечението на МС, имат редица нежелани странични ефекти. Някои пациенти прибягват към помощта на алтернативната медицина, но за тези случаи липсват сериозни поддържащи научни изследвания.
| Генерика | Източник | |
|---|---|---|
| Основна терапия | ||
| Интерферон | [134][135][136][137] | |
| Глатирамер ацетат | [138][139][140][141] | |
| Алтернативна терапия (въз основа на противопоказания за лечение) | ||
| Азатиоприн | [142] | |
| Имуноглобулин | [143] | |
| Ескалационна терапия | ||
| Натализумаб | [144] | |
| Митоксантрон | [145] | |
| Циклофосфамид | [146] | |
| Циклоспорин | [147] | |
| Метотрексат | [148] | |
| Дексаметазон | [149][150][151][152] | |
| Триамцинолон ацетонид | [153][154][155][156] | |
| В клинично изпитване | ||
| Терифлуномид | [157][158][159][160] | |
| Алемтузумаб | [161][162] | |
| Даклизумаб | [163] | |
| MBP8298 | [164] | |
| Ритуксимаб | [165] | |
| BHT-3009 | [166] | |
| Кладрибин | [167] | |
| BG-12 | [168] | |
| Естриол | [169] | |
| FTY720 | [170][171] | |
| Лаквинимод | [172][173][174][175] | |
| Миноциклин | [176] | |
| Статин | [177] | |
| Темсиролимус | [178] | |
| Дирукотид | [179] | |
Остри атаки[редактиране | редактиране на кода]
При обостряне на симптоматиката, рутинна процедура е интравенозното прилагането на високи дози кортикостероиди, като метилпреднизолон, за справяне с рецидива.[1] Въпреки ефективността за облекчаване на симптомите в краткосрочен план кортикостероидното лечение не указва значимо влияние за дългосрочното възстановяване.[180] Интравенозното и прилагането per os са еднакво ефикасни.[181] За преодоляване на последствията от рецидиви, които не се повлияват от кортикостероидната терапия, може да се прибегне до плазмафереза.[1]
Потискащо заболяването лечение[редактиране | редактиране на кода]
През 2010 г. в САЩ, от 2011 г. и в Европа е одобрен за лечение на МС fingolimod, имуномодулатор извлечен от гъбата Isaria sinclairii.
От 2009 г. са одобрени пет потискащи заболяването лечения от регулаторните агенции на някои държави (предимно Северна Америка и Европа). Първите два са интерферон beta-1a и интерферон beta-1b. Третият медикамент е глатирамер ацетат, нестероиден, неинтерферонен имуномодулатор. Четвъртият – митоксантрон, е имуносупресор, използван също и при химиотерапия за лечение на рак. Петият е хуманизирано моноклоналното антитяло natalizumab срещу адхезивната молекула α4-интегрин.[1] Интерфероните и глатирамер ацетатът се прилагат чрез многократни инжекции: веднъж дневно за глатирамер ацетат и веднъж седмично, но мускулно, за интерферон beta-1b. Natalizumab и митоксантрон се прилагат венозно на месечен интервал.
И петте медикамента имат умерена ефективност при потискане на честотата на атаките при пристъпно-ремитентната форма, като капацитетът на интерфероните и глатирамер ацетата е по-спорен. Все още липсват проучвания за дългосрочната им ефективност.[1][182] Сравнението между имуномодулаторите (без митоксантрон) показва, че най-ефективен е натализумаб както в контекста на редуциране на честотата на рецидивите, така и в забавянето на развитието на болестта.[183] Възможно е митоксантронът да е най-ефикасен от всички, но той не е разглеждан като вариант при дългосрочна терапия, заради ограничаващи употребата му странични ефекти.[1][182] Най-ранната клинична проява на пристъпно-ремитентна множествена склероза е клинично изолираният синдром (clinically isolated syndrome, CIS). Прилагането на интерферони по време на началната атака намалява вероятността пациентът да развие МС.[1]
Лечението на прогресивната форма е по-затрудняващо от това на пристъпно-ремитентната МС. Митоксантронът показва положителен ефект при пациенти с вторично прогресивна и пристъпно-прогресивна форма. Умерено ефективен е при редуцирането на рецидивите в краткосрочен план, както и при забавянето на прогреса на заболяването.[184] Не е открито лечение, което да повлиява съществено първично-прогресивната форма на МС.[185]
Както повечето медикаменти, така и тези имат редица странични ефекти. Един от най-често срещаните е сърбеж в зоната на поставяне на инжекциите при глатирамер ацетат и интерферон. С времето се образува видима вдлъбнатина на мястото на поставяне, дължаща се на локалното разрушаване на мастната тъкан, липоатрофия. Интерфероните предизвикват появата на симптоми подобни на грипа.[186] Някои пациенти, лекувани с глатирамер, получават реакции след инжектирането като зачервяване, стягане в гърдите, сърцебиене, задух, тревожност, които обикновено отшумяват в рамките на половин час.[187] По-опасни, но много по-рядко срещани са увреждане на черния дроб от интерфероните,[188] кардиотоксичност, безплодие и остра миелоидна левкемия митоксантрон,[1][182] и предполагаема връзка между натализумаб и някои случаи на прогресивна мултифокална левкоенцефалопатия.[1]
Справяне с ефектите на МС[редактиране | редактиране на кода]
Потискащото заболяването лечение забавя развитието на болестта, но не го спира. С напредване на множествената склероза, симптоматиката са увеличава и обостря. Болестта е съпроводена от многообразни симптоми и функционални дефицити, които водят до редица прогресиращи увреждания и инвалидизация. Затова справянето с тези дефицити е много важно. Медикаментозната терапия, както и неврорехабилитацията, облекчават бремето на някои симптоми, но не повлияват напредването на болестта.[1][189] Някои симптоми като инконтиненция и спастичност се повлияват добре от медикаментите, много други обаче са по-трудни за контролиране.[1] Както при другите пациенти с неврологични увреждания, мултидисциплинарният подход е ключов за подобряването на качеството на живота. Трудно обаче се определя „ударната група“ от специалисти, защото пациентите с МС имат нужда от почти всички видове медицинска помощ едновременно.[1] Мултидисциплинарните програми за рехабилитация повишават активността и съучастието на пациентите, но не повлияват нивото на увреждане.[190]
В ретроспективен план болни от МС са съветвани да ограничават физическата натовареност поради риск от влошаване на симптомите.[191] Под контрола на физиотерапевт физическата активност е безопасна и има доказано благотворен ефект върху пациентите с МС.[192] Научни изследвания потвърждават ролята при възстановяването при физическа активност и подобряване мускулната сила,[193] подвижността,[193] психическото състояние,[194] чревното здраве,[195] общото състояние и качеството на живот.[193] Все пак, особено важно е пациентът да не се преуморява и да не прегрява по време на тренировките. Физиотерапевтите се нуждаят от експертна оценка на състоянието, за да направят подходяща рехабилитационна програма. В зависимост от пациента упражненията може да включват тренировки за издръжливост,[196] ходене, плуване, йога, тай чи и други.[195] Назначаването на подходяща и безопасна програма трябва да е внимателно подбрана за всеки пациент индивидуално, като са взети предвид всички противопоказания и предпазни мерки.[192]
Алтернативно лечение[редактиране | редактиране на кода]
Както при повечето хронични заболявания, пациентите се обръщат за помощ към алтернативната медицина, която често не е подплатена с клинични и научни аргументи.[197] Примери: диета на Суанк,[198] билколечение (включително и употребата на медицински канабис),[199] хипербарно оксигениране[200] и самозаразяване с анкилостома (известно като хелминтна терапия).[201]
Множествена склероза в България[редактиране | редактиране на кода]
Като представители на европеидната раса и живеещи в умерения климатичен пояс гражданите на България попадат в една от най-уязвимите групи.[1] По официални данни от 1984 г. броят на болните от МС е 4000 души.[202] Оттогава насам не се води точна статистика за болните в България. По неофициални данни от различните регионални болнични регистри засегнатите от МС са около 7000 – 8000.[202] Заболеваемостта се оценява 1,03 от 100 000 население. Средно на година се установяват по 80 нови случая.[203]
Специализирани центрове за рехабилитация и лечение на МС в България няма. Ползват се различни такива според клинична пътека: общински, санаториални по НОИ и други. По отношение на нормативна уредба, гарантираща правата на труд на хора с МС, то това би следвало да бъде Наредба № 5 на МЗ от 20.02.1987 г. за болестите, при които работниците, боледуващи от тях, имат особена закрила съгласно чл. 333, ал. 1 от Кодекса на труда, в която обаче МС все още не е включена, както и Наредба за определяне на видовете работи, за които се установява намалено работно време.[204]
Към началото на 2013 г. Министерството на здравеопазването е направило проект за промяна на Наредба № 5, в която множествената склероза е включена като диагноза със защита от уволнение. Предстои проектът на документа да се разгледа на заседание на Тристранния съвет към Министерски съвет съвместно с профсъюзи и работодателски организации. След това да бъде внесен за гласуване на заседание на Министерския съвет.
Историческа справка[редактиране | редактиране на кода]

Френският невролог Жан Шарко (1825 – 1893) е първият, който разпознава множествената склероза като отделно заболяване през 1868 г.[205] Осланяйки се на предишни съобщения, както и на собствените си клинични и физиологични наблюдения, Шарко нарекъл новата болест sclerose en plaques. Трите симптома на МС известни днес като триадата на Шарко са нистагмус, тремор и телеграфна реч, макар че те съвсем не са уникални за МС. Шарко забелязва и промените в когнитивните способности на пациентите си, като ги описва като „със значително отслабена памет“ и „бавно схващащи“.[3]
Още преди Шарко, Роберт Карсуел (1793 – 1857), британски професор по патология и Жан Крьовел (1791 – 1873), френски професор по патоанатомия, са описали и илюстрирали много от клиничните особености на болестта, но не успяват да я идентифицират като отделно заболяване.[205] Шарко описва уврежданията, които установява като „забележими лезии по гръбначния мозък придружени от атрофия“.[1] През 1863 г. швейцарският патолог Георг Едуард Риндфлайш (1836 – 1908) наблюдава под микроскоп възпалителни лезии, разпръснати около кръвоносните съдове.[206][207]
След откритието на Шарко други учени, Йожен Девич (1858 – 1930), Жозеф Бало (1895 – 1979), Пол Фердинанд Шилдер (1886 – 1940) и Ото Марбург (1874 – 1948) описват различни форми на заболяването. През целия 20 век теоретичните познания за етимологията и патогенезата на МС се развиват и обогатяват, но едва през деветдесетте започва да се появява ефикасно лечение.[1]
Световен ден на множествената склероза[редактиране | редактиране на кода]
Световният ден на множествената склероза е инициатива на Международната Федерация по множествена склероза и нейните регионални МС-общества по държави. Световният МС ден е създаден, за да популяризира проблемите съпътстващи множествената склероза, ролята на МС обществата и глобалното МС движение. За първи път се отбелязва през 2009 г., като оттогава се провежда ежегодно през последната сряда на месец май.[208]
Бележки[редактиране | редактиране на кода]
- ↑ Неоползотворените години са годините преживени след инвалидизация плюс годините, които не достигат до средната продължителност на живот
Източници[редактиране | редактиране на кода]
- ↑ а б в г д е ж з и к л м н о п р с т у ф х ц ч ш щ ю я аа аб ав аг ад ае аж аз аи ак ал ам ан ао ап ар ас ат ау аф ах ац Compston A, Coles A. Multiple sclerosis // Lancet 372 (9648). Октомври 2008. DOI:10.1016/S0140-6736(08)61620-7. с. 1502 – 17.
- ↑ а б Rosati G. The prevalence of multiple sclerosis in the world: an update // Neurol. Sci. 22 (2). Април 2001. DOI:10.1007/s100720170011. с. 117 – 39.
- ↑ а б в Clanet M. Jean-Martin Charcot. 1825 to 1893 (PDF) // Int MS J 15 (2). Юни 2008. с. 59 – 61. Архивиран от оригинала на 2019-03-30. Посетен на 2011-07-26.
* Charcot, J. Histologie de la sclerose en plaques // Gazette des hopitaux, Paris 41. 1868. с. 554 – 5. - ↑ а б в г д е ж з и к л м н о п р с Compston A, Coles A. Multiple sclerosis // Lancet 359 (9313). Април 2002. DOI:10.1016/S0140-6736(02)08220-X. с. 1221 – 31.
- ↑ а б в г д е Ascherio A, Munger KL. Environmental risk factors for multiple sclerosis. Part I: the role of infection // Ann. Neurol. 61 (4). Април 2007. DOI:10.1002/ana.21117. с. 288 – 99.
- ↑ а б в г д е ж Lublin FD, Reingold SC. Defining the clinical course of multiple sclerosis: results of an international survey. National Multiple Sclerosis Society (USA) Advisory Committee on Clinical Trials of New Agents in Multiple Sclerosis // Neurology 46 (4). Април 1996. с. 907 – 11.
- ↑ а б в Weinshenker BG. Natural history of multiple sclerosis // Ann. Neurol. 36 (Suppl). 1994. DOI:10.1002/ana.410360704. с. S6–11.
- ↑ Pittock SJ, Rodriguez M. Benign multiple sclerosis: a distinct clinical entity with therapeutic implications // Curr. Top. Microbiol. Immunol. 318. 2008. DOI:10.1007/978-3-540-73677-6_1. с. 1 – 17.
- ↑ а б Miller D, Barkhof F, Montalban X, Thompson A, Filippi M. Clinically isolated syndromes suggestive of multiple sclerosis, part I: natural history, pathogenesis, diagnosis, and prognosis // Lancet Neurol 4 (5). Май 2005. DOI:10.1016/S1474-4422(05)70071-5. с. 281 – 8.
- ↑ Rovaris M, Confavreux C, Furlan R, Kappos L, Comi G, Filippi M. Secondary progressive multiple sclerosis: current knowledge and future challenges // Lancet Neurol 5 (4). Април 2006. DOI:10.1016/S1474-4422(06)70410-0. с. 343 – 54.
- ↑ а б в Miller DH, Leary SM. Primary-progressive multiple sclerosis // Lancet Neurol 6 (10). Октомври 2007. DOI:10.1016/S1474-4422(07)70243-0. с. 903 – 12.
- ↑ Stadelmann C, Brück W. Lessons from the neuropathology of atypical forms of multiple sclerosis // Neurol. Sci. 25 (Suppl 4). Ноември 2004. с. S319–22.
- ↑ а б в Kurtzke JF. Epidemiologic evidence for multiple sclerosis as an infection // Clin. Microbiol. Rev. 6 (4). Октомври 1993. с. 382 – 427.
- ↑ а б в г д е ж з и Marrie RA. Environmental risk factors in multiple sclerosis aetiology // Lancet Neurol 3 (12). Декември 2004. DOI:10.1016/S1474-4422(04)00933-0. с. 709 – 18.
- ↑ а б в г д Ascherio A, Munger KL. Environmental risk factors for multiple sclerosis. Part II: Noninfectious factors // Ann. Neurol. 61 (6). Юни 2007. DOI:10.1002/ana.21141. с. 504 – 13.
- ↑ а б в Alonso A, Hernán MA. Temporal trends in the incidence of multiple sclerosis: a systematic review // Neurology 71 (2). Юли 2008. DOI:10.1212/01.wnl.0000316802.35974.34. с. 129 – 35.
- ↑ Kulie T, Groff A, Redmer J, Hounshell J, Schrager S. Vitamin D: an evidence-based review // J Am Board Fam Med 22 (6). 2009. DOI:10.3122/jabfm.2009.06.090037. с. 698 – 706.
- ↑ Minagar A, Jy W, Jimenez JJ, Alexander JS. Multiple sclerosis as a vascular disease // Neurol Res. 28 (3). Април 2006. DOI:10.1179/016164106X98080. с. 230 – 5. Архивиран от оригинала на 2011-08-16. Посетен на 2011-07-26.
- ↑ Dyment DA, Ebers GC, Sadovnick AD. Genetics of multiple sclerosis // Lancet Neurol 3 (92). Февруари 2004. DOI:10.1016/S1474-4422(03)00663-X. с. 104 – 10.
- ↑ Who gets MS? // Multiple Sclerosis Trust, 30 декември 2009. Посетен на 18 април 2011.
- ↑ Ascherio A, Munger KL, Simon KC. Vitamin D and multiple sclerosis // Lancet Neurol 9 (6). Юни 2010. DOI:10.1016/S1474-4422(10)70086-7. с. 599 – 612.
- ↑ Mikaeloff et al.: Hepatitis B vaccination and the risk of childhood-onset multiple sclerosis. Arch Pediatr Adolesc Med. 2007 Dec;161(12):1176 – 1182. PMID 18056563
- ↑ DeStefano et al.: Vaccinations and risk of central nervous system demyelinating diseases in adults. Arch Neurol. 2003 Apr;60(4):504 – 9. PMID 12707063
- ↑ Mikaeloff et al.: Hepatitis B vaccine and risk of relapse after a first childhood episode of CNS inflammatory demyelination. Brain. 2007;130:1105 – 1110. PMID 17276994
- ↑ Zipp et al.: No increase in demyelinating diseases after hepatitis B vaccination.Nat Med. 1999;5(9):964 – 5. PMID 10470051
- ↑ Zamboni P. et al.: Chronic cerebrospinal venous insufficiency in patients with multiple sclerosis. J Neurol Neurosurg Psychiatry. 2009 April; 80(4): 392 – 399. PMID 19060024 Volltext
- ↑ Simka M.: Blood Brain Barrier Compromise with Endothelial Inflammation may Lead to Autoimmune Loss of Myelin during Multiple Sclerosis. Curr Neurovasc Res. 2009; 6(2): 132 – 139. ISSN – 2026 1567 – 2026 Abstract Архив на оригинала от 2010-07-07 в Wayback Machine.
- ↑ Ghadirian P, Jain M, Ducic S, Shatenstein B, Morisset R. Nutritional factors in the aetiology of multiple sclerosis: a case-control study in Montreal, Canada // Int J Epidemiol. 27 (5). 1998. с. 845 – 52. (primary source)
- ↑ Spitsin S, Koprowski H. Role of uric acid in multiple sclerosis // Curr. Top. Microbiol. Immunol. 318. 2008. DOI:10.1007/978-3-540-73677-6_13. с. 325 – 42.
- ↑ Gilden DH. Infectious causes of multiple sclerosis // The Lancet Neurology 4 (3). Март 2005. DOI:10.1016/S1474-4422(05)01017-3. с. 195 – 202.
- ↑ а б Chari DM. Remyelination in multiple sclerosis // Int. Rev. Neurobiol. 79. 2007. DOI:10.1016/S0074-7742(07)79026-8. с. 589 – 620.
- ↑ Pittock SJ, Lucchinetti CF. The pathology of MS: new insights and potential clinical applications // Neurologist 13 (2). Март 2007. DOI:10.1097/01.nrl.0000253065.31662.37. с. 45 – 56.
- ↑ Iglesias A, Bauer J, Litzenburger T, Schubart A, Linington C. T- and B-cell responses to myelin oligodendrocyte glycoprotein in experimental autoimmune encephalomyelitis and multiple sclerosis // Glia 36 (2). Ноември 2001. DOI:10.1002/glia.1111. с. 220 – 34.
- ↑ Kurtzke JF. Rating neurologic impairment in multiple sclerosis: an expanded disability status scale (EDSS) // Neurology 33 (11). 1983. с. 1444 – 52.
- ↑ Navarro S, Mondéjar-Marín B, Pedrosa-Guerrero A, Pérez-Molina I, Garrido-Robres J, Alvarez-Tejerina A. [Aphasia and parietal syndrome as the presenting symptoms of a demyelinating disease with pseudotumoral lesions] // Rev Neurol 41 (10). 2005. с. 601 – 3.
- ↑ Jongen P. Psychiatric onset of multiple sclerosis // J Neurol Sci 245 (1 – 2). 2006. DOI:10.1016/j.jns.2005.09.014. с. 59 – 62.
- ↑ Paty D, Studney D, Redekop K, Lublin F. MS COSTAR: a computerized patient record adapted for clinical research purposes. Ann Neurol 1994;36 Suppl:S134-5. PMID 8017875
- ↑ Hennessey A, Robertson NP, Swingler R, Compston DA. Urinary, faecal and sexual dysfunction in patients with multiple sclerosis // J. Neurol. 246 (11). 1999. DOI:10.1007/s004150050508. с. 1027 – 32.
- ↑ Burguera-Hernández JA. [Urinary alterations in multiple sclerosis] // Revista de neurologia 30 (10). 2000. с. 989 – 92. (Грешка в записа: Неразпознат езиков код
es; castilian) - ↑ Nour S, Svarer C, Kristensen JK, Paulson OB, Law I. Cerebral activation during micturition in normal men // Brain 123 (Pt 4) (4). 2000. DOI:10.1093/brain/123.4.781. с. 781 – 9.
- ↑ Ayuso-Peralta L, de Andrés C. [Symptomatic treatment of multiple sclerosis] // Revista de neurologia 35 (12). 2002. с. 1141 – 53. (Грешка в записа: Неразпознат езиков код
es; castilian) - ↑ Information from the USA National library of medicine on alfuzosin
- ↑ Information from the USA National library of medicine on trospium
- ↑ Information from the USA National library of medicine on flavoxate
- ↑ Bosma R, Wynia K, Havlíková E, De Keyser J, Middel B. Efficacy of desmopressin in patients with multiple sclerosis suffering from bladder dysfunction: a meta-analysis // Acta Neurol. Scand. 112 (1). 2005. DOI:10.1111/j.1600-0404.2005.00431.x. с. 1 – 5.
- ↑ Information from the USA National library of medicine on desmopressin
- ↑ Frances M Diro (2006) „Urological Management in Neurological Disease“
- ↑ Bobholz J, Rao S. Cognitive dysfunction in multiple sclerosis: a review of recent developments // Curr Opin Neurol 16 (3). 2003. DOI:10.1097/00019052-200306000-00006. с. 283 – 8.
- ↑ а б в Amato MP, Ponziani G, Siracusa G, Sorbi S. Cognitive dysfunction in early-onset multiple sclerosis: a reappraisal after 10 years // Arch. Neurol. 58 (10). Октомври 2001. DOI:10.1001/archneur.58.10.1602. с. 1602 – 6.
- ↑ а б Benedict RH, Carone DA, Bakshi R. Correlating brain atrophy with cognitive dysfunction, mood disturbances, and personality disorder in multiple sclerosis // J Neuroimaging 14 (3 Suppl). Юли 2004. DOI:10.1177/1051228404266267. с. 36S–45S.
- ↑ Shawaryn M, Schultheis M, Garay E, Deluca J. Assessing functional status: exploring the relationship between the multiple sclerosis functional composite and driving // Arch Phys Med Rehabil 83 (8). 2002. DOI:10.1053/apmr.2002.33730. с. 1123 – 9.
- ↑ Rao S, Leo G, Bernardin L, Unverzagt F. Cognitive dysfunction in multiple sclerosis. I. Frequency, patterns, and prediction // Neurology 41 (5). 1991. с. 685 – 91.
- ↑ Dujardin, K. и др. Attention impairment in recently diagnosed multiple sclerosis // Eur J Neurol 5 (1). 1998. DOI:10.1046/j.1468-1331.1998.510061.x. с. 61 – 66.
- ↑ Achiron A, Barak Y. Cognitive impairment in probable multiple sclerosis // J Neurol Neurosurg Psychiatry 74 (4). 2003. DOI:10.1136/jnnp.74.4.443. с. 443 – 6.
- ↑ а б Chiaravalloti ND, DeLuca J. Cognitive impairment in multiple sclerosis // Lancet neurol 7 (12). Dec 2008. DOI:10.1016/S1474-4422(08)70259-X. с. 1139 – 51.
- ↑ Sadovnick A, Remick R, Allen J, Swartz E, Yee I, Eisen K, Farquhar R, Hashimoto S, Hooge J, Kastrukoff L, Morrison W, Nelson J, Oger J, Paty D. Depression and multiple sclerosis // Neurology 46 (3). 1996. с. 628 – 32.
- ↑ Patten S, Beck C, Williams J, Barbui C, Metz L. Major depression in multiple sclerosis: a population-based perspective // Neurology 61 (11). 2003. с. 1524 – 7.
- ↑ Siegert R, Abernethy D. Depression in multiple sclerosis: a review // J. Neurol. Neurosurg. Psychiatr. 76 (4). 2005. DOI:10.1136/jnnp.2004.054635. с. 469 – 75.
- ↑ Sadovnick A, Eisen K, Ebers G, Paty D. Cause of death in patients attending multiple sclerosis clinics // Neurology 41 (8). 1991. с. 1193 – 6.
- ↑ Bakshi R. Fatigue associated with multiple sclerosis: diagnosis, impact and management // Mult. Scler. 9 (3). 2003. DOI:10.1191/1352458503ms904oa. с. 219 – 27.
- ↑ Mohr DC, Hart SL, Goldberg A. Effects of treatment for depression on fatigue in multiple sclerosis // Psychosomatic medicine 65 (4). 2003. DOI:10.1097/01.PSY.0000074757.11682.96. с. 542 – 7.
- ↑ а б The Royal College of Physicians. Multiple Sclerosis. National clinical guideline for diagnosis and management in primary and secondary care. Salisbury, Wiltshire, Sarum ColourView Group, 2004. ISBN 186016 182 0.Free full text(2004-08-13). Посетен на 1 октомври 2007.
- ↑ Pucci E, Branãs P, D'Amico R, Giuliani G, Solari A, Taus C. Amantadine for fatigue in multiple sclerosis // Cochrane database of systematic reviews (Online) (1). 2007. DOI:10.1002/14651858.CD002818.pub2. с. CD002818.
- ↑ Amantadine. US National Library of Medicine (Medline) (2003-04-01). Посетен на 7 октомври 2007.
- ↑ Weinshenker BG, Penman M, Bass B, Ebers GC, Rice GP. A double-blind, randomized, crossover trial of pemoline in fatigue associated with multiple sclerosis // Neurology 42 (8). 1992. с. 1468 – 71.
- ↑ Pemoline. US National Library of Medicine (Medline) (2006-01-01). Посетен на 7 октомври 2007.
- ↑ Mathiowetz VG, Finlayson ML, Matuska KM, Chen HY, Luo P. Randomized controlled trial of an energy conservation course for persons with multiple sclerosis // Mult. Scler. 11 (5). 2005. DOI:10.1191/1352458505ms1198oa. с. 592 – 601.
- ↑ Matuska K, Mathiowetz V, Finlayson M. Use and perceived effectiveness of energy conservation strategies for managing multiple sclerosis fatigue // The American Journal of Occupational Therapy 61 (1). 2007. с. 62 – 9.
- ↑ Sepulcre J, Masdeu J, Goñi J, et al. Fatigue in multiple sclerosis is associated with the disruption of frontal and parietal pathways // Mult. Scler. 15 (3). Ноември 2008. DOI:10.1177/1352458508098373. с. 337.
- ↑ Leigh RJ, Averbuch-Heller L, Tomsak RL, Remler BF, Yaniglos SS, Dell'Osso LF. Treatment of abnormal eye movements that impair vision: strategies based on current concepts of physiology and pharmacology // Ann. Neurol. 36 (2). 1994. DOI:10.1002/ana.410360204. с. 129 – 41.
- ↑ Starck M, Albrecht H, Pöllmann W, Straube A, Dieterich M. Drug therapy for acquired pendular nystagmus in multiple sclerosis // J. Neurol. 244 (1). 1997. DOI:10.1007/PL00007728. с. 9 – 16.
- ↑ а б Clanet MG, Brassat D. The management of multiple sclerosis patients // Curr. Opin. Neurol. 13 (3). 2000. DOI:10.1097/00019052-200006000-00005. с. 263 – 70.
- ↑ Menon GJ, Thaller VT. Therapeutic external ophthalmoplegia with bilateral retrobulbar botulinum toxin- an effective treatment for acquired nystagmus with oscillopsia // Eye (London, England) 16 (6). 2002. DOI:10.1038/sj.eye.6700167. с. 804 – 6.
- ↑ Jain S, Proudlock F, Constantinescu CS, Gottlob I. Combined pharmacologic and surgical approach to acquired nystagmus due to multiple sclerosis // Am. J. Ophthalmol. 134 (5). 2002. DOI:10.1016/S0002-9394(02)01629-X. с. 780 – 2.
- ↑ Weinshenker BG, Bass B, Rice GP, et al. The natural history of multiple sclerosis: a geographically based study. I. Clinical course and disability // Brain 112 (Pt 1). 1989. с. 133 – 46.
- ↑ Freeman JA. Improving mobility and functional independence in persons with multiple sclerosis // J. Neurol. 248 (4). 2001. DOI:10.1007/s004150170198. с. 255 – 9.
- ↑ Beck RW, Trobe JD. What we have learned from the Optic Neuritis Treatment Trial // Ophthalmology 102 (10). 1995. с. 1504 – 8.
- ↑ The 5-year risk of MS after optic neuritis: experience of the optic neuritis treatment trial. 1997 // Neurology 57 (12 Suppl 5). 2001. с. S36–45.
- ↑ Cervetto L, Demontis GC, Gargini C. Cellular mechanisms underlying the pharmacological induction of phosphenes // Br. J. Pharmacol. 150 (4). Февруари 2007. DOI:10.1038/sj.bjp.0706998. с. 383 – 90.
- ↑ Stenager E, Knudsen L, Jensen K. Acute and chronic pain syndromes in multiple sclerosis. A 5-year follow-up study // Italian journal of neurological sciences 16 (9). 1995. DOI:10.1007/BF02230913. с. 629 – 32.
- ↑ Archibald CJ, McGrath PJ, Ritvo PG, et al. Pain prevalence, severity and impact in a clinic sample of multiple sclerosis patients // Pain 58 (1). 1994. DOI:10.1016/0304-3959(94)90188-0. с. 89 – 93.
- ↑ Pöllmann W, Feneberg W, Erasmus LP. [Pain in multiple sclerosis—a still underestimated problem. The 1 year prevalence of pain syndromes, significance and quality of care of multiple sclerosis inpatients] // Der Nervenarzt 75 (2). 2004. DOI:10.1007/s00115-003-1656-5. S. 135 – 40. (на немски)
- ↑ Kerns RD, Kassirer M, Otis J. Pain in multiple sclerosis: a biopsychosocial perspective // Journal of rehabilitation research and development 39 (2). 2002. с. 225 – 32.
- ↑ Brisman R. Trigeminal neuralgia and multiple sclerosis // Arch. Neurol. 44 (4). 1987. с. 379 – 81.
- ↑ Bayer DB, Stenger TG. Trigeminal neuralgia: an overview // Oral Surg. Oral Med. Oral Pathol. 48 (5). 1979. DOI:10.1016/0030-4220(79)90064-1. с. 393 – 9.
- ↑ а б Information from the USA National library of medicine on carbamazepine
- ↑ Information from the USA National library of medicine on phenytoin
- ↑ Information from the USA National library of medicine on gabapentin
- ↑ Solaro C, Messmer Uccelli M, Uccelli A, Leandri M, Mancardi GL. Low-dose gabapentin combined with either lamotrigine or carbamazepine can be useful therapies for trigeminal neuralgia in multiple sclerosis // Eur. Neurol. 44 (1). 2000. DOI:10.1159/000008192. с. 45 – 8.
- ↑ Kondziolka D, Lunsford LD, Bissonette DJ. Long-term results after glycerol rhizotomy for multiple sclerosis-related trigeminal neuralgia // The Canadian journal of neurological sciences. Le journal canadien des sciences neurologiques 21 (2). 1994. с. 137 – 40.
- ↑ Athanasiou TC, Patel NK, Renowden SA, Coakham HB. Some patients with multiple sclerosis have neurovascular compression causing their trigeminal neuralgia and can be treated effectively with MVD: report of five cases // British journal of neurosurgery 19 (6). 2005. DOI:10.1080/02688690500495067. с. 463 – 8.
- ↑ Eldridge PR, Sinha AK, Javadpour M, Littlechild P, Varma TR. Microvascular decompression for trigeminal neuralgia in patients with multiple sclerosis // Stereotactic and functional neurosurgery 81 (1 – 4). 2003. DOI:10.1159/000075105. с. 57 – 64.
- ↑ Gutrecht JA, Zamani AA, Slagado ED. Anatomic-radiologic basis of Lhermitte's sign in multiple sclerosis // Arch. Neurol. 50 (8). 1993. с. 849 – 51.
- ↑ Al-Araji AH, Oger J. Reappraisal of Lhermitte's sign in multiple sclerosis // Mult. Scler. 11 (4). 2005. DOI:10.1191/1352458505ms1177oa. с. 398 – 402.
- ↑ Sandyk R, Dann LC. Resolution of Lhermitte's sign in multiple sclerosis by treatment with weak electromagnetic fields // Int. J. Neurosci. 81 (3 – 4). 1995. DOI:10.3109/00207459509004888. с. 215 – 24.
- ↑ Kanchandani R, Howe JG. Lhermitte's sign in multiple sclerosis: a clinical survey and review of the literature // J. Neurol. Neurosurg. Psychiatr. 45 (4). 1982. DOI:10.1136/jnnp.45.4.308. с. 308 – 12.
- ↑ Information from the USA National library of medicine on clonazepam
- ↑ Information from the USA National library of medicine on amitriptyline
- ↑ Moulin DE, Foley KM, Ebers GC. Pain syndromes in multiple sclerosis // Neurology 38 (12). 1988. с. 1830 – 4.
- ↑ O'Leary et al., 2007
- ↑ O'Leary, M., Heyman, R., Erickson, J., Chancellor, M.B.: Premature ejaculation and MS: A Review, Consortium of MS Centers, www.mscare.org, June 2007
- ↑ Cardini RG, Crippa AC, Cattaneo D. Update on multiple sclerosis rehabilitation // J. Neurovirol. 6 Suppl 2. 2000. с. S179–85.
- ↑ Lakhan SE, Rowland M. „Whole plant cannabis extracts in the treatment of spasticity in multiple sclerosis: a systematic review“. BMC Neurology. 2009;9(59). PMID 19961570.
- ↑ Baclofen oral. US National Library of Medicine (Medline) (2003-04-01). Посетен на 17 октомври 2007.
- ↑ Dantrolene oral. US National Library of Medicine (Medline) (2003-04-01). Посетен на 17 октомври 2007.
- ↑ Diazepam. US National Library of Medicine (Medline) (2005-07-01). Посетен на 17 октомври 2007.
- ↑ Tizanidine. US National Library of Medicine (Medline) (2005-07-01). Посетен на 17 октомври 2007.
- ↑ Beard S, Hunn A, Wight J. Treatments for spasticity and pain in multiple sclerosis: a systematic review // Health technology assessment (Winchester, England) 7 (40). 2003. с. iii, ix–x, 1 – 111.
- ↑ Paisley S, Beard S, Hunn A, Wight J. Clinical effectiveness of oral treatments for spasticity in multiple sclerosis: a systematic review // Mult. Scler. 8 (4). 2002. DOI:10.1191/1352458502ms795rr. с. 319 – 29.
- ↑ Becker WJ, Harris CJ, Long ML, Ablett DP, Klein GM, DeForge DA. Long-term intrathecal baclofen therapy in patients with intractable spasticity // The Canadian journal of neurological sciences. Le journal canadien des sciences neurologiques 22 (3). 1995. с. 208 – 17.
- ↑ Chamberlin SL, Narins B (eds.). The Gale Encyclopedia of Neurological Disorders. Detroit, Thomson Gale, 2005. ISBN 0-7876-9150-X. с. 1859 – 70.
- ↑ Transverse myelitis. Retrospective analysis of 33 cases, with differentiation of cases associated with multiple sclerosis and parainfectious events
- ↑ Koch M, Mostert J, Heersema D, De Keyser J. Tremor in multiple sclerosis // J. Neurol. 254 (2). 2007. DOI:10.1007/s00415-006-0296-7. с. 133 – 45.
- ↑ Bozek CB, Kastrukoff LF, Wright JM, Perry TL, Larsen TA. A controlled trial of isoniazid therapy for action tremor in multiple sclerosis // J. Neurol. 234 (1). 1987. DOI:10.1007/BF00314007. с. 36 – 9.
- ↑ Duquette P, Pleines J, du Souich P. Isoniazid for tremor in multiple sclerosis: a controlled trial // Neurology 35 (12). 1985. с. 1772 – 5.
- ↑ Hallett M, Lindsey JW, Adelstein BD, Riley PO. Controlled trial of isoniazid therapy for severe postural cerebellar tremor in multiple sclerosis // Neurology 35 (9). 1985. с. 1374 – 7.
- ↑ Information from the USA National library of medicine on Isoniazid [1]
- ↑ Koller WC. Pharmacologic trials in the treatment of cerebellar tremor // Arch. Neurol. 41 (3). 1984. с. 280 – 1.
- ↑ Sechi GP, Zuddas M, Piredda M, Agnetti V, Sau G, Piras ML, Tanca S, Rosati G. Treatment of cerebellar tremors with carbamazepine: a controlled trial with long-term follow-up // Neurology 39 (8). 1989. с. 1113 – 5.
- ↑ Information from the USA National library of medicine on propanolol
- ↑ Aisen ML, Holzer M, Rosen M, Dietz M, McDowell F. Glutethimide treatment of disabling action tremor in patients with multiple sclerosis and traumatic brain injury // Arch. Neurol. 48 (5). 1991. с. 513 – 5.
- ↑ Mills RJ, Yap L, Young CA. Treatment for ataxia in multiple sclerosis // Cochrane database of systematic reviews (Online) (1). 2007. DOI:10.1002/14651858.CD005029.pub2. с. CD005029.
- ↑ Aisen ML, Arnold A, Baiges I, Maxwell S, Rosen M. The effect of mechanical damping loads on disabling action tremor // Neurology 43 (7). 1993. с. 1346 – 50.
- ↑ Bittar RG, Hyam J, Nandi D, Wang S, Liu X, Joint C, Bain PG, Gregory R, Stein J, Aziz TZ. Thalamotomy versus thalamic stimulation for multiple sclerosis tremor // Journal of Clinical Neuroscience 12 (6). 2005. DOI:10.1016/j.jocn.2004.09.008. с. 638 – 42.
- ↑ Trojano M, Paolicelli D. The differential diagnosis of multiple sclerosis: classification and clinical features of relapsing and progressive neurological syndromes // Neurol. Sci. 22 (Suppl 2). Ноември 2001. DOI:10.1007/s100720100044. с. S98–102. Архивиран от оригинала на 2014-10-20. Посетен на 2011-07-27.
- ↑ Poser CM, Brinar VV. Diagnostic criteria for multiple sclerosis: an historical review // Clin Neurol Neurosurg 106 (3). Юни 2004. DOI:10.1016/j.clineuro.2004.02.004. с. 147 – 58.
- ↑ а б в г McDonald WI, Compston A, Edan G, et al. Recommended diagnostic criteria for multiple sclerosis: guidelines from the International Panel on the diagnosis of multiple sclerosis // Ann. Neurol. 50 (1). Юли 2001. DOI:10.1002/ana.1032. с. 121 – 7.
- ↑ Polman CH, Reingold SC, Edan G, et al. Diagnostic criteria for multiple sclerosis: 2005 revisions to the „McDonald Criteria“ // Ann. Neurol. 58 (6). Декември 2005. DOI:10.1002/ana.20703. с. 840 – 6.
- ↑ Rashid W, Miller DH. Recent advances in neuroimaging of multiple sclerosis // Semin Neurol 28 (1). Февруари 2008. DOI:10.1055/s-2007-1019127. с. 46 – 55.
- ↑ Link H, Huang YM. Oligoclonal bands in multiple sclerosis cerebrospinal fluid: an update on methodology and clinical usefulness // J. Neuroimmunol. 180 (1 – 2). Ноември 2006. DOI:10.1016/j.jneuroim.2006.07.006. с. 17 – 28.
- ↑ Gronseth GS, Ashman EJ. Practice parameter: the usefulness of evoked potentials in identifying clinically silent lesions in patients with suspected multiple sclerosis (an evidence-based review): Report of the Quality Standards Subcommittee of the American Academy of Neurology // Neurology 54 (9). Май 2000. с. 1720 – 5.
- ↑ а б в Phadke JG. Survival pattern and cause of death in patients with multiple sclerosis: results from an epidemiological survey in north east Scotland // J. Neurol. Neurosurg. Psychiatr. 50 (5). Май 1987. DOI:10.1136/jnnp.50.5.523. с. 523 – 31.
- ↑ Myhr KM, Riise T, Vedeler C, et al. Disability and prognosis in multiple sclerosis: demographic and clinical variables important for the ability to walk and awarding of disability pension // Mult. Scler. 7 (1). Февруари 2001. с. 59 – 65.
- ↑ {Rieckmann et al.: Rekombinante Beta-Interferone: Immunmodulatorische Therapie der schubförmigen Multiplen Sklerose. Deutsches Ärzteblatt 93, Ausgabe 46 vom 15. November 1996, Seite A-3022} Volltext
- ↑ {Filippini et al.: Interferons in relapsing remitting multiple sclerosis: a systematic review. Lancet. 2003;361(9357):545 – 52. PMID 12598138}
- ↑ European public assessment peport (EPAR), Betaferon[неработеща препратка]
- ↑ Galetta SL. The controlled high risk Avonex multiple sclerosis trial (CHAMPS Study) // J Neuroophthalmol 21 (4). 2001. с. 292 – 5.
- ↑ -{Munari et al.: Therapy with glatiramer acetate for multiple sclerosis. Cochrane Database Syst Rev. 2004;(1):CD004678. PMID 14974077}-
- ↑ The chemistry of the Copaxone drug // Архивиран от оригинала на 13 август 2006.
- ↑ www.mult-sclerosis.org
- ↑ Prescribing information for Copaxone (glatiramer acetate)
- ↑ Casetta et al.: Azathioprine for multiple sclerosis. Cochrane Database Syst Rev. 2007; CD003982. PMID 17943809
- ↑ Gray et al.:Intravenous immunoglobulins for multiple sclerosis. Cochrane Database Syst Rev. 2003; CD002936. PMID 14583956
- ↑ Polman et al.: A randomized, placebo-controlled trial of natalizumab for relapsing multiple sclerosis. N Engl J Med. 2006;354(9):899 – 910. PMID 16510744
- ↑ Martinelli Boneschi et al.: Mitoxantrone for multiple sclerosis. Cochrane Database Syst Rev. 2005; CD002127. PMID 16235298}-
- ↑ La Mantia et al.: Cyclophosphamide for multiple sclerosis. Cochrane Database Syst Rev. 2007; CD002819. PMID 17253481
- ↑ Rudge P, Koetsier JC, Mertin J, Mispelblom B.J.O., Van Walbeek HK, Jones RC, Harrison J, Robinson K, Mellein B, Poole T. Randomised double blind controlled trial of cyclosporin in multiple sclerosis // J Neurol Neurosurg Psychiatry 52. 1989. DOI:10.1136/jnnp.52.5.559. с. 559 – 565.
- ↑ Gray O, McDonnell GV, Forbes RB. Methotrexate for multiple sclerosis // Cochrane Reviews. 2004. DOI:10.1002/14651858.CD003208.pub2. Архивиран от оригинала на 2010-09-12.
- ↑ La Mantia L, Eoli M, Milanese C, Salmaggi A, Dufour A, Torri V. Double-blind trial of dexamethasone versus methylprednisolone in multiple sclerosis acute relapses // Eur Neurol 34 (4). 1994. с. 199 – 203.
- ↑ Schmelzeisen R, Frölich JC. Prevention of postoperative swelling and pain by dexamethasone after operative removal of impacted third molar teeth // European Journal of Clinical Pharmacology 44 (3). 2004. DOI:10.1007/BF00271371. с. 275 – 277.[неработеща препратка]
- ↑ Richard Nicholas and Jeremy Chataway. Corticosteroids versus each other[неработеща препратка]
- ↑ Nasal Administration of Dexamethasone for Multiple Sclerosis (MS) Treatment
- ↑ Diabetic Retinopathy Clinical Research Network. A randomized trial comparing intravitreal triamcinolone acetonide and focal/grid photocoagulation for diabetic macular edema // Ophthalmology 115 (9). 2008. с. 1447 – 9.
- ↑ Bonini-Filho MA, Jorge R, Barbosa JC, Calucci D, Cardillo JA, Costa RA. Intravitreal injection versus sub-Tenon's infusion of triamcinolone acetonide for refractory diabetic macular edema: a randomized clinical trial // Invest Ophthalmol Vis Sci 46 (10). 2005. с. 3845 – 9.
- ↑ Carsten Lukas; Barbara Bellenberg; Horst K. Hahn; Jan Rexilius; Robert Drescher; Kerstin Hellwig; Odo Köster; Sebastian Schimrigk. Benefit of Repetitive Intrathecal Triamcinolone Acetonide Therapy in Predominantly Spinal Multiple Sclerosis: Prediction by Upper Spinal Cord Atrophy // Ther Adv Neurol Disorders 2 (6). 2009. с. 349 – 355. Архивиран от оригинала на 2010-12-31.
- ↑ Hoffmann V, Schimrigk S, Islamova S, Hellwig K, Lukas C, Brune N, Pöhlau D, Przuntek H, Müller T. Efficacy and safety of repeated intrathecal triamcinolone acetonide application in progressive multiple sclerosis patients // J Neurol Sci. 211 (1). 2003. с. 81 – 4.
- ↑ ClinicalTrials.gov
- ↑ Magne D, Mézin F, Palmer G, Guerne PA. The active metabolite of leflunomide, A77 1726, increases proliferation of human synovial fibroblasts in presence of IL-1beta and TNF-alpha // Inflamm. Res. 55 (11). 2006. DOI:10.1007/s00011-006-5196-x. с. 469 – 75.
- ↑ Cohen JA. Emerging therapies for relapsing multiple sclerosis // Arch. Neurol. 66 (7). Юли 2009. DOI:10.1001/archneurol.2009.104. с. 821 – 8.
- ↑ Teriflunomide, Interferon adjunct reduces MS lesions
- ↑ Use for MS // Архивиран от оригинала на 2009-04-01. Посетен на Sept 2007.
- ↑ britainscienceresearch
- ↑ Rose JW, Burns JB, Bjorklund J, Klein J, Watt HE, Carlson NG. Daclizumab phase II trial in relapsing and remitting multiple sclerosis: MRI and clinical results // Neurology 69 (8). 2007. DOI:10.1212/01.wnl.0000267662.41734.1f. с. 785 – 789.
- ↑ Warren KG, Catz I, Ferenczi LZ, Krantz MJ. Intravenous synthetic peptide MBP8298 delayed disease progression in an HLA Class II-defined cohort of patients with progressive multiple sclerosis: results of a 24-month double-blind placebo-controlled clinical trial and 5 years of follow-up treatment. Eur J Neurol. 2006;13:887 – 95. PMID 16879301
- ↑ NEJM – B-Cell Depletion with Rituximab in Relapsing-Remitting Multiple Sclerosis
- ↑ -{Bayhill Therapeutics to Present Phase II Follow-up Data on BHT-3009 for Treatment of Multiple Sclerosis}- // Архивиран от оригинала на 2011-08-06. Посетен на 2012-01-01.
- ↑ Giovannoni G, et al., NEJM 2010
- ↑ Biogen Idec's oral compound BG-12 achieves development milestones in MS and RA
- ↑ Adeona Announces Additional $860,000 Grant For Oral Estriol Multiple Sclerosis Clinical Trial // Архивиран от оригинала на 2010-07-22. Посетен на 2012-01-01.
- ↑ Kappos L, Radue E-W, O'Connor P, Polman C, Hohlfield R, Calabresi P, Selmaj K, Agoropoulou C, Leyk M, Zhang-Auberson L, Burtin P for the FREEDOMS Study Group. A placebo-controlled trial of oral fingolimod in relapsing multiple sclerosis // New England Journal of Medicine 362 (5). 2010. DOI:10.1056/NEJMoa0909494. с. epub ahead of print.
- ↑ Efficacy and Safety of Fingolimod in Patients With Relapsing-Remitting Multiple Sclerosis. // ClinicalTrials.gov.
- ↑ Tan IL, Lycklama à Nijeholt GJ, Polman CH et al. Linomide in the treatment of multiple sclerosis: MRI results from prematurely terminated phase-III trials // Mult Scler 6 (2). Април 2000. с. 99 – 104.
- ↑ Comi G, Pulizzi A, Rovaris M, et al. Effect of laquinimod on MRI-monitored disease activity in patients with relapsing-remitting multiple sclerosis: a multicentre, randomised, double-blind, placebo-controlled phase IIb study // Lancet 371 (9630). Юни 2008. DOI:10.1016/S0140-6736(08)60918-6. с. 2085 – 92.
- ↑ Polman C, Barkhof F, Sandberg-Wollheim M et al. Treatment with laquinimod reduces development of active MRI lesions in relapsing MS // Neurology 64 (6). Март 2005. DOI:10.1212/01.WNL.0000154520.48391.69. с. 987 – 91.
- ↑ Keegan BM, Weinshenker BG. Laquinimod, a new oral drug for multiple sclerosis // Lancet 371 (9630). Юни 2008. DOI:10.1016/S0140-6736(08)60894-6. с. 2059 – 60.
- ↑ Minocycline is proposed as an add-on therapy to improve the efficacy of glatiramer acetate (Copaxone)
- ↑ Statin Drugs May Help Treat MS
- ↑ Temsirolimus Reduces Rate of Brain Atrophy in Patients With Relapsing-Remitting MS: Presented at ECTRIMS[неработеща препратка]
- ↑ BioMS multiple sclerosis drug gets FDA fast track
- ↑ The Royal College of Physicians. Multiple Sclerosis. National clinical guideline for diagnosis and management in primary and secondary care. Salisbury, Wiltshire, Sarum ColourView Group, 2004. ISBN 1-86016-182-0. с. 54 – 57. Посетен на 7 януари 2010.
- ↑ Burton JM, O'Connor PW, Hohol M, Beyene J. Oral versus intravenous steroids for treatment of relapses in multiple sclerosis // Cochrane Database Syst Rev (3). 2009. DOI:10.1002/14651858.CD006921.pub2. с. CD006921.
- ↑ а б в Comi G. Treatment of multiple sclerosis: role of natalizumab // Neurol. Sci. Suppl 2 (S2). Октомври 2009. DOI:10.1007/s10072-009-0147-2. с. S155–8.
- ↑ Johnson KP. Control of multiple sclerosis relapses with immunomodulating agents // J. Neurol. Sci. 256 (Suppl 1). 2007. DOI:10.1016/j.jns.2007.01.060. с. S23–8.
- ↑ Martinelli Boneschi F, Rovaris M, Capra R, Comi G. Mitoxantrone for multiple sclerosis // Cochrane database of systematic reviews (Online) (4). 2005. DOI:10.1002/14651858.CD002127.pub2. с. CD002127.
- ↑ Leary SM, Thompson AJ. Primary progressive multiple sclerosis: current and future treatment options // CNS drugs 19 (5). 2005. DOI:10.2165/00023210-200519050-00001. с. 369 – 76.
- ↑ Sládková T, Kostolanský F. The role of cytokines in the immune response to influenza A virus infection // Acta Virol. 50 (3). 2006. с. 151 – 62.
- ↑ Munari L, Lovati R, Boiko A. Therapy with glatiramer acetate for multiple sclerosis // Cochrane database of systematic reviews (Online) (1). 2004. DOI:10.1002/14651858.CD004678. с. CD004678.
- ↑ Tremlett H, Oger J. Hepatic injury, liver monitoring and the beta-interferons for multiple sclerosis // J. Neurol. 251 (11). Ноември 2004. DOI:10.1007/s00415-004-0619-5. с. 1297 – 303.
- ↑ Kesselring J, Beer S. Symptomatic therapy and neurorehabilitation in multiple sclerosis // The Lancet Neurology 4 (10). 2005. DOI:10.1016/S1474-4422(05)70193-9. с. 643 – 52.
- ↑ Khan F, Turner-Stokes L, Ng L, Kilpatrick T. Multidisciplinary rehabilitation for adults with multiple sclerosis // Cochrane Database Syst Rev (2). 2007. DOI:10.1002/14651858.CD006036.pub2. с. CD006036.
- ↑ Smith, Cath и др. How does exercise influence fatigue in people with multiple sclerosis? // Disability and Rehabilitation 31 (9). 2009. DOI:10.1080/09638280802273473. с. 685 – 692.
- ↑ а б O'Sullivan, Susan. Physical Rehabilitation Fifth Edition. Philadelphia, F.A. Davis Company, 2007. ISBN 978- 0-8036-1247-1. с. 136 – 146.
- ↑ а б в Stroud NM, Minahan CL. The impact of regular physical activity on fatigue, depression and quality of life in persons with multiple sclerosis // Health and Quality of Life Outcomes 7. 2009. DOI:10.1186/1477-7525-7-68. с. 68.
- ↑ Rietberg MB, Brooks D, Uitdehaag BMJ, Kwakkel G. Exercise therapy for multiple sclerosis // Cochrane Database of Systematic Reviews CD003980 (1). 2005. DOI:10.1002/14651858.CD003980.pub2. с. CD003980.
- ↑ а б Multiple sclerosis: its effects on you and those you love (pdf) // Multiple Sclerosis Society of Canada, 2008. Архивиран от оригинала на 2011-09-17. Посетен на 11 май 2011.
- ↑ Dalgas U, Stenager E, Jakobsen J et al. Resistance training improves muscle strength and functional capacity in multiple sclerosis // Neurology 73 (18). 2009. DOI:10.1212/WNL.0b013e3181bf98b4. с. 1478 – 1484.
- ↑ Olsen SA. A review of complementary and alternative medicine (CAM) by people with multiple sclerosis // Occup Ther Int 16 (1). 2009. DOI:10.1002/oti.266. с. 57 – 70.
- ↑ Farinotti M, Simi S, Di Pietrantonj C, et al. Dietary interventions for multiple sclerosis // Cochrane database of systematic reviews (Online) (1). 2007. DOI:10.1002/14651858.CD004192.pub2. с. CD004192.
- ↑ Chong MS, Wolff K, Wise K, Tanton C, Winstock A, Silber E. Cannabis use in patients with multiple sclerosis // Mult. Scler. 12 (5). 2006. DOI:10.1177/1352458506070947. с. 646 – 51.
- ↑ Bennett M, Heard R. Hyperbaric oxygen therapy for multiple sclerosis // Cochrane database of systematic reviews (Online) (1). 2004. DOI:10.1002/14651858.CD003057.pub2. с. CD003057.
- ↑ Adams, Tim. Gut instinct: the miracle of the parasitic hookworm // The Observer, 23 май 2010.
- ↑ а б МС Общество България – Българската фондация за множествена склероза // Архивиран от оригинала на 2013-11-26. Посетен на 17 януари 2011.
- ↑ ПАЛОВА, Елица. {{{title}}} // Лечител 8. 2010 февруари 25. Посетен на 24 януари 2013.
- ↑ Наредба за определяне на видовете работи, за които се установява намалено работно време[неработеща препратка].
- ↑ а б Compston A. The 150th anniversary of the first depiction of the lesions of multiple sclerosis // J. Neurol. Neurosurg. Psychiatr. 51 (10). Октомври 1988. DOI:10.1136/jnnp.51.10.1249. с. 1249 – 52.
- ↑ Lassmann H. The pathology of multiple sclerosis and its evolution // Philos Trans R Soc Lond B Biol Sci. 354 (1390). 29 октомври 1999. DOI:10.1098/rstb.1999.0508. с. 1635 – 40.
- ↑ Lassmann H. Multiple sclerosis pathology: evolution of pathogenetic concepts // Brain Pathology 15 (3). July 2005. DOI:10.1111/j.1750-3639.2005.tb00523.x. с. 217 – 22.
- ↑ Световен Ден на множествената склероза // Архивиран от оригинала на 2016-03-04. Посетен на 2012-05-15.
Допълнителна литература[редактиране | редактиране на кода]
- Герасимов, Борислав. Mножествена склероза и емоции. (Библ. Множествена склероза – неврологич. предизвикателство на XX в.; Кн.1). София, Университетско издателство „Св. Климент Охридски“. ISBN 954-07-1099-5. с. 30.
- Герасимов, Борислав. Памет, интелект и множествена склероза. (Библ. Множествена склероза-невролог.предизвикателство на XX в.; Кн.2). София, Университетско издателство „Св. Климент Охридски“. ISBN 954-07-1100-2. с. 36.
- Герасимов, Борислав. Тазоворезервоарни и сексуални разстройства при множествена склероза. (Библ. Множествена склероза-невролог.предизвикателство на XX в.; Кн.3). София, Университетско издателство „Св. Климент Охридски“. ISBN 954-07-1109-6. с. 38.
- Герасимов, Борислав. Психосоциални проблеми при множествена склероза (Библ. Множествена склероза-невролог.предизвикателство на XX в.; Кн.4). София, Университетско издателство „Св. Климент Охридски“. ISBN 954-07-1124-X. с. 51.
- Миланов, Иван. Множествена склероза и демиелинизиращи заболявания. Медицина и физкултура. ISBN 978-954-420-279-8.
- Langgartner M, Langgartner I, Drlicek M. The patient's journey: multiple sclerosis // BMJ 330 (7496). Април 2005. DOI:10.1136/bmj.330.7496.885. p. 885 – 8. (на английски)
| Тази страница частично или изцяло представлява превод на страницата Multiple sclerosis в Уикипедия на английски. Оригиналният текст, както и този превод, са защитени от Лиценза „Криейтив Комънс – Признание – Споделяне на споделеното“, а за съдържание, създадено преди юни 2009 година – от Лиценза за свободна документация на ГНУ. Прегледайте историята на редакциите на оригиналната страница, както и на преводната страница, за да видите списъка на съавторите.
ВАЖНО: Този шаблон се отнася единствено до авторските права върху съдържанието на статията. Добавянето му не отменя изискването да се посочват конкретни източници на твърденията, които да бъдат благонадеждни. |
|
| Тази статия е включена в списъка на избраните на 07.02.2012. Тя е оценена от участниците в проекта като една от най-добрите статии на български език в Уикипедия. |