Туберкулоза
| Туберкулоза | |
 Рентгенова снимка на гръдния кош на човек с напреднала форма на туберкулоза. Белите стрелки показват огнище на инфекцията в белите дробове. Черните стрелки показват местонахождението на образувана каверна (кухина). | |
| Класификация и външни ресурси | |
|---|---|
| МКБ-10 | A15–A19 |
| МКБ-9 | 010–018 |
| OMIM | 607948 |
| База данни DiseasesDB | 8515 |
| База данни MedlinePlus | 000077 |
| База данни eMedicine | med/2324 emerg/618 radio/411 |
| Мед. рубрики MeSH | D014376 |
| Туберкулоза в Общомедия | |
Туберкулозата (на латински: Tuberculosis), разговорно наричана също охтика или особено в литературата „Жълтата гостенка“, е хронично протичащо специфично възпалително заболяване, което засяга предимно белите дробове, но може да засегне и централната нервна система, лимфните съдове, храносмилателната система, костите, ставите или кожата.
Специфичният причинител на туберкулозата е Mycobacterium tuberculosis, наречен още бацил на Кох. Той бива 5 основни типа (човешки, говежди, птичи, миши и поикилотермен), като епидемиологично значение за човека имат първите два. Лекува се с индивидуална антибиотична терапия. В прибалтийските страни са забелязани случаи на резистентни към известните лекарства щамове. Той се намира навсякъде в околната среда. Източник на заразата е болният от туберкулоза, който кашля[1]. Повечето инфекции са асимптоматични и латентни. Но около една на десет латентни инфекции се развиват прогресивно и активират заболяването. Ако туберкулозата не се лекува, тя води до смърт при повече от 50% от инфектираните. Най-застрашени от заразяване и заболяване са контактните, т.е. живеещите и работещите в едно помещение с болния. Не всеки контактен се разболява. От туберкулоза се разболяват лица с потисната имунна система. Предразполагащи фактори са непълноценното и нерационалното хранене, стресът, преумората, злоупотребата с алкохол, тютюнопушенето, т.е. всичко, което срива защитата на организма. Рискови за заболяване от туберкулоза са и лица със захарен диабет, стомашно-чревни страдания, лекуваните продължително време с кортизонови препарати, провеждащите химио- и лъчелечение и др.
Класическите симптоми на активната туберкулозна инфекция са хронична кашлица с примесени с кръв храчки, температура, нощно потене и загуба на тегло. В миналото наричали туберкулозата „охтика“, заради загубата на тегло при инфектираните. Инфектирането на други органи предизвиква широка гама от симптоми. Диагнозата на активна туберкулоза се основава на радиологично изследване (обикновено рентген на гръдния кош), както и микроскопско изследване и микробиологична култура на телесните флуиди. Диагнозата на латентната туберкулоза се основава на туберкулинов кожен тест (TКT) и кръвни тестове. Лечението е трудно и налага прилагането на множество антибиотици в продължение на дълъг период от време. Наблюдават се също и хората, които са били в контакт с болния и ако е необходимо им се прилага лечение. Резистентността към антибиотиците е все по-нарастващ проблем при туберкулоза с мултилекарствена резистентност (MDR-TB) инфекции. За да се предотврати туберкулозата, хората трябва да бъдат проверявани за наличие на заболяването и ваксинирани с ваксина с бацил на Калмет–Герен.
Експертите смятат, че една трета от населението на света е заразено с Mycobacterium tuberculosis[2] и всяка секунда се заразява по един човек по света.[2] През 2007 г. е изчислено, че по света са активни 13,7 милиона хронични случаи.[3] През 2010 г. е изчислено, че са се заразили нови 8,8 милиона души и е имало 1,5 милиона смъртни случая, най-вече в развиващите се страни.[4] Абсолютният брой на случаите на туберкулоза намалява от 2006 г. насам, а новите случаи са намалели от 2002 г.[4] Туберкулозата не е разпределена равномерно по света. Около 80% от населението в много азиатски и африкански страни дава положителен резултат при туберкулинов тест, но само 5 – 10% от населението в САЩ дава положителен резултат от теста.[5] Повечето хора в третия свят развиват туберкулоза поради отслабен имунитет. Обикновено тези хора развиват туберкулоза, защото са инфектирани с ХИВ и развиват СПИН.[6]
Етиология[редактиране | редактиране на кода]

Главният причинител на туберкулозата при човека е аеробната неподвижна бактерия Mycobacterium tuberculosis[7]. Много от характеристиките на заболяването се дължат на високото съдържание на липиди в този патоген.[8] Клетките на бактерията се делят на всеки 16 – 20 часа, много бавно в сравнение с други бактерии, които се делят за по-малко от час.[9] Микобактериите имат клетъчна мембрана от липиден двоен слой.[10] Ако се извърши оцветяване по Грам, микобактерията или се оцветява леко Грам-положително или не задържа оцветяване, защото стената на клетката и има високо липидно и муколитично киселинно съдържание.[11] Микобактерията на туберкулозата може да устои на слаб дезинфектант и може да оцелее в сухо състояние в продължение на седмици. В природата бактерията може да се развива само в клетките на организъм-приемник, но може да бъде отгледана в лабораторни условия.[12]
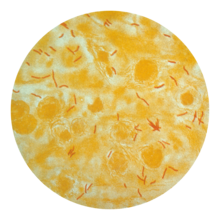
Като използват хистологични оцветявания върху изкашляни проби от храчка, учените могат да идентифицират микобактерията на туберкулозата под обикновен (светлинен) микроскоп. Микобактерията на туберкулозата задържа някои петна дори и след като се обработи с киселинен разтвор, затова се класифицира като киселинноустойчив бацил.[5][11] Най-широко разпространени са две техники на киселинноустойчиво оцветяване:
- оцветяване по Цил – Нилсен, при което киселинноустойчивият бацил се оцветява в ярко червено, което изпъква ясно на син фон;[13]
- оцветяване с аурамин – родамин, последвано от флуоресцентна микроскопия.[14]
Групата на M. tuberculosis включва още четири микобактерии, причиняващи туберкулоза – M. bovis, M. africanum, M. canetti и M. microti.[15] M. africanum не е широко разпространена, но в някои части на Африка е важен причинител на болестта.[16][17] M. bovis в миналото е основен причинител на туберкулоза, но масовата пастьоризация на млякото до голяма степен я елиминира като заплаха за хората в развитите страни.[5][18] M. canetti е рядка и изглежда се среща само в Африка, макар че са известни няколко случая при африкански емигранти.[19] M. microti е наблюдавана главно при пациенти с имунна недостатъчност, макар че е възможно разпространението ѝ да е подценявано.[20]
Другите познати патогенни микобактерии включват M. leprae, M. avium, и M. kansasii. Последните два вида се класифицират като нетуберкулозни микобактерии (НТМ). НТМ не предизвикват туберкулоза или проказа, но те в действителност причиняват белодробни заболявания, които наподобяват туберкулозата.[21]
Исторически сведения за заболяването[редактиране | редактиране на кода]
В древността[редактиране | редактиране на кода]

Туберкулозата е заболяване, известно от древността. Най-ранните сигурни доказателства за това датират от епохата на плейстоцена. Открити са фрагменти ДНК от причинителя на заболяването в кост на бизон, живял в Северна Америка и боледувал от туберкулоза преди 17 500 – 18 000 години.[22] Все още не е ясно дали човекът се е превърнал в чувствителен за заболяването вид, заразявайки се от одомашнените животни, или е настъпил точно обратният процес.[23] Последните изследвания сочат, че основните причинители за туберкулозата при човека и говедата (Mycobacterium tuberculosis и Mycobacterium bovis) не произлизат пряко един от друг, а имат общ предшественик.[24]
При археологически разкопки в източното Средиземноморие учени откриват общ гроб на майка и дете, погребани преди около 9000 години. При изследване на костите им се установява, че те са боледували от туберкулоза.[25] Характерни за туберкулозата изменения са открити в гръбначен стълб на египетска мумия на възраст 4500 – 5000 години.[26] Сигурни доказателства за наличие на туберкулоза при хората в Южна Америка датират отпреди 2000 години при мумии, открити в Андите. От общо 12 при 7 от тях има ясни доказателства, че са боледували от това заболяване.[27]
Дълго преди да бъде открит причинителят на туберкулозата се е предполагало, че тя е заразна болест. Във вавилонския кодекс на Хамурапи било разрешено правото на развод с болна жена, проявяваща признаци на белодробна туберкулоза. В Индия, Португалия и Венеция били издадени закони, които задължавали болните от туберкулоза да съобщават за своето състояние.
В народните вярвания и фолклор[редактиране | редактиране на кода]
В годините преди възникването на индустриалната революция доста често се е приемало, че болните от туберкулоза са вампири. Хората смятали, че когато в едно семейство почине човек от туберкулоза, останалите членове на семейството губят своето здраве и бавно умират. Според суеверието се вярвало, че умрелият от туберкулоза член на семейството бавно източва живота на своите близки. Тези вярвания се подкрепяли и от факта, че болните проявяват симптоми, подобни на тези за които се смята, че са свойствени за вампирите. Хората с туберкулоза почти винаги имат червени, подути очи (състояние, при което се проявява чувствителност към ярка светлина), бледа кожа, ниска телесна температура и храчене на кръв.[28] Други народни вярвания приписват болестта на непрестанни нощни самодивски танци, които изтощават жертвата поради липсата на почивка. Според други поверия болните са приемани като жертва на кошмари.[29] През 19 век на туберкулозата е придаден романтичен характер, благодарение на чувството на еуфория възникващо в последния етап на болестта. При прогресиране на заболяването страдалците проявяват особен изблик на енергия, което ги прави по-креативни за кратък етап от болестта.[30]
В миналото в България заболяването е наричано с описателните имена охтика и жълта гостенка. Тези имена се дължат на характерните признаци на заболяването – прогресивна кашлица и отслабване.
Научно изследване на болестта[редактиране | редактиране на кода]
Началото на същинското проучване на туберкулозата се поставя с труда „Медицински канон“ на Авицена от 1020 г. Той е първият учен идентифицирал белодробната туберкулоза като контагиозна болест, първи установява и връзката между диабета и туберкулозата, и първи изказва предположението, че тя може да се предаде при контакт с почва и вода.[31][32] Авицена създава и метод на карантиниране на болните във връзка с ограничаване на разпространението на туберкулозата.[33] В древността лечението на заболяванията се е фокусирало върху прилагането на диети. В тази връзка Плиний Стари в своето произведение „Естествена история“ описва няколко метода на лечение на туберкулозата. Такива например са консумацията на черен дроб от вълк, предварително накиснат в слабо вино, консумиране на свинска мас от свиня, хранена само с трева, или месен бульон от женско магаре.[34]
Въпреки че през 1689 г. д-р Ричард Мортън установява връзката на белодробната форма с наличието на туберкули,[35][36] поради многообразието на проявените симптоми, туберкулозата не е била идентифицирана като едно общо заболяване. Едва през 1820 г. става ясно, че всички признаци касаят това заболяване, а през 1839 г. Йохан Шьонлайн го нарича с името туберкулоза.[37] През периода 1838 – 1845 г., собственикът на Мамутовата пещера, д-р Джон Крогън довежда редица страдащи от туберкулоза с надежда те да се излекуват благодарение на постоянната температура и чистотата на въздуха в пещерата. Болните умират в рамките на една година след тяхното идване.[38] Първият санаториум за туберкулозно болни е открит през 1859 г. от Херман Бремер в градчето Гьорберсдорф, тогава в Германия (днес Соколовско, Полша).[39]
През 1868 г. немският патолог Теодор Лангханс при изследване на туберкули открива наличието на гигантски клетки в тях.

В средата на XIX век френския корабен лекар Жан Вилмен наблюдавал разпространението на туберкулоза благодарение на болен матрос на кораба, когото обслужвал. Като доказателство за заразния характер на болестта той събирал храчки от пациенти и заразявал с тях морски свинчета. Животните заболявали и умирали от туберкулоза. Вилмен достига до извода, че туберкулозата има заразен характер. Мнението на Вилмен било потвърдено през 1879 г. и от немския патолог Юлиус Конхайм. При опитите си той заразявал зайци с поразени тъкани на умрели от туберкулоза хора.
През XIX и началото на XX век заболяването придобива сериозна обществена значимост като се превръща в ендемично заболяване на бедните граждани.[40] През 1815 г. един от четири смъртни случая в Англия е в резултат на туберкулоза, а във Франция през 1918 г. всеки шести умира от нея. През XX век от туберкулоза умират около 100 милиона души.[41] След като е бива установен заразния характер на болестта във Великобритания е предприета кампания за прекратяване на храченето на обществени места, а болните бедняци са притискани да влязат в санаториуми, чиито условия наподобяват тези на затвор. В същия момент санаториумите за по-богатите кръгове от обществото предлагат многократно по-добри условия и постоянни медицински грижи. Въпреки това обаче, каквито и условия да се предлагат в санаториумите дори и в най-добрите 50% от постъпилите в тях са умирали до петата година в тях. В Съединените щати също се отнасят сериозно към разпространението на заболяването като се забранява плюенето на обществени места с изключение на специално поставени за целта плювалници.

Причинителят на туберкулозата Mycobacterium tuberculosis, е идентифициран и описан на 24 март 1882 г. от Роберт Кох. Това откритие се дължи на седемнадесетгодишен труд. Той бива видян от Кох в микроскопски препарат от храчка на туберкулозно болен човек. За това си откритие той получава Нобелова награда за физиология и медицина през 1905 г.,[42] а причинителят в началото е наречен в негова чест „Бацил на Кох“. Кох не е вярвал, че говеждата и човешката туберкулоза са близки помежду си. Това забавя откриването на връзката заразено мляко консумирано от хора да е възможен път за заразяване. През следващите години благодарение на пастьоризацията на млякото този процес е прекратен и спомага за ограничаване на случаите на заразяване на хора.
Развитие на диагностиката, профилактиката и лечението на туберкулозата[редактиране | редактиране на кода]
През 1819 г. френският лекар Рене Лаенек предлага метода аускултация на белите дробове. Той повлиява положително в по-нататъшната разработка на методите на диагностика на туберкулозата.
През 1890 г. Роберт Кох получава за първи път туберкулин и го описва като „водно-глицеринов извлек на туберкулинова култура“. За целите на диагностиката Кох предлага да се извършва подкожна проба с инжектиране на туберкулин. На лекарския конгрес в Берлин Кох съобщил за възможно профилактично и даже лечебно действие на туберкулина. Той бил изпитан при опитите му с морски свинчета както и върху себе си и своята сътрудничка (която впоследствие става негова съпруга). Година след това отново в Берлин е направено официално заключение относно високата ефективност на туберкулина в диагностиката, докато лечебните му свойства били доста противоречиви.
Първият истински успех в създаването на ваксина против туберкулоза е разработен от атенюиран щам на Mycobacterium bovis. Това откритие било направено от микробиолога Албер Калмет и ветеринарния лекар Камил Герин през 1906 г. Тя е наречена „БЦЖ“ („BCG“/Bacillus of Calmette and Guérin). Тази ваксина била приложена за първи път във Франция на новородено и е започнала масово да се прилага при хора в страната, а в годините след Втората световна война ваксинацията бързо се налага и в САЩ, Великобритания и Германия.
През 1943 г. Зелман Ваксман и Алберт Шац получават стрептомицин, който става и първия антимикробен препарат оказващ бактериостатично действие на причинителите на заболяването. През 1946 г. той е използван за пръв път в лечението на туберкулозата.
Въпреки надеждите за окончателно ликвидиране на болестта и въвеждането на нови лекарствени средства в борбата с нея през 80-те години се получават сведения за появата на мултирезистентни щамове. Пример за това са случаите на туберкулоза във Великобритания. През 1913 г. са регистрирани 117 000 туберкулозно болни, през 1987 г. те спадат до около 5000, но случаите отново нарастват през следващите години достигайки до 6300 през 2000 г. и 7600 през 2005 г.[43] През 1993 г. СЗО обявява декларация от опасността от разпространение на мултирезистентна туберкулоза.[44] В световен мащаб ежегодно от резистентни щамове се разболяват около половин милион души.[45]
Разпространение[редактиране | редактиране на кода]
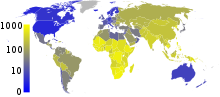
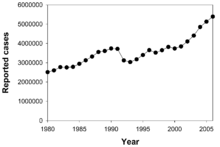
Около една трета от населението в света е инфектирано с Mycobacterium tuberculosis. На всяка секунда в света възниква по една нова инфекция.[47] Въпреки това повечето инфекции с Mycobacterium tuberculosis не причиняват туберкулозно заболяване[48], а 90 до 95 % от инфекциите остават асимптоматични.[49] През 2007 г. се е смятало, че хроничните активни заболели наброяват 13,7 милиона души.[3] През 2010 г. са диагностицирани 8,8 милиона нови случая на туберкулоза и 1,45 милиона смъртни случая, повечето от тях в развиващите се страни.[4] От тези 1,45 милиона смъртни случая около 0,35 милиона са при хора със смесена инфекция с HIV.[50]
Туберкулозата е втората най-честа причина за смъртност от инфекциозни заболявания (след смъртността от HIV/СПИН).[7] Абсолютният брой на туберкулозни случаи („болестност“) прогресивно намалява от 2005 г. Новите случаи на туберкулоза (заболеваемост) намаляват от 2002 г.[4] Китай постига особено впечатляващ напредък. Смъртността в тази страна е намаляла с приблизително 80% между 1990 и 2010 г.[50] Туберкулозата се среща по-често в развиващите се страни. Около 80% от населението в много азиатски и африкански държави дава положителен резултат от туберкулиновите тестове, при само 5 – 10 % положителни резултати от тестовете сред населението на САЩ.[5] Експертите се надяват, че туберкулозата ще може да се контролира напълно. Въпреки това няколко фактора правят малко вероятен пълния контрол върху туберкулозата. Трудно е да се разработи ефикасна ваксина. Диагностицирането на заболяването е скъпо и отнема време. Лечението изисква много месеци. Все повече хора с HIV се заразяват с туберкулоза. Лекарствено резистентната туберкулоза се появява през 80-те години на 20 век.[6]
През 2007 г. държавата с най-висока заболеваемост от туберкулоза е Свазиленд с 1200 случая на 100 000 души. Индия е с най-голяма обща заболеваемост с отчетени 2 милиона нови случая.[3] В развитите държави туберкулозата се среща по-рядко, главно в градските райони. През 2010 г. случаите на туберкулоза на 100 000 души в различни места по света са били: общо за света – 178, Африка – 32, Северна, Централна и Южна Америка – 36, Източното Средиземноморие – 173, Европа – 63, Югоизточна Азия – 278 и Западния тихоокеански регион – 139.[50] В Канада и Австралия туберкулозата се среща много по-често сред аборигенните племена, по-специално в отдалечените области.[52][53] В Съединените щати смъртността от туберкулоза при коренното население е пет пъти по-висока.[54]
Туберкулозата при говедата е слабо разпространена в страните от ЕС. В някои от тях дори е напълно ликвидирана. В България случаите на туберкулоза при говедата са също единични. При птиците заболяването е широко разпространено. Най-разпространена е сред популацията домашни птици отглеждани по екстензивен начин в малки лични стопанства. При свинете заболяването е слабо разпространено и е в пряка връзка от съвместното отглеждане с болни говеда и птици и отглеждането им от болни от туберкулоза стопани. При останалите домашни животни има спорадичен характер и се проявява с единични случаи.
Епидемиология[редактиране | редактиране на кода]
Рискови фактори[редактиране | редактиране на кода]
Съществуват няколко фактора, които правят хората по-податливи на туберкулозни инфекции. Най-важният рисков фактор в световен мащаб е HIV – 13% от всички случаи на туберкулоза са инфектирани с HIV.[4] Този проблем е често срещан в Субсахарска Африка, където процентът заразени с HIV е висок.[55][56] Туберкулозата е тясно свързана с пренаселеността и лошото хранене. Тази връзка превръща заболяването в едно от водещите болести на бедността.[6] С най-висок риск от заразяване са хора употребяващи наркотици, жители и служители на места, където се събират лесно податливи на зараза хора (например затвори и подслони за бездомни), хора, които са бедни и нямат достъп до адекватни медицински грижи, високорискови етнически малцинства, деца в близък контакт с високорискови хора и здравните работници, които обслужват тези групи.[57] Хроничното белодробно заболяване е друг значителен рисков фактор. Силикозата например увеличава риска от около 30 пъти.[58] Тютюнопушещите са около два пъти по-рискови за заразяване в сравнение от непушачите.[59] Други болестни състояния също могат да увеличат риска от развиване на туберкулоза, включително алкохолизъм[6] и захарен диабет (тройно по-висок риск).[60] Някои лекарства, като кортикостероиди и инфликсимаб (анти-αTNF моноклонално антитяло) стават все по-значими рискови фактори, особено в развития свят.[6] Съществува също и генетична предразположеност[61], но учените все още не са определили доколко тя има значение.[6]
Предаване[редактиране | редактиране на кода]
Когато хора с активна белодробна туберкулозна кашлица кихат, говорят, пеят или плюят те отделят заразни аерозолни капки с диаметър от 0,5 до 5 µm. Само при едно кихане може да отделят до 40 000 микроскопични капчици.[62] Всяка от тях може да предаде заболяването, тъй като необходимото количество за заразяване с туберкулоза е много ниско. Човек може да се зарази дори ако е вдишал по-малко от 10 бактерии.[63]
Хората в продължителен, чест или близък контакт с болни от туберкулоза са под висок риск от заразяване като процентът достига до 22%.[64] Един човек с активна, но нелекувана туберкулоза може да зарази 10 – 15 (или повече) други хора на година.[2] Обикновено само хора с активна туберкулоза предават заболяването. Счита се, че хората с латентна инфекция не са заразни.[5] Вероятността за предаване от един човек на друг зависи от няколко фактора. Тези фактори включват броя заразни капки, които отделя носителят на заразата, ефикасността на вентилацията на средата на съответните хора, продължителността на експозицията, вирулентността на микобактерията и нивото на имунитета на незаразения човек.[65] За да се предотврати каскадата на разпространение от човек на човек, хората с активна (изразена) туберкулоза трябва да бъдат отделени и подложени на лечение. След около две седмици ефикасно лечение, хората с неустойчиви към антибиотици активни инфекции в общия случай не остават заразни за другите.[64] Ако някой все пак се зарази, обикновено отнема три до четири седмици, преди новозаразеният да стане достатъчно заразен, за да предаде заболяването на другите.[66]
Възприемчивост[редактиране | редактиране на кода]
Заболеваемостта от туберкулоза варира според възрастта. В Африка заболяването засяга предимно хора на възраст между 12 и 18 години и млади хора в зряла възраст.[67] Въпреки това в държави, в които заболеваемостта е намаляла значително (като Съединените щати), туберкулозата е най-вече заболяване на по-възрастните хора и хората с отслабена имунна система.[5][68]
При говедата болестта се причинява от Mycobacterium bovis. Заразяването с Mycobacterium tuberculosis не предизвиква заболяване, а само ограничени локални поражения в лимфните възли на храносмилателния канал. Говедата се заразяват и с Mycobacterium avium в случаите на съвместно отглеждане с птици, каквото доста често се наблюдава при екстензивното животновъдство. И в този случай не се предизвиква заболяване, а само единични изменения в лимфните възли на храносмилателната система. Въпреки че последните два причинителя не предизвикват заболяване при говедата, те ги алергизират за известен период и е възможно да покажат положителна или неопределена (съмнителна) кожна реакция при алергично изследване с туберкулин.
Туберкулозата при свинете се дължи и на трите причинителя като най-често боледуват от говеждия тип, по-рядко от птичия и най-рядко от човешкия.
Домашните продуктивни птици боледуват от туберкулоза, причинена от Mycobacterium avium. Папагалите и други птици, отглеждани като домашни любимци, биват заразявани от Mycobacterium tuberculosis.
Конете и дребният рогат добитък (овце и кози) боледуват от туберкулоза, причинена от Mycobacterium bovis.
Кучетата и котките боледуват от туберкулоза, причинена от Mycobacterium bovis и Mycobacterium tuberculosis.
От домашните животни най-възприемчиви са говедата и биволите, по-слабо свинете последвани от коне, овце, кози, кучета и котки. От домашните птици най-чувствителни са кокошките, а патиците, гъските, гълъбите и пъдпъдъците са устойчиви на заболяването. Диви и екзотични бозайници и птици, отглеждани при домашни условия, могат да бъдат опасен източник на заразяване за човека. Най-често това се случва при отглеждане на примати заловени от дивата природа или отглеждани и развъждани в неблагоприятни условия.
Патогенеза[редактиране | редактиране на кода]
Около 90% от хората, които са заразени с Mycobacterium tuberculosis имат асимптоматични, латентни туберкулозни инфекции.[49] При тези хора шансът латентната инфекция да прогресира в изразена, активна туберкулоза, е само 10%.[69] При хората с HIV рискът да развият активна туберкулозна инфекция се увеличава с почти 10% на година.[69] Ако не се осигури ефикасно лечение, смъртността за случаите на активна туберкулоза е до 66%.[2]
Туберкулозната инфекция започва, когато микобактериите достигнат белодробните алвеоли, където те навлизат и се размножават в ендозомите на алвеоларните макрофаги.[5][70] Основното огнище на инфекцията в белите дробове, познато като огнище на Гон, се намира в горния или долния дял или в долната част на горния дял.[5] Туберкулозата в белите дробове може да се получи също и чрез инфекция от кръвния поток, която е позната като огнище на Саймън. Инфекцията с огнище на Саймън обикновено се открива в горната част на белия дроб.[71] Това хематогенно предаване също може да разпространи инфекцията до по-отдалечени места, като периферните лимфни възли, бъбреците, мозъка и костите.[5][72] Туберкулозата засяга всички части на тялото, макар че по неизвестни причини рядко засяга сърцето, скелетните мускули, панкреаса или щитовидната жлеза.[73]
Туберкулозата се класифицира като едно от грануломатозните възпалителни заболявания. Макрофагите, T-лимфоцитите, B-лимфоцитите и фибробластите са сред клетките, които се струпват, за да формират грануломи. Лимфоцитите заобикалят заразените макрофаги. Грануломата предотвратява разпространението на микобактериите и осигурява местна среда за взаимодействие между клетките на имунната система. Бактериите в грануломата могат да се превърнат в латентни, което води до латентна инфекция. Друга характеристика на грануломите е развитието на анормална смърт на клетките (некроза) в центъра на туберкулите. Наблюдавана с просто око тази некроза наподобява структурата на меко бяло сирене и се нарича казеозна некроза.[74]
Бактериите на туберкулозата могат да навлязат в кръвния поток от участък с нарушена тъкан. Те могат да се разпространят в цялото тяло и да създадат много огнища на инфекцията, които се виждат като малки бели туберкули в тъканите.[75] Тази остра форма на туберкулозата се нарича милиарна туберкулоза. Тя се среща най-често при малки деца и хора с HIV.[76] Хората с тази дисеминирана туберкулоза са с висок процент на смъртност дори и при лечение (около 30%).[77][78]
При много хора инфекцията се засилва и отслабва. Разрушаването на тъканите и некрозата често се компенсират със зарастване и фиброза.[74] Засегнатата тъкан се заменя с ръбцова тъкан (сраствания) и каверни (кухини), изпълнени с казеозно-некротичен материал. По време на активното заболяване, някои от тези кухини се свързват към дихателните пътища бронхи и този материал може да бъде изкашлян. Този материал съдържа живи бактерии и може да разпространи инфекцията. Лечението с подходящи антибиотици убива бактериите и благоприятства лекуването. Когато заболяването бъде излекувано, засегнатите участъци се заменят от съседна тъкан.[74]
Клинични признаци[редактиране | редактиране на кода]
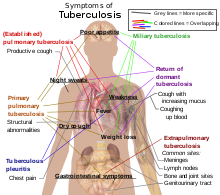
Около 5–10% от хората, които нямат ХИВ, но са заразени с туберкулоза развиват активна форма на заболяването през живота си.[80] Обратно на това 30% от хората, които са инфектирани с ХИВ и туберкулоза развиват активна форма на заболяването.[80] Туберкулозата може да инфектира всяка част на тялото, но тя най-често прониква в белите дробове (позната като пулмонарна (белодробна) туберкулоза).[7] Екстрапулмонарна туберкулоза се проявява, когато туберкулозата се развие извън белите дробове. Екстрапулмонарната туберкулоза може да съществува едновременно с пулмонарната.[7] Първите симптоми за туберкулоза са обща отпадналост, лесна умора, безапетитие, поддържане на температура 37 – 38 °C, с продължително време (месеци), обилно нощно потене. Освен това болните се оплакват от студени тръпки, загуба на апетит и телесно тегло, бърза умора.[7] Може също да се появи значителна деформация на пръстите.[80]
Пулмонарна форма[редактиране | редактиране на кода]
Ако туберкулозната инфекция се активира, тя засяга белите дробове при около 90% от хората.[6][81] Симптомите може да включват болки в гърдите и продължителна кашлица с храчки. Около 25% от хората нямат никакви симптоми (асимптоматични).[6] Понякога болните храчат кръв в малки количества. В редки случаи инфекцията може да разруши стената на белодробната артерия, което води до масивен кръвоизлив, наречен аневризъм на Расмунсен. Туберкулозата може да стане хронично заболяване и да остави значителни следи в горните белодробни лобове. Най-често се засяга горната част на белите дробове.[7] Причината за това не е напълно ясна.[5] Може би горната част на белите дробове се засяга повече заради по-добрия приток на въздух[5] или поради лош лимфен дренаж.[7]
Екстрапулмонарна форма[редактиране | редактиране на кода]
При 15–20% от активните случаи инфекцията се разпространява извън дихателните органи, което причинява други видове туберкулоза.[82] Туберкулозаната инфекция, чиито огнища са извън дихателните органи се нарича „екстрапулмонарна туберкулоза“.[83] Екстрапулмонарната туберкулоза се появява най-често при хора с потисната имунна система и при малки деца. Екстрапулмонарната форма се появява при повече от 50% от хората, които имат HIV.[83] Главните местонахождения на екстрапулмонарна инфекция включват плеврата (при туберкулозен плеврит), централната нервна система (при туберкулозен менингит) и лимфната система (като скрофулоза на врата). Екстрапулмонарната туберкулоза се проявява също и в пикочно-половата система (като урогенитална туберкулоза) и в костите и ставите (като болест на Пот на гръбначния стълб), а също и на други места. Когато се разпростре до костите, тя е позната също и като „костна туберкулоза“,[84] която е форма на остеомиелит.[85] Една потенциално по-сериозна, широко разпространена форма на туберкулозата, се нарича „дисеминираната“ туберкулоза, позната като милиарна туберкулоза.[7] Милиарната туберкулоза съставлява 10% от екстрапулмонарните случаи.[77]
Прогноза[редактиране | редактиране на кода]
Преминаването на туберкулозната инфекция изразено туберкулозно заболяване става, когато бацилите преодолеят защитата на имунната система и започнат да се размножават. При първично туберкулозно заболяване (около 1 – 5% от случаите), това развитие се случва скоро след първоначалната инфекция.[5] Въпреки това в повечето случаи латентната инфекция протича без явни симптоми.[5] Тези скрити бацили произвеждат активна туберкулоза в 5 до 10 % от латентните случаи, като често това става много години след инфекцията.[80]
Опасността от повторно активиране се увеличава при потисната имунна система, причинена например от инфекция с HIV. При хора, коинфектирани с Mycobacterium tuberculosis и HIV, опасността от повторно активиране нараства до 10 % на година.[5] Проучванията, които използват ДНК отпечатъци на щамове на Mycobacterium tuberculosis, сочат, че повторното инфектиране причинява повторно развиване на туберкулоза по-често, отколкото се считаше по-рано.[86] Повторните инфекции могат да възлизат на над 50 % от повторно активираните случаи в районите, където туберкулозата е често срещана.[87] Шансът за смъртност при туберкулоза е около 4 %, считано от 2008 г. – при 8 % през 1995 г.[6]
Патологоанатомични изменения[редактиране | редактиране на кода]
В резултат на възпалителния процес се образува специфичен туберкулозен гранулом наречен „туберкул“ от лимфоцити, епителоидни клетки, гигантски клетки тип Лангханс и централно разположена казеозна некроза.
Диагноза[редактиране | редактиране на кода]
Активна туберкулоза[редактиране | редактиране на кода]
Трудно е да се диагностицира активната туберкулоза въз основа само на признаци и симптоми.[88] Трудно е също заболяването да се диагностицира при хора, които са с потисната имунна система.[89] Хората, които показват признаци на белодробно заболяване или конституционални симптоми, които продължават за период по-дълъг от две седмици е възможно обаче да са заразени с туберкулоза.[89] Рентгенова снимка на гръдния кош и неколкократни посевки от храчки за киселиноустойчиви бацили обикновено са част от първоначалната оценка.[89] Интерферон-гама базираните тестове (IGRA) и кожните проби с туберкулин не са от полза в развиващите се страни.[90][91] IGRA са с подобни ограничения и при хората с HIV.[92][93]
Окончателна диагноза туберкулоза се поставя, когато се идентифицира Mycobacterium tuberculosis в клинична проба (например храчка, гной или биопсия на тъкан). Трудният процес на посявка за този организъм с бавен растеж обаче може да отнеме две до шест седмици за посявка от кръв или храчка.[94] Ето защо често лечението започва преди потвърждаване на посевките.[95]
Тестовете за амплификация на нуклеинови киселини и тестването на аденозин дезаминаза могат бързо да диагностицират туберкулозата.[88] Тези тестове обаче обикновено не се препоръчват, защото рядко променят начина на лечение на болния.[95] Кръвните тестове за отчитане на антитела не са специфични или чувствителни и поради тази причина не се препоръчват.[96]
Латентна туберкулоза[редактиране | редактиране на кода]

Туберкулинов кожен тест на Манту се използва често за скрининг на хора с висок риск за заболяване от туберкулоза.[89] Възможно е хора, които са били имунизирани по-рано, да дадат фалшив положителен резултат от пробата.[97] Пробата може да е фалшиво отрицателна при хора със саркоидоза, лимфом на Ходжкин и недохранване. Най-важното е, че пробата може да даде фалшив положителен резултат при хора с активна туберкулоза.[5] Интерферон-гама тестовете на кръвна проба се препоръчват за хора с положителна проба на Манту.[98] Интерферон-гама тестовете не се влияят от имунизация или от повечето бактерии от околната среда, така че те много рядко дават фалшиви положителни резултати.[99] Но те са засегнати от M. szulgai, M. marinum и M. kansasii.[100] Интерферон-гама тестът може да увеличи чувствителността, когато се използва в допълнение към кожната проба. Използван самостоятелно обаче, интерферон-гама тестът може да е по-малко чувствителен от кожната проба.[101]
Лечение[редактиране | редактиране на кода]
За лечението на туберкулоза се използват антибиотици, които унищожават бактериите. Ефикасното лечение на туберкулозата е трудно поради нетипичната структура и химически състав на микобактериалната клетъчна стена. Клетъчната стена отблъсква лекарствата и прави много от антибиотиците неефикасни.[102] Двата най-често използвани антибиотика са изониазид и рифампицин, а лечението може да продължи с месеци.[65] При лечението на латентна туберкулоза обикновено се прилага един антибиотик.[103] Активната форма на туберкулоза се лекува най-добре с комбинация от няколко антибиотика за намаляване на опасността бактериите да развият резистентност към антибиотици.[6] Латентната инфекция се лекува и за предотвратяване на активна форма на туберкулоза на по-късен етап от живота.[103] СЗО препоръчва пряко наблюдавано лечение. При това лечение лекарите наблюдават как пациентите вземат лекарствата си. Целта е да се намали броят на хората, които не приемат правилно антибиотиците.[104] Въпреки това, доказателствата в подкрепа на пряко наблюдаваното лечение са оскъдни.[105] Методите чрез напомняне на хората, че лечението е важно са ефикасни.[106]
Първоначална проява[редактиране | редактиране на кода]
От 2010 г. препоръчителното лечение при първоначална проява на белодробната туберкулоза е комбинация от антибиотици, приемана в продължение на шест месеца. През първите два месеца се приемат рифампицин, изониацид, пиразинамид и етамбутол. През следващите четири месеца се приема рифампицин и изониацид.[6] При висока резистентност към изоцианид през последните четири месеца може да се приложи етамбутол.[6]
Повторна проява на заболяването[редактиране | редактиране на кода]
При повторна проява на туберкулозата и преди определяне на лечението следва да се направи изследване на резистетността на заболяването към антибиотиците.[6] Ако се открие туберкулоза с мултилекарствена резистентност (MDR-TB), се препоръчва лечение с най-малко четири ефикасни антибиотика за период от 18 – 24 месеца.[6]
Лекарствена резистентност[редактиране | редактиране на кода]
Първична резистентност възниква, когато човек е инфектиран с резистентен щам на туберкулоза. Човек с напълно податлива туберкулоза може да развие вторична (придобита) резистентност по време на лечението. Даден пациент може да развие вторична резистентност поради неподходящо лечение, в случай че не е предписана съответната схема (липса на съответствие) или ако използва некачествени лекарства.[107] Лекарствено резистентната туберкулоза е сериозен проблем на общественото здраве в много развиващи се страни. Лечението на лекарствено резистентната туберкулоза е по-дълго и изисква по-скъпи лекарства. MDR-TB се определя като резистентност към двете най-ефикасни лекарства от първа линия за лечение на туберкулоза: рифампицин и изониацид. Екстензивно лекарствено резистентната туберкулоза е резистентна към три или повече от шестте класа лекарства от втора линия.[108] Напълно лекарствено резистентната туберкулоза е резистентна на всички използвани понастоящем лекарства. Напълно лекарствено резистентната туберкулоза е наблюдавана за първи път през 2003 г. в Италия, но до 2012 г. не се съобщава за голям брой случаи.[109]
Профилактика и борба[редактиране | редактиране на кода]
Усилията, насочени към профилактиката и контрола на туберкулозата разчитат на ваксинация на децата и откриване на подходящо лечение за проявите на активното заболяване.[6] Световната здравна организация е постигнала определен успех в подобряване на схемите на лечение. Отбелязва се слабо намаляване на броя на случаите.[6]
Ваксини[редактиране | редактиране на кода]
От 2011 г. насам единствената налична ваксина е бацил на Калмет и Герен (БЦЖ). БЦЖ е ефикасна ваксина срещу разпространяването на заболяването в детска възраст, но не осигурява достатъчна защита срещу белодробната туберкулоза.[110] И все пак това е най-широко използваната ваксина в света, като с нея са ваксинирани над 90% от всички деца.[6] След десет години обаче имунитетът, който тя дава, намалява.[6] Туберкулозата не е често срещана в повечето части на Канада, Великобритания и Съединените щати, така че ваксината БЦЖ се прилага само при хора с висок риск от заболяването.[111][112][113] Една от причините да не се използва ваксината е, че резултатите, които тя дава при кожен туберкулинов тест, са фалшиво положителни, което прави теста безполезен при проверка за това заболяване.[113] Разработват се нови ваксини.[6]
Обществено здравеопазване[редактиране | редактиране на кода]
През 1993 г. Световната здравна организация обявява туберкулозата като „извънредна ситуация по отношение на здравеопазването в световен мащаб“.[6] През 2006 г. в рамките на Инициативата за борба с туберкулозата (Stop TB Partnership) е разработен Глобален план за спиране на туберкулозата, чиято цел е спасяването на 14 милиона живота до 2015 г.[114] Редица от поставените цели вероятно няма да бъдат изпълнени до 2015 г., най-вече поради увеличаването на случаите на туберкулоза, свързана с HIV и появата на туберкулоза с мултилекарствена резистентност (MDR-TB).[6] В обществените програми за здравеопазване се използва система класификация на туберкулозата, разработена от Американското торакално общество.[115]
Общество и култура[редактиране | редактиране на кода]
Световната здравна организация и Фондацията на Бил и Мелинда Гейтс субсидират нов бързодействащ диагностичен тест за страните с ниски и средни доходи.[116][117] До 2011 г. много бедни населени места все още имат достъп само до микроскопско изследване на храчка.[118]
През 2010 г. Индия е с най-голям общ брой случаи на туберкулоза в света. Една от причините е слабият контрол над заболяването от страна на частния сектор на здравеопазването. Програми като Ревизирана програма за национален контрол на туберкулозата помагат за намаляване на случаите на туберкулоза сред хората, получаващи обществени здравни грижи.[119][120]
Изследвания[редактиране | редактиране на кода]
БЦЖ ваксината има известни ограничения и са в ход изследвания за разработване на нова ваксина против туберкулоза.[121] Няколко потенциални кандидата са в процес на фаза I и II на клинично изпитване.[121] Два основни подхода се опитват да подобрят ефикасността на съществуващите ваксини. Единият от тях включва добавяне на субединична ваксина към БЦЖ. Другата стратегия се опитва да създаде нови и по-добри живи ваксини.[121] MVA85A е пример за субединична ваксина, която се изпитва в Южна Африка. MVA85A е базирана на генетично модифициран вакциния вирус.[122] Надеждата е, че ваксините ще изиграят решаваща роля в лечението на латентното и активното заболяване.[123]
За да се насърчават бъдещите открития, изследователите и политиците популяризират нови икономически модели за разработване на ваксини, включващи цени, данъчни стимули и предварителни търговски договорености.[124][125] Няколко групи са ангажирани с изследвания, включително и Партньорството за спиране на туберкулозата (Stop TB Partnership),[126] Южноафриканската инициатива за туберкулозна ваксина и Световната фондация Aeras за ваксиниране за туберкулоза (Aeras Global TB Vaccine Foundation).[127] Световната фондация Aeras за ваксиниране за туберкулоза получи дарение от повече от 280 милиона щатски долара от Фондацията на Бил и Мелинда Гейтс за разработване и лицензиране на подобрена ваксина срещу туберкулоза за страните с висока заболеваемост.[128][129]
Туберкулоза при животните[редактиране | редактиране на кода]
Микобактериите заразяват много различни видове животни, включително птици,[130] гризачи [131] и влечуги.[132] Подвидовете на „микобактериум туберкулозис“ са рядко срещани сред дивите животни.[133] Сравнително успешно беше усилието за унищожаване на туберкулозата сред едрия рогат добитък, причинена от „микобактериум бовис“ (говежда микобактерия) сред говедата и стадата от елени в Нова Зеландия.[134] По-малко успешни бяха усилията във Великобритания.[135][136]
Известни личности, заболели от туберкулоза[редактиране | редактиране на кода]
- Нелсън Мандела – първия чернокож президент на ЮАР
Известни личности, починали от туберкулоза[редактиране | редактиране на кода]
- Йордан Йовков – български писател
- Сава Филаретов – български просветител
- Марин Дринов – български историк
- Любен Каравелов – български поет
- Христо Смирненски – български поет
- Екатерина Ненчева – българска поетеса
- Луций Елий – римски император
- Джовани Перголези – италиански композитор, цигулар и органист
- Махмуд II – султан на Османската империя
- Алфонсо XII – крал на Испания
- Фридрих Шилер – немски поет, историк и драматург
- Луи Брайл – създател на азбуката за незрящи
- Фредерик Шопен – полски композитор
- Симон Боливар – латиноамерикански революционер и политик
- Джоузеф Конрад – британски писател
- Хенри Дейвид Торо – американски писател
- Франц Кафка – австрийски писател
- Антон Павлович Чехов – руски писател и драматург
- Максим Горки – руски писател
- Иля Илф – руски писател-сатирик.
- Гаврило Принцип – босненски сърбин, убил австрийския ерцхерцог Франц Фердинанд
- Дан Колов или Дончо Колев Данев – първият български кечист
- Джон Кийтс – английски писател – романтик
- Владимир Дьомин – съветски футболист
- Георги Раковски – български революционер
- Васил Априлов - български дарител
Бележки[редактиране | редактиране на кода]
- ↑ Konstantinos A. Testing for tuberculosis // Australian Prescriber 33 (1). 2010. с. 12 – 18.
- ↑ а б в г Tuberculosis Fact sheet N°104 // World Health Organization, November 2010. Архивиран от оригинала на 2010-01-02. Посетен на 26 юли 2011.
- ↑ а б в World Health Organization. Epidemiology // Global tuberculosis control: epidemiology, strategy, financing. 2009. ISBN 978-92-4-156380-2. с. 6 – 33. Посетен на 12 ноември 2009.[неработеща препратка]
- ↑ а б в г д World Health Organization. The sixteenth global report on tuberculosis // 2011. Архивиран от оригинала на 2012-01-10.
- ↑ а б в г д е ж з и к л м н о п Kumar, Vinay; Abbas, Abul K.; Fausto, Nelson; & Mitchell, Richard N. Robbins Basic Pathology. 8th. Saunders Elsevier, 2007. ISBN 978-1-4160-2973-1. с. 516 – 522.
- ↑ а б в г д е ж з и к л м н о п р с т у ф х Lawn, SD и др. Tuberculosis // Lancet 378 (9785). 2 юли 2011. DOI:10.1016/S0140-6736(10)62173-3. с. 57 – 72.
- ↑ а б в г д е ж з Dolin, [edited by] Gerald L. Mandell, John E. Bennett, Raphael. Mandell, Douglas, and Bennett's principles and practice of infectious diseases. 7th. Philadelphia, PA, Churchill Livingstone/Elsevier, 2010. ISBN 978-0-443-06839-3. с. Chapter 250.
- ↑ Southwick, Frederick. Infectious Diseases: A Clinical Short Course, 2nd ed. McGraw-Hill Medical Publishing Division, 2007. ISBN 0071477225. с. 313 – 314.
- ↑ Cox R. Quantitative relationships for specific growth rates and macromolecular compositions of Mycobacterium tuberculosis, Streptomyces coelicolor A3(2) and Escherichia coli B/r: an integrative theoretical approach // Microbiology 150 (Pt 5). 2004. DOI:10.1099/mic.0.26560-0. с. 1413 – 1426. Архивиран от оригинала на 2007-03-10.
- ↑ Niederweis M, Danilchanka O, Huff J, Hoffmann C, Engelhardt H. Mycobacterial outer membranes: in search of proteins // Trends in Microbiology 18 (3). Март 2010. DOI:10.1016/j.tim.2009.12.005. с. 109 – 16.
- ↑ а б Madison B. Application of stains in clinical microbiology // Biotech Histochem 76 (3). 2001. DOI:10.1080/714028138. с. 119 – 25.
- ↑ Parish T, Stoker N. Mycobacteria: bugs and bugbears (two steps forward and one step back) // Molecular Biotechnology 13 (3). 1999. DOI:10.1385/MB:13:3:191. с. 191 – 200.
- ↑ Medical Laboratory Science: Theory and Practice. New Delhi, Tata McGraw-Hill, 2000. ISBN 0-07-463223-X. с. 473.
- ↑ Piot, editors, Richard D. Semba, Martin W. Bloem; foreword by Peter. Nutrition and health in developing countries. 2nd ed. Totowa, NJ, Humana Press, 2008. ISBN 978-1-934115-24-4. с. 291.
- ↑ van Soolingen D, Hoogenboezem T, de Haas PE, et al. A novel pathogenic taxon of the Mycobacterium tuberculosis complex, Canetti: characterization of an exceptional isolate from Africa // Int. J. Syst. Bacteriol. 47 (4). Октомври 1997. DOI:10.1099/00207713-47-4-1236. с. 1236 – 45. Архивиран от оригинала на 2010-05-26. Посетен на 2010-02-23.
- ↑ Niemann S, Rüsch-Gerdes S, Joloba ML, et al. Mycobacterium africanum subtype II is associated with two distinct genotypes and is a major cause of human tuberculosis in Kampala, Uganda // J. Clin. Microbiol. 40 (9). Септември 2002. DOI:10.1128/JCM.40.9.3398-3405.2002. с. 3398 – 405.
- ↑ Niobe-Eyangoh SN, Kuaban C, Sorlin P, et al. Genetic biodiversity of Mycobacterium tuberculosis complex strains from patients with pulmonary tuberculosis in Cameroon // J. Clin. Microbiol. 41 (6). Юни 2003. DOI:10.1128/JCM.41.6.2547-2553.2003. с. 2547 – 53.
- ↑ Thoen C, Lobue P, de Kantor I. The importance of Mycobacterium bovis as a zoonosis // Vet. Microbiol. 112 (2 – 4). Февруари 2006. DOI:10.1016/j.vetmic.2005.11.047. с. 339 – 45.
- ↑ Pfyffer GE, Auckenthaler R, van Embden JD, van Soolingen D. Mycobacterium canettii, the smooth variant of M. tuberculosis, isolated from a Swiss patient exposed in Africa // Emerging Infect. Dis. 4 (4). 1998. с. 631 – 4.
- ↑ Niemann S, Richter E, Dalügge-Tamm H, Schlesinger H, Graupner D, Königstein B, Gurath G, Greinert U, Rüsch-Gerdes S. Two cases of Mycobacterium microti derived tuberculosis in HIV-negative immunocompetent patients // Emerg Infect Dis 6 (5). 2000. DOI:10.3201/eid0605.000516. с. 539 – 42.
- ↑ American Thoracic Society. Diagnosis and treatment of disease caused by nontuberculous mycobacteria. This official statement of the American Thoracic Society was approved by the Board of Directors, March 1997. Medical Section of the American Lung Association // Am J Respir Crit Care Med 156 (2 Pt 2). 1997. с. S1–25.
- ↑ Rothschild B, Martin L, Lev G, Bercovier H, Bar-Gal G, Greenblatt C, Donoghue H, Spigelman M, Brittain D. Mycobacterium tuberculosis complex DNA from an extinct bison dated 17 000 years before the present // Clin Infect Dis 33 (3). 2001. DOI:10.1086/321886. с. 305 – 11.
- ↑ Pearce-Duvet J. The origin of human pathogens: evaluating the role of agriculture and domestic animals in the evolution of human disease // Biol Rev Camb Philos Soc 81 (3). 2006. DOI:10.1017/S1464793106007020. с. 369 – 82.
- ↑ Ernst JD, Trevejo-Nuñez G, Banaiee N. Genomics and the evolution, pathogenesis, and diagnosis of tuberculosis // J. Clin. Invest. 117 (7). Юли 2007. DOI:10.1172/JCI31810. с. 1738 – 45.
- ↑ Hershkovitz I, Donoghue HD, Minnikin DE, Besra GS, Lee OY-C, et al. Detection and Molecular Characterization of 9000-Year-Old Mycobacterium tuberculosis from a Neolithic Settlement in the Eastern Mediterranean. // PLoS ONE 3 (10). 15 октомври 2008. DOI:10.1371/journal.pone.0003426. с. e3426.
- ↑ Zink A, Sola C, Reischl U, Grabner W, Rastogi N, Wolf H, Nerlich A. Characterization of Mycobacterium tuberculosis complex DNAs from Egyptian mummies by spoligotyping // J Clin Microbiol 41 (1). 2003. DOI:10.1128/JCM.41.1.359-367.2003. с. 359 – 67.
- ↑ „South America: Prehistoric Findings“. Memorias do Instituto Oswaldo Cruz, Vol. 98 (Suppl.I) January 2003.
- ↑ Sledzik P, Bellantoni N. Brief communication: bioarcheological and biocultural evidence for the New England vampire folk belief // Am J Phys Anthropol 94 (2). 1994. DOI:10.1002/ajpa.1330940210. с. 269 – 74. Архивиран от оригинала на 2007-01-09. Посетен на 2009-03-26.
- ↑ Katharine Mary Briggs, An Encyclopedia of Fairies „Consumption“ (Pantheon Books, 1976) p. 80. ISBN 0-394-73467-X
- ↑ Lawlor, Clark. „Transatlantic Consumptions: Disease, Fame and Literary Nationalism in the Davidson Sisters, Southey, and Poe“. Studies in the Literary Imagination, Fall 2003. Available at findarticles.com Архив на оригинала от 2010-09-24 в Wayback Machine..
- ↑ Y. A. Al-Sharrah (2003), „The Arab Tradition of Medical Education and its Relationship with the European Tradition“, Prospects 33 (4), Springer.
- ↑ George Sarton, Introduction to the History of Science.
(cf. Dr. A. Zahoor and Dr. Z. Haq (1997). Quotations From Famous Historians of Science, Cyberistan.) - ↑ David W. Tschanz, MSPH, PhD (August 2003). „Arab Roots of European Medicine“, Heart Views 4 (2).
- ↑ Pliny the Elder, Natural History, quoted at Naphtali Lewis, Meyer Reinhold. Roman Civilization
- ↑ Who Named It? Léon Charles Albert Calmette. Посетен на 6 октомври 2006.
- ↑ Trail R. Richard Morton (1637 – 1698) // Med Hist 14 (2). 1970. с. 166 – 74.
- ↑ Zur Pathogenie der Impetigines. Auszug aus einer brieflichen Mitteilung an den Herausgeber. [Müller’s] Archiv für Anatomie, Physiologie und wissenschaftliche Medicin. 1839, page 82.
- ↑ Kentucky: Mammoth Cave long on history Архив на оригинала от 2008-09-21 в Wayback Machine.. CNN. 27 февруари 2004. Посетен на 8 октомври 2006.
- ↑ McCarthy OR. The key to the sanatoria // J R Soc Med 94 (8). 2001. с. 413 – 7.
- ↑ Tuberculosis through history. Encyclopædia Britannica.
- ↑ Torrey EF and Yolken RH. 2005. Their bugs are worse than their bite. Washington Post, 3 април p. B01., архив на оригинала от 28 април 2013, https://www.webcitation.org/6GCwhaHD6?url=http://birdflubook.com/a.php?id=40, посетен на 2 май 2009
- ↑ Nobel Foundation. The Nobel Prize in Physiology or Medicine 1905. Посетен на 7 октомври 2006.
- ↑ Tuberculosis — Respiratory and Non-respiratory Notifications, England and Wales, 1913 – 2005 // Health Protection Agency Centre for Infections, 21 март 2007. Посетен на 1 август 2007.
- ↑ World Health Organization (WHO). Frequently asked questions about TB and HIV Архив на оригинала от 2012-01-27 в Wayback Machine.. Посетен на 6 октомври 2006.
- ↑ Health ministers to accelerate efforts against drug-resistant TB Архив на оригинала от 2013-12-30 в Wayback Machine.. World Health Organization.
- ↑ World Health Organization. The Stop TB Strategy, case reports, treatment outcomes and estimates of TB burden // Global tuberculosis control: epidemiology, strategy, financing. 2009. ISBN 978-92-4-156380-2. с. 187 – 300. Посетен на 14 ноември 2009. Архив на оригинала от 2009-11-19 в Wayback Machine.
- ↑ Tuberculosis // World Health Organization. 2002. Архивиран от оригинала на 2002-09-07.
- ↑ Fact Sheets: The Difference Between Latent TB Infection and Active TB Disease // Centers for Disease Control, 20 юни 2011. Посетен на 26 юли 2011.
- ↑ а б Skolnik, Richard. Global health 101. 2nd ed. Burlington, MA, Jones & Bartlett Learning, 2011. ISBN 978-0-7637-9751-5. с. 253.
- ↑ а б в Global Tuberculosis Control 2011 // World Health Organization. Архивиран от оригинала на 2011-12-16. Посетен на 15 април 2012.
- ↑ World Health Organization. WHO report 2008: Global tuberculosis control // Архивиран от оригинала на 2008-12-25. Посетен на 13 април 2009.
- ↑ FitzGerald, JM и др. Tuberculosis: 13. Control of the disease among aboriginal people in Canada. // CMAJ: Canadian Medical Association journal = journal de l'Association medicale canadienne 162 (3). 2000 Feb 8. с. 351 – 5.
- ↑ Quah, Stella R.; Carrin, Guy; Buse, Kent; Kristian Heggenhougen. Health Systems Policy, Finance, and Organization. Boston, Academic Press, 2009. ISBN 0-12-375087-3. с. 424.
- ↑ Anne-Emanuelle Birn. Textbook of International Health: Global Health in a Dynamic World. 2009. ISBN 9780199885213. с. 261.
- ↑ World Health Organization. Global tuberculosis control–surveillance, planning, financing WHO Report 2006 // Архивиран от оригинала на 2006-01-07. Посетен на 13 октомври 2006.
- ↑ Chaisson, RE и др. Tuberculosis in Africa--combating an HIV-driven crisis // The New England Journal of Medicine 358 (11). 13 март 2008. DOI:10.1056/NEJMp0800809. с. 1089 – 92.
- ↑ Griffith D, Kerr C. Tuberculosis: disease of the past, disease of the present // J Perianesth Nurs 11 (4). 1996. DOI:10.1016/S1089-9472(96)80023-2. с. 240 – 5.
- ↑ Targeted tuberculin testing and treatment of latent tuberculosis infection. American Thoracic Society // MMWR Recomm Rep 49 (RR–6). Юни 200. с. 1 – 51.
- ↑ van Zyl Smit, RN и др. Global lung health: the colliding epidemics of tuberculosis, tobacco smoking, HIV and COPD. // The European respiratory journal: official journal of the European Society for Clinical Respiratory Physiology 35 (1). 2010 Jan. с. 27 – 33. These analyses indicate that smokers are almost twice as likely to be infected with TB and to progress to active disease (RR of ∼1.5 for latent TB infection (LTBI) and RR of ∼2.0 for TB disease). Smokers are also twice as likely to die from TB (RR of ∼2.0 for TB mortality), but data are difficult to interpret because of heterogeneity in the results across studies.
- ↑ Restrepo, BI. Convergence of the tuberculosis and diabetes epidemics: renewal of old acquaintances // Clinical infectious diseases: an official publication of the Infectious Diseases Society of America 45 (4). 15 август 2007. DOI:10.1086/519939. с. 436 – 8.
- ↑ Möller, M и др. Current findings, challenges and novel approaches in human genetic susceptibility to tuberculosis // Tuberculosis (Edinburgh, Scotland) 90 (2). 2010 Mar. DOI:10.1016/j.tube.2010.02.002. с. 71 – 83.
- ↑ Cole E, Cook C. Characterization of infectious aerosols in health care facilities: an aid to effective engineering controls and preventive strategies // Am J Infect Control 26 (4). 1998. DOI:10.1016/S0196-6553(98)70046-X. с. 453 – 64.
- ↑ Nicas M, Nazaroff WW, Hubbard A. Toward understanding the risk of secondary airborne infection: emission of respirable pathogens // J Occup Environ Hyg 2 (3). 2005. DOI:10.1080/15459620590918466. с. 143 – 54.
- ↑ а б Ahmed N, Hasnain S. Molecular epidemiology of tuberculosis in India: Moving forward with a systems biology approach // Tuberculosis 91 (5). 2011. DOI:10.1016/j.tube.2011.03.006. с. 407 – 3.
- ↑ а б Core Curriculum on Tuberculosis: What the Clinician Should Know // Centers for Disease Control and Prevention (CDC), Division of Tuberculosis Elimination, 2011.
- ↑ Causes of Tuberculosis // Mayo Clinic, 21 декември 2006. Архивиран от оригинала на 2006-09-02. Посетен на 19 октомври 2007.
- ↑ World Health Organization. Global Tuberculosis Control Report, 2006 – Annex 1 Profiles of high-burden countries (PDF) // Архивиран от оригинала на 2006-07-16. Посетен на 13 октомври 2006.
- ↑ Centers for Disease Control and Prevention. 2005 Surveillance Slide Set // 12 септември 2006. Посетен на 13 октомври 2006.
- ↑ а б editors, Arch G. Mainous III, Claire Pomeroy,. Management of antimicrobials in infectious diseases: impact of antibiotic resistance. 2nd rev. ed. Totowa, N.J., Humana, 2009. ISBN 978-1-60327-238-4. с. 74.
- ↑ Houben E, Nguyen L, Pieters J. Interaction of pathogenic mycobacteria with the host immune system // Curr Opin Microbiol 9 (1). 2006. DOI:10.1016/j.mib.2005.12.014. с. 76 – 85.
- ↑ Khan. Essence Of Paediatrics. Elsevier India, 2011. ISBN 978-81-312-2804-3. с. 401.
- ↑ Herrmann J, Lagrange P. Dendritic cells and Mycobacterium tuberculosis: which is the Trojan horse? // Pathol Biol (Paris) 53 (1). 2005. DOI:10.1016/j.patbio.2004.01.004. с. 35 – 40.
- ↑ Agarwal R, Malhotra P, Awasthi A, Kakkar N, Gupta D. Tuberculous dilated cardiomyopathy: an under-recognized entity? // BMC Infect Dis 5 (1). 2005. DOI:10.1186/1471-2334-5-29. с. 29.
- ↑ а б в Grosset J. Mycobacterium tuberculosis in the Extracellular Compartment: an Underestimated Adversary // Antimicrob Agents Chemother 47 (3). 2003. DOI:10.1128/AAC.47.3.833-836.2003. с. 833 – 6.
- ↑ Crowley, Leonard V. An introduction to human disease: pathology and pathophysiology correlations. 8th ed. Sudbury, Mass., Jones and Bartlett, 2010. ISBN 978-0-7637-6591-0. с. 374.
- ↑ Anthony, Harries. TB/HIV a Clinical Manual. 2nd. Geneva, World Health Organization, 2005. ISBN 978-92-4-154634-8. с. 75.
- ↑ а б Ghosh, editors-in-chief, Thomas M. Habermann, Amit K. Mayo Clinic internal medicine: concise textbook. Rochester, MN, Mayo Clinic Scientific Press, 2008. ISBN 978-1-4200-6749-1. с. 789.
- ↑ Jacob, JT и др. Acute forms of tuberculosis in adults. // The American journal of medicine 122 (1). 2009 Jan. с. 12 – 7.
- ↑ Schiffman G. Tuberculosis Symptoms // eMedicine Health, 15 януари 2009.
- ↑ а б в г al]., edited by Peter G. Gibson; section editors, Michael Abramson... [et. Evidence-based respiratory medicine. 1. publ. Oxford, Blackwell, 2005. ISBN 978-0-7279-1605-1. с. 321.
- ↑ Behera, D. Textbook of pulmonary medicine. 2nd ed. New Delhi, Jaypee Brothers Medical Pub., 2010. ISBN 978-81-8448-749-7. с. 457. Архивиран от оригинала на 2013-07-18.
- ↑ Jindal, editor-in-chief SK. Textbook of pulmonary and critical care medicine. New Delhi, Jaypee Brothers Medical Publishers. ISBN 978-93-5025-073-0. с. 549.
- ↑ а б Golden MP, Vikram HR. Extrapulmonary tuberculosis: an overview // American family physician 72 (9). 2005. с. 1761 – 8.
- ↑ Kabra, [edited by] Vimlesh Seth, S.K. Essentials of tuberculosis in children. 3rd ed. New Delhi, Jaypee Bros. Medical Publishers, 2006. ISBN 978-81-8061-709-6. с. 249. Архивиран от оригинала на 2013-07-18.
- ↑ Kumar V, Abbas AK, Fausto N, Mitchell RN. Robbins Basic Pathology. 8th. Saunders Elsevier, 2007. ISBN 978-1-4160-2973-1. с. 516 – 522.
- ↑ Lambert M и др. Recurrence in tuberculosis: relapse or reinfection? // Lancet Infect Dis 3 (5). 2003. DOI:10.1016/S1473-3099(03)00607-8. с. 282 – 7.
- ↑ Wang, JY и др. Prediction of the tuberculosis reinfection proportion from the local incidence // The Journal of infectious diseases 196 (2). 15 юли 2007. DOI:10.1086/518898. с. 281 – 8.
- ↑ а б Bento, J и др. [Diagnostic tools in tuberculosis]. // Acta medica portuguesa 24 (1). 2011 Jan-Feb. с. 145 – 54.
- ↑ а б в г Escalante, P. In the clinic. Tuberculosis. // Annals of internal medicine 150 (11). 2009 Jun 2. с. ITC61-614; quiz ITV616.
- ↑ Metcalfe, JZ и др. Interferon-γ release assays for active pulmonary tuberculosis diagnosis in adults in low – and middle-income countries: systematic review and meta-analysis. // The Journal of infectious diseases 204 Suppl 4. 2011 Nov 15. с. S1120-9.
- ↑ Sester, M и др. Interferon-γ release assays for the diagnosis of active tuberculosis: a systematic review and meta-analysis. // The European respiratory journal: official journal of the European Society for Clinical Respiratory Physiology 37 (1). 2011 Jan. с. 100 – 11.
- ↑ Chen, J и др. Interferon-gamma release assays for the diagnosis of active tuberculosis in HIV-infected patients: a systematic review and meta-analysis. // PloS one 6 (11). 2011. с. e26827.
- ↑ Sester, M и др. Interferon-γ release assays for the diagnosis of active tuberculosis: a systematic review and meta-analysis. // The European respiratory journal: official journal of the European Society for Clinical Respiratory Physiology 37 (1). 2011 Jan. с. 100 – 11.
- ↑ Diseases, Special Programme for Research & Training in Tropical. Diagnostics for tuberculosis: global demand and market potential. Geneva, World Health Organization on behalf of the Special Programme for Research and Training in Tropical Diseases, 2006. ISBN 978-92-4-156330-7. с. 36.
- ↑ а б National Institute for Health and Clinical Excellence. Clinical guideline 117: Tuberculosis. London, 2011.
- ↑ Steingart, KR и др. Commercial serological tests for the diagnosis of active pulmonary and extrapulmonary tuberculosis: an updated systematic review and meta-analysis. // PLoS medicine 8 (8). 2011 Aug. DOI:10.1371/journal.pmed.1001062. с. e1001062.
- ↑ Rothel J, Andersen P. Diagnosis of latent Mycobacterium tuberculosis infection: is the demise of the Mantoux test imminent? // Expert Rev Anti Infect Ther 3 (6). 2005. DOI:10.1586/14787210.3.6.981. с. 981 – 93.
- ↑ Шаблон:NICE
- ↑ Pai M, Zwerling A, Menzies D. Systematic Review: T-Cell–based Assays for the Diagnosis of Latent Tuberculosis Infection: An Update // Ann. Intern. Med. 149 (3). 2008. с. 1 – 9.
- ↑ Jindal, editor-in-chief SK. Textbook of pulmonary and critical care medicine. New Delhi, Jaypee Brothers Medical Publishers. ISBN 978-93-5025-073-0. с. 544.
- ↑ Amicosante, M и др. Rational use of immunodiagnostic tools for tuberculosis infection: guidelines and cost effectiveness studies. // The new microbiologica 33 (2). 2010 Apr. с. 93 – 107.
- ↑ Brennan PJ, Nikaido H. The envelope of mycobacteria // Annu. Rev. Biochem. 64. 1995. DOI:10.1146/annurev.bi.64.070195.000333. с. 29 – 63.
- ↑ а б Menzies, D и др. Recent developments in treatment of latent tuberculosis infection. // The Indian journal of medical research 133. 2011 Mar. с. 257 – 66.
- ↑ Arch G., III Mainous. Management of Antimicrobials in Infectious Diseases: Impact of Antibiotic Resistance. Humana Pr, 2010. ISBN 1-60327-238-0. с. 69.
- ↑ Volmink J, Garner P. Directly observed therapy for treating tuberculosis // Cochrane Database Syst Rev (4). 2007. DOI:10.1002/14651858.CD003343.pub3. с. CD003343.
- ↑ Liu, Q и др. Reminder systems and late patient tracers in the diagnosis and management of tuberculosis. // Cochrane database of systematic reviews (Online) (4). 2008 Oct 8. с. CD006594.
- ↑ O'Brien R. Drug-resistant tuberculosis: etiology, management and prevention // Semin Respir Infect 9 (2). 1994. с. 104 – 12.
- ↑ Centers for Disease Control and Prevention (CDC). Emergence of Mycobacterium tuberculosis with extensive resistance to second-line drugs—worldwide, 2000 – 2004 // MMWR Morb Mortal Wkly Rep 55 (11). 2006. с. 301 – 5.
- ↑ Maryn McKenna. Totally Resistant TB: Earliest Cases in Italy // Wired, 12 януари 2012. Посетен на 12 януари 2012.
- ↑ McShane, H. Tuberculosis vaccines: beyond bacille Calmette–Guérin // Philosophical transactions of the Royal Society of London. Series B, Biological sciences 366 (1579). 12 октомври 2011. DOI:10.1098/rstb.2011.0097. с. 2782 – 9.
- ↑ Vaccine and Immunizations: TB Vaccine (BCG) // Centers for Disease Control and Prevention, 2011. Архивиран от оригинала на 2011-11-17. Посетен на 26 юли 2011.
- ↑ BCG Vaccine Usage in Canada – Current and Historical // Public Health Agency of Canada. Септември 2010. Архивиран от оригинала на 2012-03-30. Посетен на 30 декември 2011.
- ↑ а б Teo, SS и др. Does BCG have a role in tuberculosis control and prevention in the United Kingdom? // Archives of Disease in Childhood 91 (6). 2006 Jun. DOI:10.1136/adc.2005.085043. с. 529 – 31.
- ↑ The Global Plan to Stop TB // World Health Organization, 2011. Посетен на 13 юни 2011.
- ↑ Warrell, ed. by D. J. Weatherall... [4. + 5. ed.] ed. by David A. Sections 1 – 10. 4. ed., paperback. Oxford [u.a.], Oxford Univ. Press, 2005. ISBN 978-0-19-857014-1. с. 560.
- ↑ Lawn, SD и др. Xpert® MTB/RIF assay: development, evaluation and implementation of a new rapid molecular diagnostic for tuberculosis and rifampicin resistance. // Future microbiology 6 (9). 2011 Sep. с. 1067 – 82.
- ↑ WHO says Cepheid rapid test will transform TB care // Reuters. 8 декември 2010.
- ↑ Lienhardt, C и др. What research is needed to stop TB? Introducing the TB Research Movement. // PLoS medicine 8 (11). 2011 Nov. DOI:10.1371/journal.pmed.1001135. с. e1001135.
- ↑ Anurag Bhargava, Lancelot Pinto, Madhukar Pai. Mismanagement of tuberculosis in India: Causes, consequences, and the way forward // Hypothesis 9 (1). 2011. с. e7. Архивиран от оригинала на 2020-01-12. Посетен на 2014-07-23.
- ↑ Amdekar, Y. Changes in the management of tuberculosis. // Indian journal of pediatrics 76 (7). 2009 Jul. с. 739 – 42.
- ↑ а б в Martín Montañés, C и др. New tuberculosis vaccines. // Enfermedades infecciosas y microbiologia clinica 29 Suppl 1. 2011 Mar. DOI:10.1016/S0213-005X(11)70019-2. с. 57 – 62.
- ↑ Ibanga H, Brookes R, Hill P, Owiafe P, Fletcher H, Lienhardt C, Hill A, Adegbola R, McShane H. Early clinical trials with a new tuberculosis vaccine, MVA85A, in tuberculosis-endemic countries: issues in study design // Lancet Infect Dis 6 (8). 2006. DOI:10.1016/S1473-3099(06)70552-7. с. 522 – 8.
- ↑ Kaufmann SH. Future vaccination strategies against tuberculosis: Thinking outside the box // Immunity 33 (4). 2010. DOI:10.1016/j.immuni.2010.09.015. с. 567 – 77.
- ↑ Webber D, Kremer M. Stimulating Industrial R&D for Neglected Infectious Diseases: Economic Perspectives // Bulletin of the World Health Organization 79 (8). 2001. с. 693 – 801. Архивиран от оригинала на 2007-09-26.
- ↑ Barder O, Kremer M, Williams H. Advance Market Commitments: A Policy to Stimulate Investment in Vaccines for Neglected Diseases // The Economists' Voice 3 (3). 2006. DOI:10.2202/1553-3832.1144. Архивиран от оригинала на 2006-11-05. Посетен на 2014-07-23.
- ↑ Economic, Department of и др. Achieving the global public health agenda: dialogues at the Economic and Social Council. New York, United Nations, 2009. ISBN 978-92-1-104596-3. с. 103. Архивиран от оригинала на 2013-07-18.
- ↑ Jong, [edited by] Jane N. Zuckerman, Elaine C. Travelers' vaccines. 2nd ed. Shelton, CT, People's Medical Pub. House, 2010. ISBN 978-1-60795-045-5. с. 319.
- ↑ Bill and Melinda Gates Foundation Announcement. Gates Foundation Commits $82.9 Million to Develop New Tuberculosis Vaccines // 12 февруари 2004. Архивиран от оригинала на 2009-10-10. Посетен на 2014-07-23.
- ↑ Nightingale, Katherine. Gates foundation gives US$280 million to fight TB // 19 септември 2007.
- ↑ Shivaprasad, HL и др. Pathology of mycobacteriosis in birds. // The veterinary clinics of North America. Exotic animal practice 15 (1). 2012 Jan. с. 41 – 55, v-vi.
- ↑ Reavill, DR и др. Mycobacterial lesions in fish, amphibians, reptiles, rodents, lagomorphs, and ferrets with reference to animal models. // The veterinary clinics of North America. Exotic animal practice 15 (1). 2012 Jan. с. 25 – 40, v.
- ↑ Mitchell, MA. Mycobacterial infections in reptiles. // The veterinary clinics of North America. Exotic animal practice 15 (1). 2012 Jan. с. 101 – 11, vii.
- ↑ Wobeser, Gary A. Essentials of disease in wild animals. 1st ed. Ames, Iowa [u.a.], Blackwell Publ., 2006. ISBN 978-0-8138-0589-4. с. 170.
- ↑ Ryan, TJ и др. Advances in understanding disease epidemiology and implications for control and eradication of tuberculosis in livestock: the experience from New Zealand. // Veterinary microbiology 112 (2 – 4). 2006 Feb 25. с. 211 – 9.
- ↑ White, PC и др. Control of bovine tuberculosis in British livestock: there is no 'silver bullet'. // Trends in microbiology 16 (9). 2008 Sep. с. 420 – 7.
- ↑ Ward, AI и др. Farm husbandry and badger behaviour: opportunities to manage badger to cattle transmission of Mycobacterium bovis? // Preventive veterinary medicine 93 (1). 2010 Jan 1. с. 2 – 10.
Вижте също[редактиране | редактиране на кода]
- Уикипедия:Медицина/Translation/Tuberculosis- превод на български на английската статия
|
