Злато
Златото е химичен елемент с атомен номер 79 и означение Au. То е тежък, мек, блестящ, и ковък метал. Провежда електричеството. Има яркожълт цвят и блясък, традиционно смятан за привлекателен. Не ръждясва във въздуха и във водата.
Златото е преходен метал. Намира се в период 6, група 11 на периодичната система.При нормални условия е в твърдо агрегатно състояние. То е един от най-слабо активните елементи. По тази причина се среща често в самородна форма – като златни зърна и жили в скалите или в алувиални отлагания. По-рядко е съставна част на химични съединения, образуващи минерали, най-често в съединение с телура.
Златото е устойчиво на действието на най-силните киселини поотделно, но може да бъде разтворено в смес на азотна и солна киселина, наричана по тази причина царска вода. То се разтваря и в алкални разтвори на цианиди, които намират приложение в добивната промишленост, както и в живак, образувайки амалгамни сплави. Златото е неразтворимо в азотна киселина, която разтваря повечето метали, включително среброто. Този факт се използва за установяване на наличието на злато чрез т. нар. киселинна проба.
Още отпреди появата на писана история златото е ценен и много търсен благороден метал, използван като парично средство, в бижутерията и за изработване на различни предмети на изкуството. Златните стандарти са най-често срещаната основа на паричната политика в историята на човечеството до първата половина на XX век, когато започват да отстъпват на фиатните пари.
Количеството злато, добито от началото на човешката история до 2011 г., се оценява на 171 хиляди тона, от които 59% са произведени след 1950 г.[3] Около 50% от новопроизведеното злато се използва в бижутерията, 40% – като инвестиция и 10% – в промишлеността.[4] Добрата ковкост, проводимост, устойчивостта на корозия и слабата химическа активност правят златото подходящо за различни практически приложения в стоматологията, електрониката и други области.
Наименование
Българската дума „злато“, както и сродните наименования на метала в повечето славянски и балтийски езици (сърбохърватски, словенски, чешки и словашки: „злато“/„zlato“; руски и украински: „золото“; беларуски: „золата“; полски: „złoto“; латвийски: „zelts“), произлиза от праиндоевропейския корен *g'helto- („жълт“, „зелен“).[5] Със същия произход са и думите „зелен“ и „злак“.[5] Чрез различна промяна на праиндоевропейския корен *g'helto- са образувани и наименованията на златото в повечето германски езици (английски и немски: „gold“; датски и шведски: „guld“; нидерландски: „goud“).[6]
Символът на златото Au е получен от латинското му наименование aurum, което според различни източници означава „жълто“ или „светла зора“, и е родствено с „Аврора“ (Aurora) – утринна заря. Според определенията в съвременните латински речници смисълът на думата aurum се простира само до метала злато.
Свойства
Физични свойства

Златото е най-ковкият метал – един грам от него може да бъде изкован в лист с площ един квадратен метър. Златното фолио може да бъде направено толкова тънко, че да стане прозрачно, като преминаващата през него светлина е зеленикавосиня, тъй като златото отразява силно жълтото и червеното.[7] Такива полупрозрачни листове отразяват и голяма част от инфрачервената светлина, поради което се използват като инфрачервени щитове във визьорите на топлозащитни костюми и скафандри.[8]
Златото е добър проводник на топлината и електричеството. То има голяма плътност – 19,3 тона на кубичен метър. За сравнение плътността на оловото е 11,34 t/m3, а тази на най-тежкия елемент – осмия – е 22,610 t/m3. Златото има коефициент на линейно разширение 0,0000142 K−1 и коефициент на обемно разширение 0,0000426 K−1, а специфичната му топлоемкост e 128 J/(kg·K)
Златото лесно образува сплави с други метали. Това се използва за промяна на твърдостта и други свойства на метала, за контролиране на температурата на топене или за оцветяване в специфични цветове.[9]
Цвят
За разлика от повечето метали, които в чист вид са сиви или сребристобели на цвят, златото е жълто. Този цвят се дължи на плътността на слабо свързаните (валентни) електрони, трептящи в обща среда, която може да се разглежда като квазичастица, наричана плазмон. При повечето метали честотата на това трептене е в ултравиолетовия обхват, но при златото е във видимия обхват, поради слабите релативистични ефекти, засягащи орбиталите на неговите атоми.[10][11] На подобни ефекти се дължи и златистият отенък на цезия.
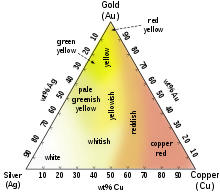
Сплавите на златото могат да имат различен цвят, както е показано на триъгълната диаграма на сплавите му със среброто и медта. Такова цветно злато намира приложение в бижутерията, където различните цветове се използват с декоративна цел. Например, сплавите на злато с паладий или никел имат бял цвят и намират широко приложение в бижутерията. По-рядко се използват сплави с други елементи, като манган, алуминий, желязо или индий, с които се получават необичайни цветове със специфично приложение.[12]
Химични свойства
Златото не реагира химически с въздуха, влагата и повечето корозивни вещества, което го прави подходящо за използване в монети и украшения, а също и като защитно покритие на други, по-реактивни метали. Въпреки това златото не е напълно инертно химически. То е неразтворимо в повечето течности, но се разтваря в смес от силни киселини – т. нар. царска вода.
Обичайни степени на окисление на златото са +1 и +3. Златните йони в разтвор се редуцират и утаяват чрез добавяне на друг метал като редукционен агент. Добавеният метал се окислява и се разтваря, измествайки златото от разтвора и давайки му възможност да се отдели като твърда утайка. Златото с висока чистота няма вкус и мирис, което е свързано с неговата устойчивост на корозия: вкусът на металите се дължи на образуваните в разтвора метални йони.[13]
Изотопи
Златото има само един стабилен изотоп, 197Au – единственият срещан в природата. Синтезирани са 36 други радиоактивни изотопа с атомни маси от 169 до 205. Най-устойчив сред тях е 195Au, който има период на полуразпад 186,1 дена. Най-неустойчив е 171Au, при който протича протонен разпад с период на полуразпад 30 µs.
Повечето радиоактивни изотопи на златото с атомна маса под 197 се разпадат чрез съчетание от протонен разпад, алфа-разпад и позитронен бета-разпад (β+). Изключения са 195Au, който се трансформира чрез поглъщане на електрони, и 196Au, при който е налице най-често поглъщане на електрони (93%) с ограничен електронен бета-разпад (β-).[14] Всички радиоактивни изотопи на златото с атомна маса над 197 се разпадат чрез електронен бета-разпад (β-).[15]
Освен тези изотопи са известни поне 32 ядрени изомера с атомни маси от 170 до 200. В този диапазон само 178Au, 180Au, 181Au, 182Au и 188Au нямат изомери. Най-устойчивият изомер на златото е 198 m2Au с период на полуразпад 2,27 дни, а най-неустойчив е 177 m2Au с период на полуразпад само 7 ns. 184 m1Au има три пътя на разпад: β+ разпад, изомерен преход и алфа-разпад – повече, отколкото всеки друг изомер или изотоп на златото.[15]
Получаване
Златото се среща рядко в чист вид, но лесно могат да бъдат изолирани негови съединения с други елементи. Златото се извлича от златоносния пясък при обработка с разтвори на натриева основа и натриев цианид в присъствие на кислород.
Разпространен метод за извличане на златото, когато е във вид на прах, е с помощта на живак. Живакът образува амалгама със златото. Течните живачни отпадъци обаче тровят реките и хранителните вериги, а при вдишване носят риск за здравето.
Добив на злато
Известна е обработката на злато още от петото хилядолетие преди новата ера. За цялата история на развитие на човешката цивилизация са добити около 161 хиляди тона (по оценка от 2011 г.).[16]
През 2007 г. в света са добити 2,38 хил. тона злато, а през 2008 – 2,33 хил. тона. Лидери в добива на злато са:[17]:
| Място | Страна | Добив 2006 (т) | Добив 2007 (т) | Добив 2008 (т) | Добив 2009 (т) | Добив 2010 (т) | Добив 2011 (т) | Добив 2012 (т) | Добив 2013 (т) |
|---|---|---|---|---|---|---|---|---|---|
| 1 | 245 | 275 | 295 | 320 | 345 | 362 | 403 | 420 | |
| 2 | 272 | 252 | 250 | 198 | 189 | 181 | 160 | 145 | |
| 3 | 252 | 238 | 230 | 223 | 231 | 234 | 235 | 227 | |
| 4 | 244 | 246 | 225 | 222 | 261 | 258 | 250 | 255 | |
| 5 | 203 | 170 | 175 | 182 | 164 | 164 | 161 | 150 | |
| 6 | 159 | 157 | 165 | 191 | 192 | 200 | 218 | 220 | |
| 7 | 104 | 101 | 100 | 97 | 91 | 97 | 104 | 120 | |
| 8 | 164 | 118 | 90 | 130 | 120 | 96 | 59 | 60 | |
| 9 | 85 | 85 | 90 | 90 | 91 | 93 | 93 | ||
| 10 | 84 | 84 | 86 | 82 | 80 | 87 | 85 | ||
| 11 | 65 | 65 | 66 | 68 | 66 | 53 | 62 | ||
| 12 | 42 | 42 | 41 | 38 | 45 | 50 | 55 | ||
| 13 | 39 | 41 | 51 | 73 | 84 | 97 | 100 | ||
| 14 | 40 | 40 | 60 | 58 | 62 | 65 | 75 | ||
| други страни | 818 | 471 | 446 | 490 | 559 | 640 | 655 | 700 | |
| Общо тона годишен добив | 2460 | 2383 | 2264 | 2447 | 2561 | 2660 | 2690 | 2767 | |
| Цена млн. $ за тон | 16.5 | 20.3 | 26.8 | 28 | 35 | 45.2 | 51.4 | 53.3 | |
| Общо милиарда $ | 40.59 | 48.375 | 60.675 | 68.516 | 89.635 | 120.232 | 138.266 | 147.481 |
Най-големите държавни златни запаси в света
В долната таблица са показани само държавните златни запаси (и златният запас на МВФ). Трябва да се отчете, че в много страни частни лица притежават значително по-голям по обем злато в сравнение със златният запас на съответните държави. Например, през декември 2011 г. частното злато в Индия е 18000 тона[18], като държавният златен запас през 2013 г. е 557.7 тона[19].
Най-големите златни запаси в света през април 2016 г.[20].
| № | Страна/Организация | Злато (тона) |
Процентът на златото в общият обем на държавния валутен резерв (%) |
|---|---|---|---|
| 1 | 8133,5 | 75,3 % | |
| 2 | 3381 | 69 % | |
| 3 | Международен валутен фонд | 2814 | - |
| 4 | 2451,8 | 68,3 % | |
| 5 | 2435,6 | 63,2 % | |
| 6 | 1788,4 | 2,2 % | |
| 7 | 1447 | 15,1 % | |
| 8 | 1040 | 6,8 % | |
| 9 | 765,2 | 2,4 % | |
| 10 | 612,5 | 59,4 % |
Приложения
Паричен обмен

Още от древността златото се използва в много части на света като парично средство за размяна във вид на монети или в друга форма. Тъй като чистото злато е твърде меко за употреба в ежедневния паричен обмен, златните монети обикновено се секат от сплави с примеси на мед, сребро или други метали, които им придават по-голяма твърдост. Така например английските златни монети, в обращение от 1526 г. до 30-те години на XX век, са с чистота 22 карата (91,6%),[21] а американските след 1837 г. – със златно съдържание 90,0% (21,6 карата).[22]
Първите златни монети през Античността се секат в Лидия около 700 г. пр.н.е.[23] Древногръцкият златен талант е с маса между 8,42 и 8,75 грама.[24] След продължителен период на използване на предимно сребърни монети, европейските икономики подновяват масовото сечене на златни монети през XIII-XIV век.[25] През XIX век златото започва да се използва широко като обезпечение на банкноти чрез системата на златния стандарт.
Рязкото нарастване на държавните разходи по време на Първата световна война кара повечето държави, участващи в нея, да финансират дефицитите си за сметка на увеличаване на паричната маса и обезценяване на парите, отказвайки се на практика от златния стандарт. След войната някои страни правят опити да се върнат към него, но след Втората световна война почти всички държави изоставят тази система за сметка на фиатните пари. Последната държава, прибягнала до тази мярка, е Швейцария, която се отказва от задължителното обезпечение на парите със злато през 2000 г.[26]
Инвестиция

Дори след премахването на златния стандарт златото запазва част от монетарните си свойства и някои инвеститори го използват като запас от стойност, като влагат средствата си обикновено в инвестиционни монети или златни кюлчета. Това обикновено се прави като защита срещу инфлация или други икономически сривове. Някои икономисти подлагат на съмнение ефективността на такива вложения.[27]
Тъй като не са предназначени за ежедневна употреба, изискванията към механичните свойства на инвестиционните монети са по-ниски и те обикновено се изготвят с чистота 24 карата (минимум 99,9%, най-често 99,99%), макар че има и изключения. Например, американският златен орел, британският соверен и южноафриканският крюгерранд и днес по традиция използват чистота 22 карата.[28] Инвестиционната монета с най-голяма чистота на златото е канадският златен кленов лист, в който златото е 99,999%.
Най-често използваното кюлче злато е с маса 1 kg и форма, близка до правоъгълен паралелепипед.
Бижутерия

Златото намира широко приложение в бижутерията. Както и при монетите, чистото злато е твърде меко и в бижутерията обикновено се използват различни сплави с чистота 22, 18, 14 или 10 карата, като по този начин се изменят неговата твърдост и дуктилност, температура на топене, цвят и други свойства. Най-често използваният допълнителен метал в тези сплави е медта.[9]
18-каратовото злато, съдържащо 25% мед, често използвано в античната и руската бижутерия, има червеникав цвят, 14-каратовата златно-медна сплав има цвят, почти еднакъв с този на някои бронзови сплави. Синкав цвят може да се получи чрез добавяне на желязо, а лилав – на алуминий, но тези разновидности се използват много рядко, поради по-трудната им обработка.[9]
14 и 18-каратовата сплав със сребро има зеленикаво-жълт цвят. Бялото злато се получава чрез добавяне на паладий или никел, а 18-каратовото злато, съдържащо 17,3% никел, 5,5% цинк и 2,2% мед е сребристо на цвят. От друга страна никелът е токсичен и отделянето му от бялото злато е регулирано в някои страни.[9] Бялото злато, съдържащо паладий, е по-скъпо от съдържащото никел. Висококаратните сплави на бяло злато са много по-устойчиви на корозия от среброто и стърлинга.
Медицина

Според някои изследователи златото е най-старото използвано лекарство.[29] То е известно още на Педаний Диоскурид.[30][31] В същото време токсикологията му не е изцяло изучена.[32]
Преди появата на научната медицина златото е смятано за полезно за здравето поради своята рядкост и красота. Дори някои съвременни езотерични течения и форми на алтернативната медицина приписват на златото лечебни свойства.[33] Някои соли и радиоизотопи на златото действително имат противовъзпалително действие и се използват при артрит и други подобни състояния,[34] както и за лекуване на рак, но като чист метал златото е напълно инертно към химическите вещества в човешкото тяло.
Сплави на златото се използват във възстановителната стоматология за изготвяне на корони и мостове. Ковкостта на златните сплави позволява по-прецизно възстановяване на повърхността на зъба, отколкото при порцелановите корони. Използването на златни корони при видими зъби, като резците, се насърчава при някои култури и се смята за нежелателно при други.
Различни форми на златото намират приложение в някои изследователски методи, използвани в медицината и биологията. Колоидното злато представлява суспензия на златни наночастици, които имат свойството да абсорбират протеинови молекули по своята повърхност. Такива частици, покрити с определени антитела, могат да се използват за откриване на дадени антигени по повърхността на клетките.[35][36]
Златото и негови сплави с паладий се използват като електропроводящо покритие на биологични проби и други непроводящи материали, като пластмаси и стъкло, за да бъдат наблюдавани със сканиращ електронен микроскоп. Покритието, което обикновено се нанася чрез магнетронно разпрашване с аргонова плазма, изпълнява три функции. Много високата електропроводимост на златото отвежда електрическите заряди от пробата, а високата му плътност спира проникването на електроните, ограничавайки дълбочината, до която електронният лъч прониква в образеца. Това подобрява определянето на положението и топографията на повърхността на образеца и увеличава пространствената разделителна способност на изображението. В същото време от златото се отделят голямо количество вторично емитирани електрони, които имат ниска енергия и са най-често използваният източник на сигнал в сканиращите електронни микроскопи.[37]
Хранителна добавка
Златото е регистрирано като хранителна добавка с код Е175.[38] Златно фолио, люспи или прах се използва в някои специални храни, главно в десерти и напитки, като декоративна съставка.[39] Голдвасер („златна вода“) е традиционен билков ликьор, приготвян в Гданск и Швабах, който съдържа частици златно фолио.
В чист вид златото е напълно инертно към химичните вещества в човешкия организъм, не променя вкуса на храните и няма хранителна стойност.[40]
Електротехника
- Златото е незаменимо като материал за електрически контакти. В космическата техника и микроелектрониката проводниците често са златни, а контактни повърхности, съединители, печатни платки и т.н. често се покриват галванично със злато.
Други области на техниката
Любопитни факти
- Сходството между златото и минерала пирит е станало причина пиритът да бъде наречен „златото на глупака“. Разликата между златото и пирита се установява при силен удар с остър предмет. Пиритът ще се надроби, а по златото ще остане дълбока следа от острието.
Бележки
- ↑ Lide 2005.
- ↑ Kelly 2015.
- ↑ World Gold Council 2012.
- ↑ Soos 2011.
- ↑ а б Георгиев 1971, с. 644 – 645.
- ↑ Hesse 2007.
- ↑ webexhibits.org 2009.
- ↑ Mallan 1971, с. 216.
- ↑ а б в г Utilisegold.com 2000a.
- ↑ Math.ucr.edu 2009.
- ↑ Schmidbaur 2005, с. 151 – 161.
- ↑ Utilisegold.com 2000b.
- ↑ Pelouze 1854, с. 280.
- ↑ National Nuclear Data Center 2012.
- ↑ а б Audi 2003, с. 3 – 128.
- ↑ За свою историю человечество добыло 161 тысячу тонн золота – National Geographic Россия
- ↑ Mineral commodity summaries 2009
- ↑ Обзор на пазарите за злато в Индия и Китай
- ↑ Reserve asset statistics
- ↑ Statistics | World Gold Council
- ↑ Lawrence 1948, с. 103.
- ↑ Tucker 1839, с. 393.
- ↑ Friedberg 2009.
- ↑ Seltman 1924.
- ↑ Postan 1967.
- ↑ The New York Times 1999.
- ↑ Feldstein 2009.
- ↑ americansilvereagletoday.com 2010.
- ↑ Kean 2008, с. 112 – 125.
- ↑ Moir 1831, с. 225.
- ↑ Mortier 2006.
- ↑ Merchant 1998, с. 49 – 59.
- ↑ ninemsn 2007.
- ↑ Messori 2004, с. 280 – 301.
- ↑ Faulk 1971, с. 1081 – 1083.
- ↑ Roth 1980, с. 55 – 57.
- ↑ Bozzola 1999, с. 65.
- ↑ Food Standards Agency 2010.
- ↑ Barron's Educational Services 1995.
- ↑ Geology.com 2010.
- Цитирани източници
- Георгиев, Вл. И. (ред.). Български етимологичен речник. Том I. А-З. София, Издателство на Българската академия на науките, 1971. (на български)
- The Ever Popular Krugerrand // americansilvereagletoday.com. americansilvereagletoday.com, 2010. Посетен на 30 август 2011. (на английски)
- Audi, G et al. The NUBASE Evaluation of Nuclear and Decay Properties // Nuclear Physics A 729. Atomic Mass Data Center, 2003. DOI:10.1016/j.nuclphysa.2003.11.001. p. 3 – 128. (на английски)
- The Food Dictionary: Varak // Barron's Educational Services, 1995. Посетен на 27 май 2007. (на английски)
- Bozzola, John J. et al. Electron microscopy: principles and techniques for biologists. Jones & Bartlett Learning, 1999. ISBN 0-7637-0192-0. (на английски)
- Faulk, WP et al. An immunocolloid method for the electron microscope // Immunochemistry 8 (11). 1971. (на английски)
- Feldstein, Martin. Is Gold a Good Hedge? // Project Syndicate, 26 декември 2009. Посетен на 29 декември 2009. (на английски)
- Current EU approved additives and their E Numbers // Food Standards Agency, 2010. Посетен на 4 юни 2010. (на английски)
- Friedberg, A L et al. Gold Coins of the World: From Ancient Times to the Present: an Illustrated Standard Catalog With Valuations. Coin & Currency Institute, 30 юли 2009. ISBN 0871843080. (на английски)
- The Many Uses of Gold // Geology.com, 2010. Посетен на 4 юни 2010. (на английски)
- Hesse, R W. Jewelrymaking Through History: An Encyclopedia. Greenwood Publishing Group, 2007. ISBN 0313335079. (на английски)
- Kean, W. F. et al. Clinical pharmacology of gold // Inflammopharmacology 16 (3). 2008. DOI:10.1007/s10787-007-0021-x. p. 112 – 25. (на английски)
- Lawrence, Thomas Edward. The Mint: A Day-book of the R.A.F. Depot Between August and December 1922, with Later Notes. 1948. (на английски)
- Mallan, Lloyd. Suiting up for space: the evolution of the space suit. John Day Co, 1971. ISBN 978-0-381-98150-1. (на английски)
- Relativity in Chemistry // Math.ucr.edu, 2009. Посетен на 5 април 2009. (на английски)
- Merchant, B. Gold, the Noble Metal and the Paradoxes of its Toxicology // Biologicals 26 (1). 1998. DOI:10.1006/biol.1997.0123. p. 49 – 59. (на английски)
- Messori, L. Gold Complexes in the treatment of Rheumatoid Arthritis // Metal ions and their complexes in medication. CRC Press, 2004. ISBN 9780824753511. (на английски)
- Moir, David Macbeth. Outlines of the ancient history of medicine. 1831. (на английски)
- Mortier, Tom. An experimental study on the preparation of gold nanoparticles and their properties // kuleuven.be. University of Leuven, 2006. Посетен на 16 октомври 2013. (на английски)
- Nudat 2 // National Nuclear Data Center, 2012. Посетен на 12 април 2012. (на английски)
- The healing power of precious metals // ninemsn, 2007. Посетен на 6 юни 2010. (на английски)
- Pelouze, Jules et al. General notions of chemistry. Lippincott, Grambo & Co, 1854. p. 280. (на английски)
- Postan, M M et al. The Cambridge Economic History of Europe: Trade and industry in the Middle Ages. Cambridge University Press, 1967. ISBN 0521087090. (на английски)
- Roth, J. et al. FITC-protein A-gold complex for light and electron microscopic immunocytochemistry // The journal of histochemistry and cytochemistry: official journal of the Histochemistry Society 28 (1). 1980. DOI:10.1177/28.1.6153194. p. 55 – 57. (на английски)
- Schmidbaur, Hubert et al. Understanding gold chemistry through relativity // Chemical Physics 311 (1 – 2). 2005. DOI:10.1016/j.chemphys.2004.09.023. p. 151 – 161. (на английски)
- Seltman, C T. Athens, Its History and Coinage Before the Persian Invasion. 1924. ISBN 0871843080. Посетен на 4 юни 2012. (на английски)
- Soos, Andy. Gold Mining Boom Increasing Mercury Pollution Risk // Oilprice.com. Advanced Media Solutions, 6 януари 2011. Посетен на 26 март 2011. (на английски)
- Swiss Narrowly Vote to Drop Gold Standard // nytimes.com. The New York Times, 19 април 1999. Посетен на 15 октомври 2013. (на английски)
- Tucker, George. The theory of money and banks investigated. 1839. (на английски)
- Gold: causes of color // webexhibits.org. webexhibits.org, 2009. Посетен на 6 юни 2009. (на английски)
- Gold Jewellery Alloys > Utilise Gold. Scientific, industrial and medical applications, products, suppliers from the World Gold Council // Utilisegold.com. Utilisegold.com, 20 януари 2000. Посетен на 5 април 2009. (на английски)
- Gold Jewellery Alloys > Utilise Gold. Scientific, industrial and medical applications, products, suppliers from the World Gold Council // Utilisegold.com, 20 януари 2000. Посетен на 5 април 2009. (на английски)
- FAQs // gold.org. World Gold Council, 2012. Посетен на 17 ноември 2012. (на английски)
- Lide, D. R. Magnetic susceptibility of the elements and inorganic compounds // CRC Handbook of Chemistry and Physics. 86th. Boca Raton (FL), CRC Press, 2005. ISBN 0-8493-0486-5. (на английски)
- Kelly, P.F. Properties of Materials. CRC Press, 2015. ISBN 978-1-4822-0624-1. p. 355. (на английски)
Периодична система на елементите
| |||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| H | He | ||||||||||||||||||||||||||||||||||||||||
| Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||||||||||||
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||||||||||||||||||||||||
| Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | ||||||||||
| Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | ||||||||||
| |||||||||||||||||||||||||||||||||||||||||


